Материал: экз патан кафедра 1 (2)
Мікроскопічно
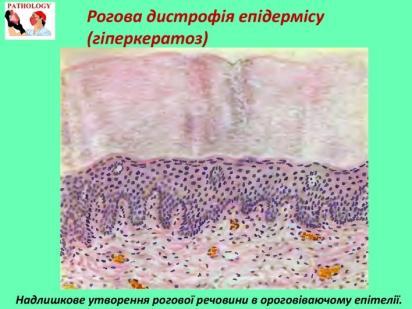
При гіперкератозі :
потовщення епідермісу в результаті гіперплазії клітин мальпігієвого шару й надмірного накопичення рогової речовини.
В слизових оболонках шкіряного типу і в епідермісі шкіри можлива поява сосочкоподібних потовщень внаслідок гіперплазії шару шипуватих клітин і подовження шипуватих відростків (акантоз).
При гіпокератозі та паракератозі :
виражена атрофія зернистого шару шкіри.
Роговий шар рихлий з дискомплексованими клітинами, що мають палочкоподібні ядра.
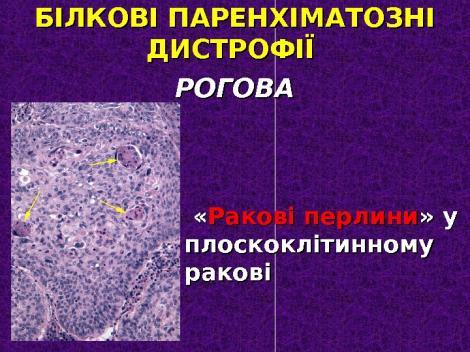
При патологічном зроговінні :
-
метаплазію однорядного секреторного епітелію в багаторядний зроговілий плоский епітелій.
Наслідки
Рогова дистрофія – процес оборотний, але новонароджені тварини з іхтіозом як правило гинуть в перші дні життя. Часто ускладнюється вторинною інфекцією, а лейкоплакія може стати джерелом розвитку пухлин (папілом, рідше – раку).
Дистрофії. Білкові паренхіматозні дистрофії. Гідропічна дистрофія. Визначення. Механізм розвитку. Морфологічна характеристика. Наслідки.
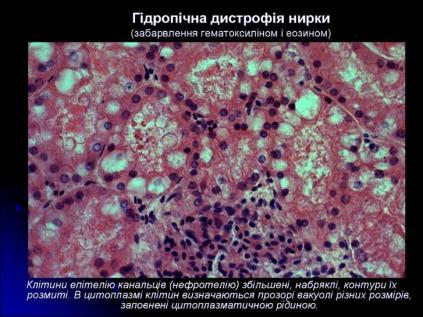
Цей вид дистрофії називається ще водянковою, або вакуольною. Найчастіше спостерігається в епітелії шкіри й ниркових канальців, клітинах печінки, м'язових і нервових клітинах. Характеризується появою в клітині вакуолей, які заповнені цитоплазматичною рідиною.
Механізм розвитку
Розвивається внаслідок гіпоксії тканин у зв’язку зі звільненням і затримкою в клітині зв’язаної води та надходженням води з тканинної рідини, крові й лімфи внаслідок підвищення колоїдно-осмотичного тиску й порушення проникливості клітинних мембран.
В нирках зумовлена ураженням гломерулярного фільтра, в печінці при гепатитах.
Морфологічна характеристика
Макроскопічно несуттєві зміни , звичайно ця дистрофія виявл. при мікроскопічному дослідженні.
Мікроскопічно
-
Клітини збільшені в об’ємі
-
Цитоплазма заповнена вакуолями з прозорою рідиною
-
Ядро зміщене на периферію, іноді у ньому з’являються вакуолі або воно зморщується.
-
Клітина перетворюється на балони, заповнені рідиною, в якій плаває пухиревидне ядро.
Наслідки – фокальний/тотальний колікваційний некроз (балонна дистрофія).
Дистрофії. Жирові паренхіматозні дистрофії. Визначення. Причини. Класифікація. Механізм розвитку. Морфологічна характеристика. Наслідки.
Паренхіматозні жирові дистрофії - це структурні прояви порушення обміну цитоплазматичних ліпідів, які можуть виражатися в накопиченні жиру у вільному стані в клітинах, де він присутній і в нормі,в появі ліпідів там, де вони зазвичай не зустрічаються, і в синтезі жирів незвичайного хімічного складу.
Причини
-
Тканинна гіпоксія
-
Важкі або тривалі за перебігом інфекції
-
Інтоксикації
-
Авітамінози, нераціональне харчування
Класифікація
-
Набуті
-
Спадкові (системні ліпідози)
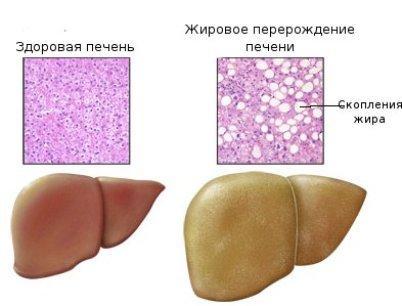
Жирова дистрофія печінки проявляється різким збільшенням вмісту і зміною складу жиру в гепатоцитах. У клітинах печінки спочатку з'являються гранули ліпідів (пиловидне ожиріння), потім дрібні краплі (дрібнокрапельне ожиріння), які в подальшому зливаються у великі краплі (крупнокрапельне ожиріння) або в одну жирову вакуоль, яка заповнює всю цитоплазму і відсуває ядро на периферію. Змінені таким чином печінкові клітини нагадують жирові. Частіше відкладення жиру в печінці починається на периферії, рідше - в центрі часточок; при значно вираженій дистрофії ожиріння клітин печінки має дифузний характер.
Макроскопічно печінка при жировій дистрофії
-
Збільшена
-
Недокрівна
-
Тістоподібної консистенції
-
Має жовтий або охряно-жовтий колір, з жирним блиском на розрізі.
-
При розрізі на лезі ножа і поверхні розрізу видно наліт жиру.
Причини жирової дистрофії печінки:
1) Збільшення мобілізації жиру в жировій тканині, що призводить до збільшення кількості жирних кислот, які досягають печінки, наприклад, при голодуванні і цукровому діабеті;
2) коли швидкість перетворення жирних кислот в тригліцериди в клітині печінки збільшена через підвищену активність відповідних ферментних систем. Це - головний механізм впливу алкоголю, який є потужним стимулятором ферментів.
3) коли зменшене окислення тригліцеридів до ацетил-КоА і кетонових тіл в органах, наприклад, при гіпоксії, і принесений потоком крові і лімфи жир не окислюється - жирова інфільтрація;
4) коли синтез білків-акцепторів жирів недостатній. Таким шляхом виникає жирова дистрофія печінки при білковому голодуванні і при отруєнні деякими гепатотоксинами, наприклад, чотирьоххлористим вуглецем і фосфором.
Типи жирової дистрофії печінки:
a. Гостра жирова дистрофія печінки . При гострій жировій дистрофії печінки тригліцериди накопичуються в цитоплазмі як маленькі, обмежені мембраною вакуолі (дрібнокрапельна жирова дистрофія печінки).
b. Хронічна жирова дистрофія печінки. Може виникати при хронічному алкоголізмі, недоїданні та при отруєнні деякими гепатотоксинами. Жирові краплі в цитоплазмі з'єднуються, формуючи значно більші вакуолі (крупнокрапельна жирова дистрофія печінки).
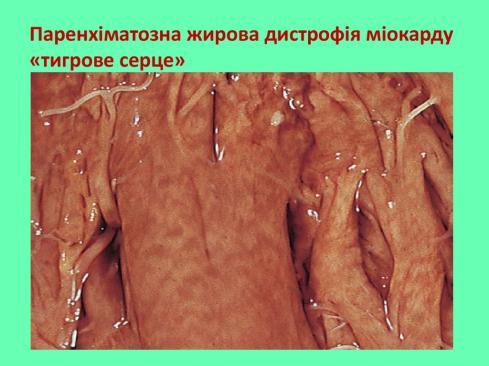
Жирова дистрофія міокарда характеризується накопиченням тригліцеридів в міокарді.
Причини жирової дистрофії міокарда:
- Хронічні гіпоксичні стани, особливо при вираженій анемії. При хронічній жировій дистрофії жовті смуги чергуються з червоно-коричневими ділянками («тигрове серце»). Клінічні ознаки в основному не дуже виражені.
- Токсичне ураження, наприклад, дифтеритический міокардит, викликає гостру жирову дистрофію.
Макроскопічно :
-
серце в'яле
-
дифузне жовте забарвлення
-
серце виглядає збільшеним в обсязі, камери його розтягнуті.
Мікроскопічно:
-
Більшість мітохондрій розпадається
-
поперечна смугастість волокон зникає
-
поява в м'язових клітинах дрібненьких жирових крапель (пиловидне ожиріння). При наростанні змін краплі (дрібнокрапельне ожиріння) повністю заміщають цитоплазму. Процес має вогнищевий характер і спостерігається в групах м'язових клітин, розташованих за ходом венозного коліна капілярів і дрібних вен, частіше субендо-і субепікардіально.
-
ТИГРОВЕ СЕРЦЕ
У нирках при жировій дистрофії
Макроскопічно:
-
вони збільшені
-
в'ялі (при поєднанні з амілоїдозом щільні)
-
кіркова речовина набрякла, сіра з жовтим крапом, помітним на поверхні та розрізі.
Механізм розвитку жирової дистрофії нирок пов'язаний з інфільтрацією епітелію ниркових канальців жиром при ліпемії і гіперхолестеринемії (нефротичний синдром), що веде до загибелі нефроцитів.
Наслідки
-
Залежать від глибини процесу
-
Оборотна якщо вона не супроводжується грубою поломкою клітинних структур
-
Глибоке порушення обміну клітинних ліпідів в більшості випадків закінчується смертю клітини.

Дистрофії. Вуглеводні паренхіматозні дистрофії. Визначення
Причини. Класифікація. Механізм розвитку. Морфологічна характеристика. Наслідки.
Паренхіматозні вуглеводні дистрофії пов'язані з порушенням обміну глікогену чи глікопротеїдів.
Порушення обміну глікогену
Порушення вмісту глікогену проявляється в зменшенні чи збільшенні кількості його в тканинах або появі там, де він звичайно не виявляється. Ці порушення найбільш яскраво виражені при цукровому діабеті і при спадкоємних вуглеводних дистрофіях - глікогенозах.
При цукровому діабеті спостерігають недостатнє вироблення інсуліну, що пов'язують з патологією бета-клітин острівців підшлункової залози. При цьому відбувається недостатнє використання глюкози тканинами, збільшення її вмісту в крові (гіперглікемія) і виведення із сечею (глюкозурія). Тканинні запаси глікогену різко зменшуються. Це в першу чергу стосується печінки, у якій порушується синтез глікогену, що веде до інфільтрації її жирами - розвивається жирова дистрофія печінки, в ядрах гепатоцитів з'являються включення глікогену, вони стають світлими ("порожні" ядра - симптом "дірчастих ядер").
З глюкозурією пов'язані характерні зміни нирок при діабеті. Вони виражаються в глікогенній інфільтрації епітелію канальців, головним чином вузького і дистального сегментів (морфогенетичний механізм - спотворений синтез). Епітелій стає високим, зі світлою пінистою цитоплазмою; зерна глікогену спостерігають у просвіті канальців. Зазначені зміни відбивають стан синтезу глікогену (полімеризація глюкози) у канальцевому епітелії при резорбції багатого глюкозою ультрафільтрату плазми. При діабеті страждають не тільки ниркові канальці, але і капілярні петлі клубочків, базальна мембрана яких стає більш проникливою для цукрів і білків плазми. Виникає один із проявів діабетичної мікроангіопатії - діабетичний гломерулосклероз.
Спадкові вуглеводні дистрофії, в основі яких лежать порушення обміну глікогену, називаються глікогенозами. Глікогенози обумовлені відсутністю чи недостатністю ферменту, що приймає участь у розщепленні депонованого глікогену, і відносяться тому до спадкоємних ферментопатій, чи хворобам накопичення. В даний час гарно вивчені 6 типів глікогенозів, обумовлених спадкоємною недостатністю 6 різних ферментів. Це хвороби Гірке (І тип), Помпе (ІІ тип), Мак-Ардля (V тип) і Герса (VІ тип), при яких структура глікогену, що накопичується в тканинах, не порушена, і хвороби Форбса-Корі (ІІІ тип) і Андерсена (ІV тип), при яких вона різко змінена.
Морфологічна діагностика глікогеноза того чи іншого типу можлива при дослідженні біопсії за допомогою гістоферментних методів, а також з урахуванням локалізації глікогену, що накопичується.
Вуглеводні дистрофії, зв'язані з порушенням обміну глікопротеїдів
При порушенні обміну глікопротеїдів у клітинах чи у міжклітинній речовині відбувається накопичення муцинів і мукоїдів. У зв'язку з цим при порушенні обміну глікопротеїдів говорять про слизову дистрофію.
Мікроскопічна картина: спостерігається накопичення слизу, загибель секретуючих клітин і їхня десквамація; обтурація слизом вивідних проток залоз веде до розвитку кіст. Нерідко в цих випадках приєднується запалення. Слиз може закривати просвіти бронхів, наслідком чого є виникнення ателектазів і осередків пневмонії. Іноді в залозистих структурах накопичується не слиз, а слизеподібні речовини (псевдомуцини). Ці речовини можуть ущільнюватися і приймати характер колоїду. Тоді говорять про колоїдну дистрофію, що спостерігається, наприклад, при колоїдному зобі.
Причини слизової дистрофії різноманітні, але найчастіше це запалення слизових оболонок у результаті дії різних патогенних подразників (катаральне запалення).
Слизова дистрофія лежить в основі спадкоємного системного захворювання муковісцидоза, для якого характерна зміна якості слизу, що виробляється епітелієм слизових залоз: слиз стає густим і в'язким, він погано виводиться, що обумовлює розвиток ретенційних кіст і склерозу (кістозний фіброз). Уражаються екзокринний апарат підшлункової залози, залози бронхіального дерева, травного і сечового тракту, жовчних шляхів, потові і слізні залози.
Для того щоб виявити вуглеводи в клітинахорганізму, проводять специфічний тест - ШИК-реакцію. Суть її в тому, що тканина обробляють йодною кислотою, а потім фуксином. І все альдегіди стають червоними. Якщо потрібно виділити глікоген, то до реактивів додають амилазу. Глікозаміноглікани і глікопротеїди фарбуються метиленовим синім. Паренхіматозні вуглеводні дистрофії пов'язані, як правило, з порушенням обміну глікогену і глікопротеїдів.
Наслідки значною мірою визначаються ступенем і тривалістю підвищеного слизеутворення. В одних випадках регенерація епітелію приводить до повного відновлення слизуватої оболонки, в інших – в ній розвивається атрофія з переходом у склероз, що суттєво влпиває на функцію органа.
Дистрофії. Стромально-судинні дистрофії. Визначення. Причини, класифікація. Механізм розвитку.
Дистрофія (від. грец. dys — порушення і trophe — харчую) — складний патологічний процес, в основі якого лежить порушення тканинного (клітинного) метаболізму, що приводить до структурних змін.
Стромально-судинні (мезенхімальні) дистрофії – структурні прояви порушення обміну речовин в сполучній тканині, що виявляються в стромі органів, стінках судин та розвиваються на території гістіона
Гістіон – структурно-функціональна одиниця сполучної тканини, що
складається з відрізка мікроциркуляторного русла із оточуючими його елементами
Причини:Порушення обміну речовин в сполучній тканині( стромі органів і стінках судин)
(Более подробно причины будут рассмотрены дальше. В других вопросах)
Класифікація
В залежності від виду порушеного обміну мезенхімальні дистрофії поділяються на:
-
Білкові(диспротеїнози)
-
Жирові(ліпідози)
-
Вуглеводні
Механізм розвитку
-
Неадекватне надходження та накопичення продуктів метаболізму, які надходять з кров’яного або лімфатичного русла(інфільтрація)
-
Дезорганізація основної речовини та волокон сполучної тканин (декомпозиція(фанероз))
-
Поява та накопичення аномальних речовин(спотворений синтез)
Дистрофії. Білкові стромально-судинні дистрофії. Визначення, причини, класифікація. Механізм розвитку
Диспротеїнози – структурні прояви порушення обміну білків в сполучній тканині, що виявляються в стромі органів, стінках судин
До стромально-судинних диспротеїнозів відносять мукоїдне, фібрино’їдне набухання, гіаліноз, амілоїдоз.(класифікація)
Досить часто мукоїдне і фібриноїдне набухання та гіаліноз є послідовними стадіями дезорганізації сполучної тканини.
Механізм розвитку:
- накопичення продуктів плазми крові в основній речовині в результаті підвищення тканинної-судинної проникності (плазморагія) (інфільтрація)
- деструкція елементів сполучної тканини і утворення білкових (білково-полісахаридних) комплексів (декомпозиція)
Амілоїдоз утворення аномального фібрилярного білку, що синтезується клітинами амілоїдобластами(спотворений синтез)
Причини: мукоїдне, фібріноідне набухання і гіаліноз: інфекційно-алергі-
чні захворювання, гіпоксія, імунопатологічні процеси, ангіо-
невротичні реакції, ендокринопатії, порушення харчування, генетичні фактори.
Морфогенез стромально-судинних диспротеїнозів представлений на малюнку

Причини амілоїдозу:
Системні амілоїдози:1)Плазмоклітинні дискразії(первинний амілоїдоз. (AL-амілоїд) наприклад, у хворих на мієлому. Також коли причина не з’ясована кажуть про ідіопатичний амілоїдоз), 2)як ускладнення первинного захворювання(хронічні запальні захворювання – наприклад, туберкульоз. Це вторинний або набутий амілоїдоз(АА-амілоїд)), 3)внаслідок тривалого гемодіалізу( амілоїдоз, пов’язаний з гемодіалізом)(Аβ2m-амілоїд), 4)внаслідок тривалого накопичення амілоїдогенних білків(ATTR-амілоїд), які накопичуються у людей старечого віку(Системний старечий амілоїдоз), 5)наявність мутантних генів, які кодують амілоїдогенні білки(Спадковий(сімейнний) амілоїдоз. Наприклад, сімейна середземноморська лихорадка, сімейні нейропатії)
Локальні амілоїдози:1)доброякісні скупчення моноклональних В-клітин або плазматичних клітин, які виробляють легкі ланцюги імуноглобулінів(відкладання AL-амілоїда у органах дихання, шкірі, сечополовій системі),2) ендокринні пухлини(надмірне вироблення білків ендокринними залозами)(ендокринний амілоїдоз),3) накопичення амілоїда(Аβ-білка) у мозку з білків-попередників(старечий церебральний амілоїдоз, хвороба Альцгеймера)
Дистрофія. Білкові стромально-судинні дистрофії. Мукоїдне набухання. Визначення. Механізм розвитку. Морфологічна характеристика. Наслідки.
Мукоїдне набухання — поверхнева й оборотна дезорганізація
сполучної тканини.
Механім розвитку:
-
в основній речовині накопичуються і перерозподіляються глікозаміноглікани за рахунок збільшення вмісту гіалуронової кислоти.
-
Глікозаміноглікани мають гідрофільні властивості, і накопичення їх обумовлює підвищення тканинної та судинної проникності.
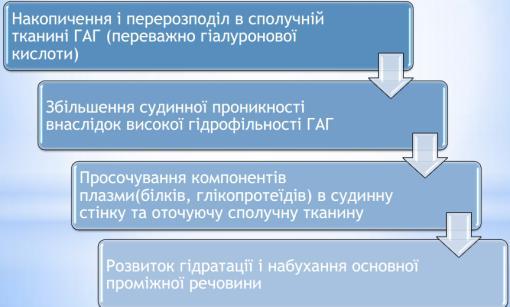
(ГАГ-глікозамінглікани)
Морфологічна характеристика
При мікроскопічному дослідженні
-
основна речовина базофільна
-
при офарбленні толуїдиновим синім — бузкового або червоного кольору
-
При фарбуванні пікрофуксином колагенові волокна виглядають жовто-помаранчевими, а не цегляно-червоними
-
Виникає феномен метахромазії, в основі якого лежить зміна стану основної проміжної речовини з накопиченням хромотропних речовин.
-
Колагенові волокна зазвичай зберігають пучкову будову, але набухають і піддаються фібрилярному разволокненню. Вони стають малостійкими до впливу колагенази..
-
Мукоїдне набухання частіше в стінках артерій, клапанах серця, ендо- і перикарді, тобто
там, де хромотропні речовини зустрічаються і в нормі;
-
Зовнішній вигляд тканини або органу при мукоїдному набуханні не змінюється(макроскопічно не змінюється); характерні зміни виявляються за допомогою гістохімічних реакцій при мікроскопічному дослідженні.
Наслідки мукоїдного набухання можуть бути різними: повне відновлення тканини або перехід в фібриноїдне набухання. Функція органів при цьому порушується (наприклад, порушення функції
серця при розвитку ревматичного ендокардита — вальвуліта).

Дистрофія. Білкові стромально-судинні дистрофії. Фібриноїдне набухання. Визначення. Механізм розвитку. Морфологічна характеристика. Наслідки.
Фібриноїдне набухання — глибока і необоротна дезорганізація сполучної тканини, в основі якої лежить деструкція її основної речовини і волокон, яка супроводжується різким підвищенням судинної проникності та утворенням фібриноїду.
Механізм розвитку:
-
виражений процес деполімеризації глікозаміногліканів, глибоке порушення судинної проникності, просочування стінки судин не тільки альбумінами і глобулінами, а й фибриногеном плазми (відсюди термін фибриноїдное набухання, фібриноїд).
-
Фібриноїд являє собою складну речовину,
-
входять в фібриноїд білки і полісахариди з колагенових волокон, які розпадаються, основної речовини і плазми крові, нуклеопротеїди. обов’язковим його компонентом є фібрин


Морфологічна характеристика
При мікроскопічному дослідженні :
-
пучки колагенових волокон, які просочені білками крові гомогенні, вони утворюють з фібрином нерозчинні міцні сполуки;
-
стають еозинофільними; пікрофуксином
-
офарблюються в жовтий колір, різко РАS-позитивні та піронінофільні при реакції Браше, а також, аргірофільні при імпрегнації солями срібла.
-
Метахромазія сполучної тканини при цьому не виявляється, або мало виражена як результат деполімеризації глікозаміногліканів основної речовини.