Материал: Екстракційне відділення виробництва фосфатної кислоти напівгідратним способом
Екстракційне відділення виробництва фосфатної кислоти напівгідратним способом
Міністерство освіти і науки України
Національний університет Львівська політехніка
Кафедра
ХТНР
Курсовий проект
Екстракційне
відділення виробництва фосфатної кислоти напівгідратним способом
Виконала:
ст. гр. ТНРс-11
Капущак Н.Б.
Перевірила:
доц. Зозуля Г.І.
Львів-2014
Зміст
Вступ
. Аналітичний огляд
.1 Термічний спосіб одержання фосфатної кислоти
.2 Екстракційний спосіб одержання фосфатної кислоти
. Технологічна частина
.1 Фізико-хімічні основи екстракційного способу одержання фосфатної кислоти
.2 Технологічна схема виробництва екстракційної фосфатної кислоти дигідратним способом
.3 Розрахункова частина
.3.1 Матеріальний розрахунок розміщення апатитового концентрату
.3.2 Матеріальний розрахунок екстрактора
.3.3 Тепловий розрахунок екстрактора
.3.4 Розрахунок екстрактора
.4 Техніка безпеки і протипожежні заходи
.5 Екологічна частина
.5.1 Переробка фосфогіпсу
.5.2 Отримання H2SO4 з відходів виробництва сірчаної кислоти
.5.3 Утилізація фторовмісних газів
Висновки
Список
використаної літератури
Вступ
фосфатний кислота екстракційний утилізація
Фосфатна кислота (ФК) - гігроскопічні без кольору кристали моноклинної сингонії, з густиною 1,88 г/см3. Температура плавлення 42,50°С. Розпливчаста на повітрі. У розплавленному стані переохолоджується; за 15°С утворює густу оліїсту рідину, а за -121°С - склоподібну масу. Найстабільніша сполука в ряду ки- сневмісних кислот Фосфору. Фосфатна кислота змішується з водою у будь-яких співвідношеннях. З висококонцентрованих розчинів кристалізується у вигляді гемігідрату (напівгідрату), що являють собою безколірні кристали моноклинної сингонії. Фосфатна кислота - сильна кислота, за нормальних умов - малоактивна й реагує тільки з карбонатами, гідроксидами та деякими металами. У процесі дії на поверхню металу розчином ФК, що містить цинк або марганець, утворюється захисна плівка.
Фосфатну кислоту застосовують в основному
(близько 85% виробленої) для одержання фосфорних і складних добрив, кормових
фосфатів, синтетичних миючих і водопом'якшувальних засобів. У металообробній
промисловості фосфатну кислоту застосовують в процесі фосфатування поверхні
металів, а в текстильній - для оброблення та фарбування вовни, натуральних і
синтетичних волокон. У технології органічних речовин її використовують як
каталізатор. Фосфатну кислоту і її похідні застосовують у процесі готування
бурових суспензій при нафтовидобутку, у виробництві скла, у фотографії (для
готування світлочутливих емульсій), у медицині (виготовлення медикаментів,
одержання лікарських, засобів, зубних цементів), у процесі оброблення деревини
(для додання вогнестійкості). Похідні фосфатної кислоти застосовують також у
харчовій промисловості (хлібопекарські порошки, виробництві плавлених сирів, у
ковбасному виробництві й цукроварінні) [1].
. Аналітичний огляд
Фосфорна кислота - тверда безбарвна речовина. Кристалічна фосфорна кислота - гігроскопічне з'єднання, розпилюється на повітрі і з водою змішується у будь-яких співвідношеннях. Розбавлені розчини фосфорної кислоти мають кислуватий смак
Як трьохосновна, фосфорна кислота відноситься до слабких кислот. Теплоти і вільні енергії іонізації показують, що перший ступінь дисоціації Н3РО4 протікає з екзотермічним, а остання - з ендотермічним ефектом. Хімічні властивості фосфорної кислоти схожі з іншими кислотами. Кристалічна Н3РО4 відома у вигляді безводої Н3РО4 і напівгідрату Н3РО4-0, 5Н2О. Чиста фосфорна кислота утворює призматичні кристали моноклінної системи, що легко розпливається на повітрі, кристалізується досить повільно, і концентровану Н3РО4можно легко переохолоджувати до отримання скла.
Показано, що в розчині Н3РО4 має місце обмін між атомами кисню між іонами РО43- і Н2О. В процесі термічної дисоціації Н3РО4 можуть утворюватися її дигидратировані форми піро- і метафосфорної кислоти, а також існують поліфосфатні кислоти (пиро-, три-, мета-, ангидридомета-, тетраполі -, триполі-, пиро-, отрофосфорная кислоти). Фосфорну кислоту отримують у вигляді густої, сироподібної рідини, з якої при охолодженні можуть виділити кристалічний продукт. У багатьох випадках кристалізація відбувається тільки при внесенні приманки [2].
Найбільш поширеними способами промислового
виробництва фосфорної кислоти є термічний і кислотний.
.1 Термічний спосіб одержання фосфатної кислоти
Термічний спосіб одержання фосфатної кислоти ґрунтується на окисненні елементного фосфору в надлишку повітря з наступною гідратацією й абсорбцією Р4О10, що утворюється, конденсацією фосфатної кислоти й уловлюванням туману з газової фази.
Одержують Р4О10 окисненням елементного фосфору у вигляді крапель або плівки. Ступінь окиснення Фосфору в промислових умовах визначається температурою в зоні окиснення, дифузією компонентів та інших чинників. Другу стадію одержання термічної фосфатної кислоти - гідратацію декаоксиду тетрафосфору - здійснюють абсорбцією кислотою (водою) або взаємодією пари Р4О10 з водяною парою. Гідратація Р4О10 відбувається послідовно до мета-, ди- і ортофосфатної кислоти:
O10 + 2nH2O = 4(HPO3)n (за 700 С) (1.1)
(HPO3)n + 2nH2O = 2nH4P2O7 (за 450 С) (1.2)
nH4P2O7 + 2nH2О = 4nH3PO4 (нижче 230 C) (1.3)
Сумарне рівняння процесу гідратації
O10 + 6H2O = 4H3PO4 (1.4)
Кількість теплоти, що виділяється в процесі спалювання 1 кг елементного фосфору, становить 23614 кДж, а в процесі гідратації - 3035 кДж. У процесі розведення фосфатної кислоти водою до концентрації продукційної (товарної) кислоти виділяється додаткова кількість теплоти.
Термічну фосфатну кислоту можна одержувати двома способами: одноступінчастим і двоступінчастим. Перший спосіб заснований на спалюванні фосфоровмісного газу, який відходить з печі (без попередньої конденсації пари фосфору), з гідратацією утвореного Р4О10. Спосіб не застосовують через низьку концентрацію парів фосфору в пічному газі, що потребує громіздкого устатку- вання для його перероблення, а домішки, які містить газ, забруднюють одержувану фосфатну кислоту.
Термічну фосфатну кислоту виробляють двостадійним способом. При цьому конденсують з газу фосфорної печі фосфор, а потім переробляють його у фосфатну кислоту.
У процесах окиснення Фосфору і гідратації Р4О10 виділяється значна кількість теплоти. Залежно від принципу охолодження газів існують три способи виробництва термічної фосфорної кислоти: випарний, циркулянійно-випарний, теплообмінно-випарний. Випарні системи, засновані на відведенні теплоти при випаровуванні води або розведеної фосфатної кислоти, найпростіший в апаратурному оформленні. Однак, через відносно великий об'єм відхідних газів вважається, що використання таких систем доцільне лише в установках невеликої одиничної потужності.
Циркуляційно-випарні системи дають змогу
сполучити в одному апараті стадії спалювання елементного фосфору, охолодження
газової фази циркулюючою кислотою і гідратації Р4О10. Розглянуті системи
поєднують два способи відведення теплоти: через стінку башт спалювання й
охолодження, а також випаровуванням води з газової фази. Істотною перевагою
системи є відсутність контурів циркуляції кислоти з насосно-холодильним
устаткуванням. Сьогодні на заводах експлуатують технологічні схеми з
циркуляційно-випарним способом охолодження (двобаштова система), що
відрізняються наявністю додаткової башти для охолодження газу. Виробництво
термічної фосфорної кислоти (ТФК) є дорогим і безперервно скорочується, а
замість неї в технології використовують дешевшу очищену екстракційну фосфатну
кислоту (ЕФК) [3].
.2 Екстракційний спосіб одержання фосфатної
кислоти
Кислотний метод грунтований на витісненні сильними кислотами фосфорної кислоти з фосфатів. Найбільше поширення на практиці знайшов метод сульфатнокислої екстракції основні стадії виробництва екстракційної фосфорної кислоти (ЕФК)
Процес протікає по наступному сумарному
рівнянню:
Ca5F(PO4)3 + 5H2SO4 = 5CaSO4(тв) + 3Н3РО4 + HF.
Залежно від температури процесу і концентрації Р2О5 в розчині сульфат кальцію (фосфогіпс) виділяється у вигляді CaSO4 - 2H2O (дегідратнbй режим), СаSO4 - 0,5 H2O (режим напівгідрату) і СаSO4 (ангідридовий режим). Промислове поширення знайшли перші два режими.
Початкову екстракційну фосфатну кислоту, на відміну від термічної, без проведення очищення використовують тільки для виробництва обмеженого ряду продуктів (виробництва мінеральних добрив, технічних солей). Тому розробка технології глибокого очищення ЕФК на сьогодні є дуже актуальною, економічно доцільною і затребувана у зв'язку з безперервним зростанням виробництва екстракційної фосфорної кислоти.
Основними перевагами екстракційного процесу є
його простота і можливість виробництва дешевшої Н3РО4. Недолік - отримувана
екстракційна фосфатна кислота забруднена домішкою полуторних оксидів (Al2O3,
Fe2O3), з'єднаннями фтору і СаSO4 [4].
2. 2. Технологічна частина
Сірчанокислотне розкладання фосфатної сировини у
виробництві ЕФК відрізняється від розкладання при отриманні простого
суперфосфату більш високою нормою сірчаної кислоти, яка подається з розрахунку
на зв'язування всього кальцію у вигляді СaSO4, при цьому Р2О5 переходить в
розчин (у вигляді Н3РО4), який відокремлюється від осаду фільтрацією.
.1 Фізико-хімічні основи екстракційного способу
одержання фосфатної кислоти
Екстракційний спосіб одержання фосфатної кислоти грунтується на розкладанні природних фосфатів сульфатною кислотою за реакцією
F(PO4)3 + 5H2SO4 + 5nH2O = 5CaSO4 · nH2O +
3H3PO4 + HF (2.1)
Одночасно відбувається розкладання й інших домішок у вихідній фосфатній сировині. До них належать: кальцит, доломіт, сидерит, глауконіт, феруму й алюмінію силікати. Вони також розкладаються сульфатною кислотою за схемою:
· MgCO3 + 2H2SO4 + (n - 2)H2O = CaSO4 · nH2O +MgSO4 + 2CO2 (2.2)O · Na2O · Al2O3 · 2SiO2 + 5H2SO4 =
=Na2SO4 + K2SO4 + Al2(SO4)3 + 2SiO2 + 5H2O.
(2.3)
Діоксид силіцію реагує з HF, утворюючи SiF
+ 4HF = SiF4 + 2H2O. (2.4)
+ 2HF = H2SiF6. (2.5)
Розкладання домішок призводить до збільшення витрати сульфатної кислоти, а також знижує ступінь вилучення Р205 у цільовий продукт, унаслідок утворення нерозчинних фосфатів заліза з концентрацією Р205 вищою за 40% та FeP04 · 2,5Н20- з нижчими концентраціями. Діоксид карбону, що виділяється у процесі розкладання карбонатів, утворює в екстракторах стійку піну. Розчинні фосфати Магнію, Феруму й Алюмінію знижують активність вихідної фосфатної кислоти, а також зменшують вміст засвоюваних форм P2O5 у добривах з наступною переробкою фосфатної кислоти.
З урахуванням впливу домішок фосфати з підвищеним вмістом сполук Феруму, Алюмінію, Магнію й карбонатів непридатні для виробництва фосфатної кислоти. Тому в процесах сульфатнокислотного розкладання зазвичай застосовують руди або концентрати, що характеризуються масовим відношенням Fe2О3 : Р2O5 не більше 0,08.
Основою для вибору технологічних параметрів процесів сульфатнокислотного розкладання є виділення сульфату кальцію у вигляді досить великих, легковідокремлюваних кристалів, що відмиваються добре від фосфатної кислоти. У системі CaS04 - Н3РO4 - Н20 кальцію сульфат може існувати в трьох формах: однієї безводної (ангідриту CaS04) і двох кристалогідратів (гемігідрату CaS04 • 0,5Н20 і дигідрату або гіпсу CaS04 • 2Н20). Температурні й концентраційні зони кристалізації наведених форм визначаються співвідношеннями їх розчинностей у фосфатній кислоті або співвідношеннями тисків пари над розчином і тисків дисоціації оборотних реакцій перетворення гіпсу в гемігідрат або ангідрит і гемігідрату в ангідрит. З ізотерм розчинності сульфату кальцію за 80°С (рис. 2.1) видно, що зі збіль- шенням вмісту фосфатної кислоти розчинність усіх трьох модифікацій спочатку зростає, досягає максимуму за 16-22% P2O5, а потім зменшується.
Мінімальну розчинність за 80°С має ангідрит, що є рівноважною твердою фазою. Метастабільний гіпс у розчинах, що містять 33,3% P2O5 (точка перетину ізотерми метастабільних кристалогідратів), перетворюється безпосередньо в ангідрит. У більш концентрованих розчинах спочатку відбувається конверсія гіпсу в менш розчинний гемі гідрат, після чого останній дегідратується до ангідриту [5].
На рис. 2.2 наведена політермічна діаграма, що
характеризує напрямок і послідовність фазових перетворень кальцію сульфату в
системі CaSO4 - H3PO4 - H2O.
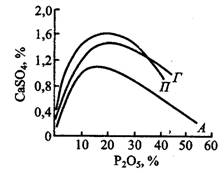
Рис. 2.1. Ізотерми розчинності
кальцію сульфату у фосфатній кислоті за 80°С: А - ангідрит; П - гемідрат; Г -
гіпс
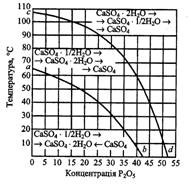
Рис. 2.2. Схема перетворень
кристалогідратів сульфату кальцію в розчинах фосфатної кислота
Стабільними твердими фазами в системі є гіпс (нижче кривої ab) й ангідрит (вище кривої ab). У зоні, розміщеній над кривою cd, гемігідрат, що здебільшого є першою фазою системи, яка кристалізується, переходить в ангідрит не безпосередньо, а спочатку оводнюється до гіпсу. Крива cd є безліччю точок співіснування цих метастабільних фаз за різних температур. Аналогічно крива аb є безліччю точок співіснування стабільних фаз гіпсу і дигідриту. Відповідно до правила Оствальда, нижче лінії аb стабільні фаза - гіпс, і послідовність перетворень має бути такою, як показано на рис. 2. На практиці утворення ангідриту не спостерігається і гемігідрат переходить у гіпс. Це пояснюється кінетичними причинами, що змінюють маршрути реакцій, наприклад, значно швидшим є перетворення ангідрит →гіпс, ніж гемігідрат → ангідрит, у даній області температур і концентрацій Р2О5. В інших умовах швидкість перетворення ангідриту може бути меншою. На швидкість і маршрут взаємних переходів можуть впливати також іони домішок.
Отже, ступінь гідратації кальцію сульфату, відокремлюваного у процесі екстракції, може не відповідати стабільним формам і залежить від конкретних умов здійснення процесу. На рис.2.3 наведена діаграма, що показує практичний ступінь гідратації сульфату кальцію залежно від технологічного режиму процесу екстракції, і передусім від температури й концентрації фосфатної кислоти.
Як видно з рис 3, у зоні нижче кривої 2 кальцію сульфат відокремлюється у вигляді гіпсу, вище кривої 1 - у вигляді ангідриту, а між цими лініями -у вигляді гемігідрату.
У виробничих умовах осад забруднений
домішками P4O10 у вигляді нерозкладених фосфатів, невідмитої Н3РО4,
суміснокристалізованих фосфатів різних металів та ін. Тому сульфати кальцію, що
утворяться, називають відповідно фосфогіпс, фосфогемігідрат і фосфоангідрит.
Залежно від типу сульфату, що осаджується, розрізняють три способи одержання
екстракційної фосфатної кислоти: дигідратний, півгідратний (напівгідратний) та
ангідритний, а також комбіновані: гемігідратно-дигідратний і
дигідратно-гемігідратний. Найпоширеніший на практиці дигідратний режим, що
здійснюють за температури 65-80°С, одержуючи при цьому кислоту з вмістом до
30-32% Р2О5.
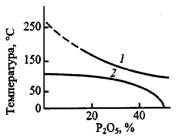
Рис. 2.3. Вплив температури та
вмісту Р205 у розчині на практичну гідратованість відокремлюваного осаду
кальцію сульфату
Гемігідратний метод, що здійснюється за температури 90-105°С, забезпечує одержання кислоти із вмістом до 50% Р205 (без додаткового упарювання). Відповідно до способу фосфатну кислоту, що містить 36-38% Р2О5, можна одержати з апатитового концентрату практично на тому самому обладнанні, що й у типовому дигідратному процесі з повітряним охолодженням суспензії. Гемігідратні процеси значного поширення поки що не одержали через високу температуру (80-100°С), виділення за цих температур гідрогену фториду в газову фазу, нижчого виходу Р2О5 у кислоту, ніж за дигідратного методу. В удосконалених промислових схемах передбачене попереднє змочування апатитової сировини у швидкісному змішувачі, поділення зон розкладання і кристалізації та ін. Проведення основної реакції при вмісті сульфатної кислоти у рідкій фазі суспензії 0,2-1,0% у першому реакторі і 2,0-3,0% у другому реакторі допомагає знизити кількість розчиненого CaS04 у продукційній фосфатній кислоті, значно зменшити заростання устаткування і трубопроводів, суттєво інтенсифікувати роботу основних технологічних вузлів.