Материал: Альонкіна К. В., Сотниченко Т. Д Хімія. Підготовка до ЗНО
тема 13. лужні та лужноЗемельні елементи
Калій потрібен у значній кількості для живлення рослин, тому його широко використовують як добриво у вигляді нітрату. Поташ K2CO3 використовують при виробництві скла та рідкого мила.
Кальцій
характеристика хімічного елемента
Кальцій перебуває в головній підгрупі II групи, належить до лужноземельних металів разом з Барієм та Стронцієм. У зовнішній оболонці він має два електрони й може легко віддавати їх, утворюючи йони зі стійкими конфігураціями інертних газів.
Поширеність у природі
Кальцій має велику хімічну активність, тому зустрічається в природі тільки у вигляді сполук. Найважливіші природні сполуки Кальцію: а) вапняк, мармур, крейда (CaCO3); б) гіпс (CaSO4 . 2H2O); в) фосфорит і апатит (Ca3 (PO4 )2 );г) доломіт (CaCO3 . MgCO3).
фізичні властивості
Кальцій — метал сріблясто-білого кольору, дуже легкий, як і лужні метали, але значно твердіший за них і має більш високу температуру плавлення (+851 °С). Кальцій зберігають під шаром гасу.
Добування
Кальцій добувають шляхом електролізу його розплавленого хлориду.
CaCl2 ел. струм→Ca +Cl2.
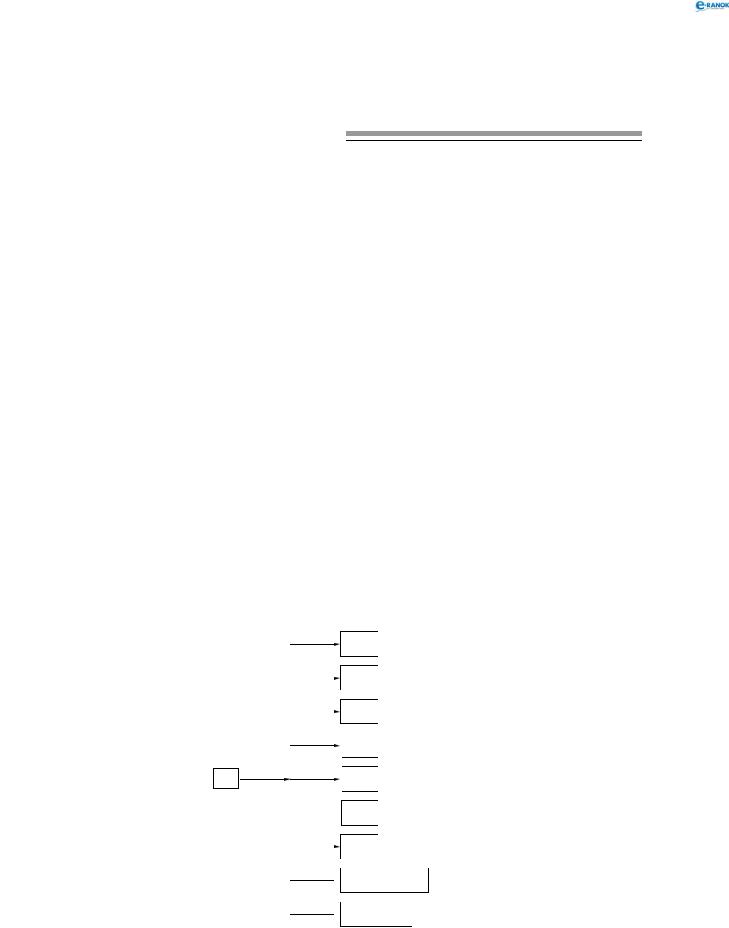
хімічні властивості
|
|
O2 |
|
|
|
CaO |
|
|
|
|
|
|
|
C, t° |
|
|
|
|
|
|
|
CaC2 |
|
|
|
|
|
|
|
Hal |
|
|
|
|
|
|
|
CaCl2 |
|
|
|
|
|
|
|
H2 |
|
|
|
CaH2 |
|
|
|
|
|
Ca |
+ |
S, t° |
CaS |
|
|
N2 , t°  Ca3N2
Ca3N2
P, t° |
Ca3 P2 |
|
H2O  Ca(OH)2 + H2↑
Ca(OH)2 + H2↑
HCl  CaCl2 + H2↑
CaCl2 + H2↑
Хімічні властивості Mg аналогічні.
95
www.e-ranok.com.ua
тема 13. лужні та лужноЗемельні елементи
Найважливішою сполукою Кальцію є його карбонат СаCO3. Він являє собою основну складову частину вапняку, мармуру, крейди, а також входить до складу доломіту (MgCO3 . СаCO3). Кальцій карбонат використовують у виробництві цементу, сталі, скла. Кальцій та кальцій карбід застосовують в органічній хімії. А ще Кальцій відіграє дуже важливу роль у біохімічних процесах, які протікають у живих організмах.
Магній застосовується для одержання легких сплавів, як відновник рідкісних металів і деяких неметалів (Si).
твердість води
Твердість води — це природна властивість води, обумовлена присутністю в ній розчинених солей Кальцію та Магнію. Сумарну концентрацію йонів Магнію й Кальцію називають загальною твердістю води. Розрізняють постійну й тимчасову твердість води, їхня порівняльна характеристика подана в таблиці.
характеристика
Причини твердості
Джерела твердої води
Усунення твердості
Тимчасова твердість, |
Постійна твердість, |
або карбонатна |
або некарбонатна |
Наявність розчинених гід- |
Наявність сульфатів, хлори- |
рогенкарбонатів Магнію |
дів або деяких інших солей |
Mg(HCO3 )2 й Кальцію |
Кальцію й Магнію (наприклад, |
Ca(HCO3 )2 |
CaSO4, MgCl2 та ін.) |
Річкові й озерні води, водо- |
Морська вода, вода солоних |
провідна вода, різні газовані |
озер, природні негазовані міне- |
мінеральні води |
ральні води |
Усувається при кип’ятінні, |
Не усувається при кип’ятінні, |
при додаванні кислот або |
але зникає при додаванні соди |
соди (Na2CO3 ) |
(Na2CO3 ) або при використанні |
|
йонообмінних смол |
Калійні добрива: K2CO3 – поташ; KNO3 – калійна селітра; KCl – калій хлорид; K2SO4 – калій сульфат; KCl ∙ NaCl – сильвініт.
96
www.e-ranok.com.ua

тема 13. лужні та лужноЗемельні елементи
виконайте контрольний тест
На його виконання відводиться 15 хвилин. Під час роботи над тестом не можна користуватися слов никами, підручниками, посібниками, довідниками тощо.
тест 26 (контрольний)
1. Укажіть формулу харчової соди.
А Na2CО3
Б NaCl
В NaHCO3
ГNaOH
2.Укажіть продукт взаємодії кальцію з водою.
А Ca(OH)2 |
+ H2O |
В CaO + H2 |
Б Ca(OH)2 |
+ H2 |
Г Ca(HCO3)2 |
3. Визначте пари речовин, що відповідають сполукам «Х1» та «Х2» у схемі перетворень:
Ca O→ Х1 → CaCl2 → Х2. А CaO та CaCO3
Б Ca(OH)2 та CaCO3
2та CaC2
ГCaO та H2O
4.Установіть відповідність між реагентами реакцій обміну та йонними рівняннями цих реакцій
ускороченому вигляді: В
А K |
SO |
+ Ba(NO |
) |
→ |
1 Al3+ + 3OH– =Al(OH) |
3 |
|||||||||
2 |
|
4 |
|
+ Na |
3 |
2 |
|
2 |
Ba2+ |
+ SO 2– |
= BaSO |
|
|
||
Б Ba(OH) |
CO |
3 |
4 |
|
|||||||||||
ВAlCl |
|
2 |
2 |
|
|
3 |
|
4 |
|
O |
|
||||
+ KOH→ |
|
|
H+ + OH– = H |
|
|
|
|||||||||
|
3 |
|
|
|
|
|
|
4 |
Ba2+ |
+ CO 2– |
2 |
|
|
|
|
Г NaOH + HCl→ |
|
|
= BaCO |
3 |
|
||||||||||
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
5. Установіть послідовність утворення речовин у ланцюгу перетворень лужноземельного металу на кальцій карбонат:
А CaCO3
Б Ca(OH)2 В Ca
ГCaO
6.Змішали 0,5 моль NaOH і 0,5 моль H2SO4. Обчислити масу солі.
97
www.e-ranok.com.ua

тема 14. алюміній
Тема 14. Алюміній
Перевірте свої знання
Виконайте тест 27. На його виконання відводиться 15 хвилин. Під час роботи над тестом не можна користуватися словниками, підручниками, посібниками, довідниками тощо.
тест 27 (вступний)
1. Укажіть найпоширеніший металічний елемент на Землі.
А Na |
В Fe |
Б Cu |
ГAl |
2. Укажіть формулу захисної плівки, що утворилася на поверхні алюмінію.
АAl4C3 |
ВAl2O3 |
БAl(OH)3 |
Г AlN |
3.У реакції з якою речовиною алюміній оксид виявляє властивості кислотного оксиду?
Алуг
Б кислота В вода
Гкислотний оксид
4.Установіть відповідність між реагентами реакцій та скороченозображеними схемами.
АAlCl |
+ Mg→ |
1 Al0 |
+… →Al3+ |
+H |
2 |
|||
|
3 |
|
|
2 Al |
|
|
|
|
БAl + HCl→ |
3+ +…→Al0 + Mg2+ |
|||||||
ВAl0 |
+ CuCl |
→ |
3 Al0 |
+ …→Al3+ |
+ Cu0 |
|||
ГAl0 |
+ Cl |
2 |
|
4 Al0 |
+ …→Al3+ |
|
|
|
→ |
|
|
|
|||||
|
|
2 |
|
|
|
|
|
|
5. Установіть послідовність утворення речовин у ланцюжку перетворень від алюмінію до алюміній гідроксиду
АAl
БAl(NO3)2 ВAl2O3 ГAl(OH)3
6. У результаті алюмінотермічного відновлення 320 г ферум (ІІІ) оксиду було добуто 170 г заліза. Яка масова частка виходу заліза (%)?
98
www.e-ranok.com.ua

тема 14. алюміній
теоретична частина
АлюмініЙ
Алюміній перебуває в головній підгрупі III групи, належить до рідкісноземельних металів. На його зовнішньому електронному шарі міститься три електрони, які він здатний віддавати.
Порівнюючи Алюміній з іншими елементами цієї підгрупи, можна відзначити неметалічність Бору, який стоїть після Берилію в періоді, металічні властивості Галію, із чого можна припустити амфотерності сполук Алюмінію, тобто проміжних (від металічних до неметалічних) властивостей цього елемента.
Алюміній — найпоширеніший метал на Землі (3-тє місце серед усіх елементів; 8% складу земної кори). У вигляді простої речовини він у природі не зустрічається; входить до складу багатьох сполук, які утворюють ґрунт: глиноземів (Al2O3) та бокситів (Al2O3 . xН2O).
Алюміній—сріблясто-білийметал.Вінковкий,легковитягуєтьсявдріт,tпл =+660°С,tкип =+2520°С. При кімнатній температурі алюміній не змінюється на повітрі, тому що його поверхня покрита тонкою оксидною плівкою, яка характеризується сильною захисною дією.
хімічні властивості
1) Взаємодія з киснем.
Алюміній є активним металом, тому на повітрі швидко реагує з киснем. Але перетворенню піддається тільки та частина алюмінію, яка перебуває на поверхні зразка, тому що продукт взаємодії — алюміній оксид — утворює щільну оксидну плівку:
4Al + 3O2 = 2Al2O3 .
2) Взаємодія з галогенами.
Порошкоподібний алюміній активно взаємодіє з йодом за звичайних умов у присутності каталітичної кількості води:
2Al + 3I2 = 2AlI3.
3) Взаємодія з сіркою:
2Al + 3S = Al2S3 .
4) Взаємодія з водою.
Незважаючи на високу хімічну активність, з водою алюміній не взаємодіє. У першу чергу, завдяки захисній плівці, а також тому, що продукт взаємодії алюмінію з водою — нерозчинна речовина.
5) Взаємодія з кислотами.
Аналогічно до всіх активних металів алюміній витісняє водень із розчинів кислот:
2Al + 6HCl = 2AlCl3 + 3H2 ;
2Al + 3H2SO4 = Al2 (SO4 )3 + 3H2 .
6) Взаємодія з лугами.
Завдяки тому, що алюміній утворює амфотерні сполуки, він також здатний витісняти водень із розчинів лугів:
2Al + 2NaOH + 6H2O → 2NaAl(OH)4 + 3H2 .
99
www.e-ranok.com.ua