Материал: Альонкіна К. В., Сотниченко Т. Д Хімія. Підготовка до ЗНО

тема 14. алюміній
Добування алюмінію
Алюміній є одним із багатотоннажних продуктів металургійної промисловості. Його добувають у величезних кількостях, тому що він є цінним матеріалом і реагентом. У сучасній металургії алюміній добувають електролізом бокситів (алюміній оксиду). Оскільки сам алюміній оксид є дуже тугоплавкою речовиною, для зменшення енерговитрат у боксит додають плавиковий шпат (кальцій фторид), що знижує температуру плавлення руди.
Застосування алюмінію
Алюміній є цінним конструкційним матеріалом. Маючи відносну легкість (густина алюмінію набагато легша, ніж у сталі), він є досить міцним металом. Його використовують для виготовлення легких конструкцій, у сплаві з магнієм для обшивки літаків тощо. З алюмінію виготовляють столові прибори й посуд. У великих кількостях алюміній використовують у металургії для добування металів алюмотермічним способом.
Al2O3 – природний мінерал корунд, амфотерний оксид, має велику твердість: Al2O3 + 6HCl = 2AlCl3 + 3H2O; Al2O3 + 2NaOH + 3H2O = 2Na[Al(OH)4]
Al(OH)3 – білого кольору нерозчинний у воді; амфотерна основа:
Al(OH)3 + 3HCl = 3H2O +AlCl3; Al(OH)3 + NaOH = Na[Al(OH)4]
виконайте контрольний тест
На його виконання відводиться 15 хвилин. Під час роботи над тестом не можна користуватися слов никами, підручниками, посібниками, довідниками тощо.
тест 28 (контрольний)
1. |
Визначте речовини, реакція між якими в розчині відповідає скороченому йонному рівнянню: |
||||
|
|
Al3+ + 3OH- =Al(OH) |
. |
|
|
|
A AlCl3 + NaOH→ |
В Al(OH) |
3 |
|
+ NaOH→ |
|
|
3 |
|||
|
БAl3PO4 + NaCl→ |
|
ГAl(OH)3 |
+ NaCl→ |
|
2. |
Укажіть оксид, який реагує як із кислотами, так і з основами: |
|
|||
|
А Na2O |
Б SO3 |
В MgO |
ГAl2O3 |
|
3. |
У реакціях із якою речовиною алюміній гідроксид виявляє властивості основи: |
||||
|
А натрій гідроксид |
|
В калій гідроксид |
||
|
Б хлоридна кислота |
|
Г натрій оксид |
||
4. Установіть відповідність між реагентами реакцій та молекулярно йонними рівняннями цих реак-
цій у скороченому вигляді. |
|
1 Al |
|
|
|
|
|
|
|
|
|
|
|
|
|||||
АAl |
O |
3 |
+ HCl→ |
O |
3 |
+ 6H+ → 2Al3+ |
+ 3H |
2 |
O |
||||||||||
2 |
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|||
БAl + HCl→ |
2 2Al0 |
+ 3Cu2+ → 3Cu0 |
+ 2Al3+ |
||||||||||||||||
ВAl + CuCl |
→ |
3 Al(OH) |
3 |
+ 3H+ →Al2+ + 3H |
2 |
O |
|||||||||||||
ГAl(OH) |
|
2 |
|
|
|
|
|
|
|
|
↑ |
|
|
|
|||||
3 |
+ HCl |
4 2Al0 + 6H+ →Al3+ + 3H |
2 |
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
5. Установіть послідовність утворення речовин у ланцюжку перетворень відAl2O3 |
до NaAlO2 |
||||||||||||||||||
АAlCl3 |
|
|
|
БAl2O3 |
В NaAlO2 |
|
ГAl(OH)3 |
||||||||||||
6. Яка масова частка алюмінію (%) у суміші, якщо в результаті обробки 40 г цієї суміші надлишком хлоридної кислоті утворилося 5,6 л водню (н. у.)?
100
www.e-ranok.com.ua

тема 15. феРум
Тема 15. Ферум
Перевірте свої знання
Виконайте тест 29. На його виконання відводиться 15 хвилин. Під час роботи над тестом не можна користуватися словниками, підручниками, посібниками, довідниками тощо.
|
|
тест 29 (вступний) |
||
1. |
Позначте оксид, який відповідає ферум(ІІІ) гідроксиду. |
|||
|
А FeO |
|
|
В OF2 |
|
Б Fe2O3 |
|
|
Г Fe3O4 |
2. |
Укажіть йон, наявність сполук якого обумовлює колір крові. |
|||
|
А Cu2+ |
|
|
В Fe3+ |
|
Б Fe2+ |
|
|
Г Na+ |
3. |
Укажіть хімічну формулу піриту (залізного коледчану). |
|||
|
А FeCl2 |
|
|
В FeS2 |
|
Б FeS |
|
|
Г FeSO4 |
4. |
Установіть відповідність між реагентами реакцій та їхніми такими процесами. |
|||
|
А Fe(OH)3 |
+ H2SO4 → |
1 |
відновлення ферум(ІІІ) оксиду СО |
|
Б Fe(OH)3 |
→ |
2 |
перетворення ферум(ІІ) гідроксиду |
|
В Fe(OH)2 |
+ O2 + H2O → |
3 |
розкладання ферум(ІІІ) гідроксиду |
|
Г Fe2O3 + CO → |
4 |
нейтралізацією Fe(OH)3 сульфатною кислотою |
|
5. Установість послідовність реагентів та умов, за яких відбувається перебіг хімічних реакцій в генетичному ланцюжку перетворень:
Fe2O3→Fe→FeCl3→Fe(OH)3→Fe2O3.
А нагрівання Б натрій гідроксид В хлор
ГAl
6.У результаті взаємодії 0,5 г двовалентного металу із сульфатною кислотою утворилося 200 мл водню (н. у.). Указати порядковий номер цього металу в ПСХЕ.
101
www.e-ranok.com.ua
тема 15. феРум
теоретична частина
феРум
Властивості хімічного елемента
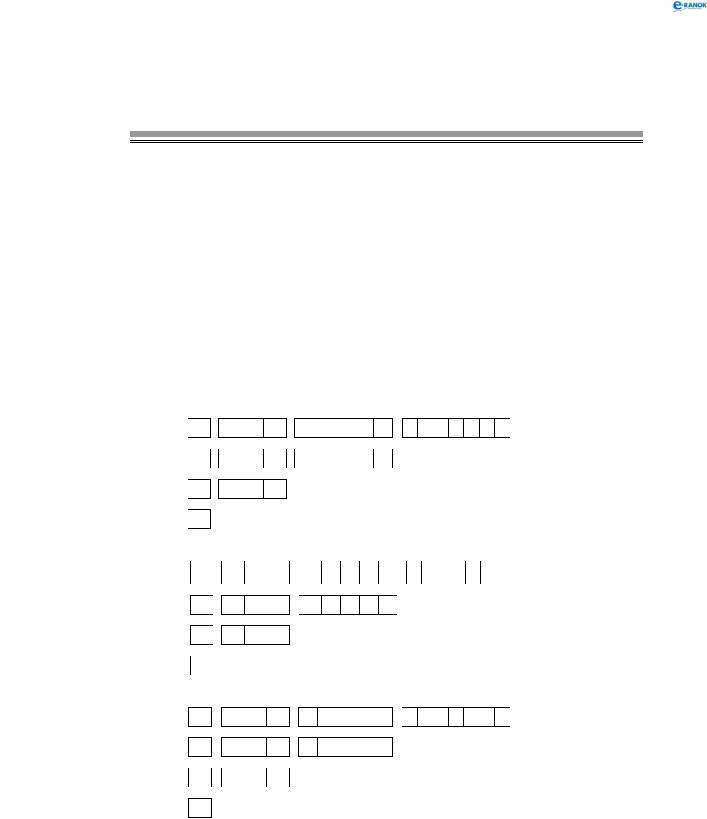
Ферум належить до металічних елементів. За будовою електронної оболонки його відносять до d-елементів, тому що в нього відбувається заповнення електронами d-підрівня.
Здебільшого Ферум виявляє ступінь окиснення +2 (за рахунок двох електронів зовнішнього рівня) або +3 (віддаючи ще один електрон з передзовнішнього рівня). Ступінь окиснення +3 для Феруму більш стабільний, оскільки передзовнішній d-підрівень у цьому разі стає наполовину заповненим, що є більш вигідним. Ферум є досить активним елементом. У хімічних реакціях він проявляє здебільшого металічні властивості.
26 |
Fe0 |
4 |
↑↓ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3↑↓ |
↑↓ |
↑↓ |
↑↓ |
↑↓ |
↑ |
↑ |
↑ |
↑ |
f |
|
|
|
2↑↓ |
↑↓ |
↑↓ |
↑↓ |
|
|
d |
|
|
|
|
|
|
1↑↓ |
|
p |
|
|
|
|
|
|
|
|
|
|
s |
|
|
|
|
|
|
|
|
|
26 |
Fe+2 |
|
4 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3↑↓ |
↑↓ |
↑↓ |
↑↓ |
↑↓ |
↑ |
↑ |
↑ |
↑ |
f |
|
|
|
2↑↓ |
↑↓ |
↑↓ |
↑↓ |
|
|
d |
|
|
|
|
|
|
1↑↓ |
|
p |
|
|
|
|
|
|
|
|
|
|
s |
|
|
|
|
|
|
|
|
|
26 |
Fe+3 |
|
4 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3↑↓ |
↑↓ |
↑↓ |
↑↓ |
↑ |
↑ |
↑ |
↑ |
↑ |
f |
|
|
|
2↑↓ |
↑↓ |
↑↓ |
↑↓ |
|
|
d |
|
|
|
|
|
|
1↑↓ |
|
p |
|
|
|
|
|
|
|
|
|
|
s |
|
|
|
|
|
|
|
|
|
фізичні властивості заліза
Залізо є речовиною з немолекулярною будовою. У звичайних умовах залізо являє собою метал сірого кольору з металічним блиском, добре проводить електричний струм і теплоту. Залізо є досить пластичним металом і добре піддається куванню. Температура плавлення заліза +1540 °С, густина 7,87 г/см3. Як і багато інших металів, залізо не розчиняється у воді та в інших розчинниках, але розчиняється в ртуті.
102
www.e-ranok.com.ua

тема 15. феРум
Залізо притягується магнітом, тобто є парамагнетиком. Для заліза також характерне явище феро магнетизму — воно зберігає намагніченість після усунення зовнішнього магнітного поля. Завдяки цьому із заліза можна виготовляти магніти, а також матеріали для запису інформації.
хімічні властивості заліза
Залізо досить активно вступає в хімічні взаємодії. Оскільки залізо має явні металічні властивості, то воно вступає переважно в реакції з неметалами.
Залізо активно вступає у взаємодію з киснем навіть у звичайних умовах. При нагріванні заліза на повітрі його поверхня покривається залізною окалиною:
3Fe +2O2 → Fe3O4 .
Залізний дріт також дуже активно згорає, якщо його помістити в посудину, наповнену хлором. При цьому утворюється ферум(III) хлорид:
2Fe +3Cl2 →2FeCl3 .
Залізо також активно взаємодіє із сіркою. У результаті цієї реакції утворюється ферум(II) сульфід:
Fe + S → FeS.
Залізо здатне реагувати з водою. При пропусканні перегрітої пари через розжарені залізні ошурки залізо перетворюється в залізну окалину й при цьому виділяється водень:
3Fe +4H2O t→Fe3O4 +4H2 .
У звичайних умовах залізо активно реагує з кислотами. При цьому утворюються солі, до яких Ферум входить зі ступенем окиснення +2:
Fe + H2SO4 → FeSO4 + H2 .
Ферум також здатен витісняти менш активні метали з розчинів солей:
Fe + CuSO4 → FeSO4 + Cu.
Зі ступенем окиснення +3 він може проявляти амфотерні властивості. Це можна довести тим, що ферум(III) гідроксид розчиняється в гарячому концентрованому лузі:
Fe(OH)3 +NaOH = Na Fe(OH)4 .
Амфотерні властивості Феруму проявляються значно слабше, ніж в Алюмінію, тому що алюміній гідроксид розчиняється в лугах у звичайних умовах, а ферум(III) гідроксид — при нагріванні й за умови високої концентрації лугу.
Застосування заліза
Залізо є одним із семи найстаріших металів — металів, відомих людству з давніх часів. Унаслідок високої хімічної активності самородне залізо (тобто у вигляді простої речовини) на Землі не зустрічається. Люди навчилися добувати залізо на початку першого тисячоліття до нашої ери. Звідтоді почався залізний вік розвитку нашої цивілізації. Хоча в археологічних розкопках іноді зустрічаються залізні вироби, датовані другим і третім тисячоліттям до нашої ери, це так зване космічне залізо — уламки залізних метеоритів, які впали на Землю.
Залізо є набагато твердішим металом, аніж мідь, тому знаряддя праці та зброю для полювання було зручніше виготовляти саме з нього. Однак для добування заліза необхідна більш висока тем-
103
www.e-ranok.com.ua

тема 15. феРум
пература вогню, ніж для добування міді. І хоча міді в земній корі міститься приблизно в 1000 разів менше, ніж заліза, її було простіше виплавляти й обробляти. Отож першим металом, який почали обробляти люди, була мідь, а не залізо.
Залізо здебільшого використовують у вигляді сплавів: чавуну й сталі. Чавун за фізичними властивостями посутньо відрізняється від заліза: він набагато твердіший і крихкіший. Саме тому чавун не піддається куванню, однак із нього виходять предмети, які можуть витримувати вели - кі механічні навантаження. Раніше з нього виплавляли гармати та ядра й навіть посуд. Зараз із чавуну роблять станини для верстатів, лещата та інші вироби, для яких більше важить механіч - на міцність, а не пластичність. Такі вироби дуже бояться ударів, від сильного удару чавун роз - бивається.
Широко розповсюджена іржостійка сталь, її добувають додаванням у сталь нікелю й хрому, а для добування зносостійкої сталі додають марганець (таку сталь використовують для виготовлення залізничних рейок).
FeO – компонент кераміки, пігмент для фарб і термостійкої емалі, Fe2O3 – для виготовлення кераміки, цементу, як пігмент.
Залізний купорос FeSO4 ∙ 7H2O застосовують у виробництві мінеральних фарб, при фарбуванні тканин, для боротьбі з шкідниками сільського господарства.
Хлористе залізо – для отримання чистого заліза.
Fe2O3 – сполука бурого кольору, відноситься до амфотерних оксидів: Fe2O3 + 6HCl = 2FeCl3 + 3H2O;
Fe2O3 + 2KOH =t 2KFeO2 + H2O
Fe(OH)2 – білого кольору, поступово зеленіє:
Fe(OH)2 + 2HCl = FeCl2 + H2O
Fe(OH)3 – бурого кольору, відноситься до амфотерних основ: Fe(OH)3 + 3HCl = FeCl3 + 3H2O Fe(OH)3 + 3KOH = K3[Fe(OH)6]
У водних розчинах сполуки Fe2+ легко окиснюється до Fe3+: 4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3.
104
www.e-ranok.com.ua