Материал: Альонкіна К. В., Сотниченко Т. Д Хімія. Підготовка до ЗНО

тема 12. Загальні відомості ПРо металічні елементи та метали
Тема 12. Загальні відомості про металічні елементи та метали
Перевірте свої знання
Виконайте тест 23. На його виконання відводиться 15 хвилин. Під час роботи над тестом не можна користуватися словниками, підручниками, посібниками, довідниками тощо.
тест 23 (вступний)
1.Під час хімічної реакції метали:
Авіддають електрони зовнішнього енергетичного рівня Б приєднують електрони В не змінюють зовнішній енергетичній рівень
Г спочатку приєднують, а потім віддають електрони
2.Визначте правильне твердження: у ряду хімічних елементів Mg → Ca → Ba→ Ra.
Азменшується число протонів у ядрах атомів
Б збільшується число енергетичних рівнів в атомах В збільшується число валентних електронів в атомах
Гзменшуються радіуси атомів
3.Який метал є найрозповсюдженішим у земній корі?
АFe
Б Ti ВAl
ГCa
4.Установіть відповідність між реагентами та схемами перетворень.
А CuCl |
+ Mg→ |
1 |
Zn0 → Zn2+ |
|
2 |
|
+ Cu → |
2 |
Zn2+ → Zn0 |
БAgNO |
3 |
|||
В ZnCl |
+Al → |
3 |
Cu0 → Cu2+ |
|
2 |
|
|
|
2+ → Cu0 |
Г Zn + CuCl → 4 Cu |
|
|||
|
|
2 |
|
|
5. Установіть послідовність відновлення залізної окалини в доменній печі.
А Fe2O3
БВ FeFe3O4
ГFeO
6.У результаті взаємодії цинкового пилу масою 0,22 г із хлоридною кислотою виділився водень об’ємом 63,8 мл. Обчислити масову частку (%) цинку в цинковому пилу.
85
www.e-ranok.com.ua

тема 12. Загальні відомості ПРо металічні елементи та метали
теоретична частина
Загальна характеристика металів
Металічні елементи займають в основному ліву нижню частину Періодичної системи хімічних елементів Д. І. Менделєєва. До металічних елементів належать ті елементи, в чиїх атомах на зовнішньому електронному рівні перебуває невелике (від одного до чотирьох) число електронів, які атоми можуть легко віддавати.
Метали мають низку спільних фізичних властивостей:
—добру електропровідність;
—добру теплопровідність;
—металічний блиск;
—добру пластичність (ковкість);
—зазвичай високу твердість;
—як правило, перебувають у твердому агрегатному стані.
Такі спільні фізичні властивості металів обумовлені наявністю в металів особливого типу хімічного зв’язку — металічного. Наявність таких властивостей, як електропровідність і теплопровідність, указує на значну рухливість електронів у металах.
Атоми металів на зовнішньому електронному рівні мають невелику кількість електронів, які досить слабко взаємодіють з ядром, отже, можуть легко віддаватися. Таким чином, кожний атом металу віддає в спільне користування щонайменше по одному електрону зі свого зовнішнього електронного рівня. Усі електрони можуть вільно переміщатися по всьому металічному кристалу й утворюють так званий «електронний газ». Присутністю вільних електронів та їхнім рухом по всьому зразку металу пояснюється значна електропровідність, теплопровідність металів та їхній характерний металічний блиск.
Чим більша активність металу, тим енергійніше він реагує з іншими речовинами. За активністю всі мета-
лиможнарозташувативряд,якийназиваютьрядомактивностіметалів,абовитискувальнимрядомметалів,
аборядомнапругметалів,атакожелектрохімічнимрядомнапругметалів.Цейрядупершедослідиввидатний український учений М.М. Бекетов, тому цей ряд називають також рядом Бекетова.
Ряд активності металів Бекетова має такий вигляд (наведені найбільш уживані метали):
K > Ca > Na > Mg >Al > Zn > Fe > Ni > Sn > Pb > H2 > Cu > Hg >Ag >Au.
У цьому ряді метали розташовані за зменшенням їхньої активності. Серед наведених металів найбільш активний калій, а найменш активний — золото. За допомогою цього ряду можна визначити, який метал активніший від іншого. Також у цьому ряді присутній водень. Звісно ж, водень не є металом, але в цьому ряді його активність прийнята за точку відліку (своєрідний нуль).
Загальні хімічні властивості металів
В атомах металів на зовнішній електронній оболонці утримується невелике число електронів. Ці електрони порівняно легко можуть відриватися від атомів. Така особливість металів є причиною не тільки їхніх фізичних, але й хімічних властивостей. Виходячи з того, що метали здатні тільки віддавати електрони зовнішнього електронного рівня, можна зробити висновок, що в хімічних реакціях метали здатні проявляти тільки властивості відновника.
86
www.e-ranok.com.ua
тема 12. Загальні відомості ПРо металічні елементи та метали
Основний процес, який характеризує хімічні властивості металів, можна записати у вигляді такої схеми:
Me0 − ne → Me+n .
Взаємодія металів з неметалами
Більшість металів активно реагують із неметалами, при цьому метали виконують роль відновника, а неметали — окисника. У результаті реакцій утворюються бінарні сполуки: солі безоксигенових кислот:
2ex2 |
2e |
3ex2 |
+2 −2 |
+2 −2 |
+3 −2 |
2Mg+O2 = 2MgO |
Fe+S= Fe S |
2Al+3I2 = 2Al I3 |
Або в загальному вигляді:
ne |
|
|
Me0 |
+ неMe0 |
= Me+nнеMe−n |
відновник |
окиснювач |
сіль безкисневої |
кислоти
Взаємодія металів з водою
метали |
хімічні процеси при реакції з водою |
Продукти реакції |
||||||
Лужні метали, а також Cа та Ва |
Me0 |
+ HOH → Me+n (OH)n + H2 ↑ |
Н2 і Me(OH)n |
|||||
Mg, Al, Mn, Zn, Cr, Fe, Ni, Pb |
Me |
0 |
+ HOH → Me |
+n |
O |
−2 |
+ H2 ↑ |
Н2 і МеО |
|
|
|
|
|
||||
Cu, Ag, Au |
З водою не взаємодіють |
|
|
|||||
Взаємодія металів з кислотами
Активні метали, які розташовані в ряді напруг до водню, витискують Гідроген із розчинів кислот. Метали, які розташовані в ряді напруг після водню, з розчинами кислот (окрім нітратної та сульфатної) не взаємодіють:
Zn + 2HCl = ZnCl2 + H2 ↑,
Zn0 + 2H+ = Zn2+ + H2 ↑ ,
відновник окиснювач
Cu + HCl ≠ не взаємодіють.
Якщо метал здатний проявляти кілька ступенів окиснення, то при взаємодії з безоксигеновою кислотою утворюється сіль, у якій метал, як правило, має нижчий ступінь окиснення, наприклад:
Fe + 2HCl = FeCl2 + H2 ↑,
Fe0 + 2H+ = Fe2+ + H2 ↑.
Взаємодія металів із солями
Більш активні метали здатні витісняти менш активні з їхніх солей:
Fe0 + Cu2+ → Fe2+ + Cu0 ; |
Cu0 + Fe2+ ≠ |
Zn0 + Fe2+ → Zn2+ + Fe0 ; |
Fe0 + Zn2+ ≠ |
87
www.e-ranok.com.ua

тема 12. Загальні відомості ПРо металічні елементи та метали
Загальні способи добування металів
лабораторні методи добування
а) відновлення оксидів металів воднем; таким способом зазвичай добувають не дуже активні метали, які не взаємодіють із воднем:
CuO + H2 → Cu + H2O;
WO3 +3H2 → W +3H2O;
б) розкладання оксидів важких металів:
2HgO →t 2Hg + O2;
в) витіснення металів з їхніх солей більш активними металами:
Fe + CuSO4 → FeSO4 + Cu;
Zn + HgCl2 → ZnCl2 + Hg.
Добування металів у промисловості
а) відновлення оксидів металів вуглецем або кремнієм:
2CuO + C → Cu + CO2;
2FeO + Si → Fe + SiO2 ;
б) відновлення оксидів металів карбон монооксидом:
Fe2O3 + CO →2Fe +3CO2;
в) відновлення металів з оксидів більш активними металами в розплавах:
3V2O5 +10Al →6V +5Al2O3 ;
MnO2 + Mg → Mn +2MgO.
Відновлення металів з оксидів більш активними металами називають металотермічним методом. Найпоширенішим металом, що його використовують як відновник, є алюміній (алюмінотермія).
Корозія металів
Корозією зазвичай називають мимовільне руйнування металів у результаті їхньої хімічної й електрохімічної взаємодії із зовнішнім середовищем та перетворення їх у стійкі сполуки (оксиди, гідроксиди, солі).
Власнекажучи,корозіяявляєсобоюсукупністьокисно-відновнихпроцесів,яківідбуваютьсяприкон- такті металів з агресивним середовищем, що призводить до руйнування металевих виробів. Під агресивним середовищем мають на увазі окисну атмосферу (присутність кисню в атмосфері Землі робить її окисною), особливо в присутності води або розчинів електролітів.
За механізмом процесу розрізняють хімічну та електрохімічну корозію металів. Хімічна корозія являє собою звичайну хімічну реакцію між атомами металів і різних окисників. Прикладами хімічної корозії є високотемпературне окиснення металів киснем, окиснення поверхні алюмінію на повітрі, взаємодія металів із хлором, сіркою, сірководнем H2S тощо.
Електрохімічна корозія протікає в розчинах, тобто, в основному, при контакті металів з розчинами електролітів, особливо у тих випадках, коли метали перебувають у контакті з менш активними метала-
88
www.e-ranok.com.ua
тема 12. Загальні відомості ПРо металічні елементи та метали
ми. Швидкість корозії істотно залежить від активності металів, а також від концентрації й природи домішок у воді. У чистій воді метали майже не піддаються корозії, а в контакті з більш активними металами навіть у розчинах електролітів не кородують.
Сумарне рівняння реакції корозії заліза можна записати так:
4Fe + 3O2 + 6H2O → 4Fe(OH)3 .
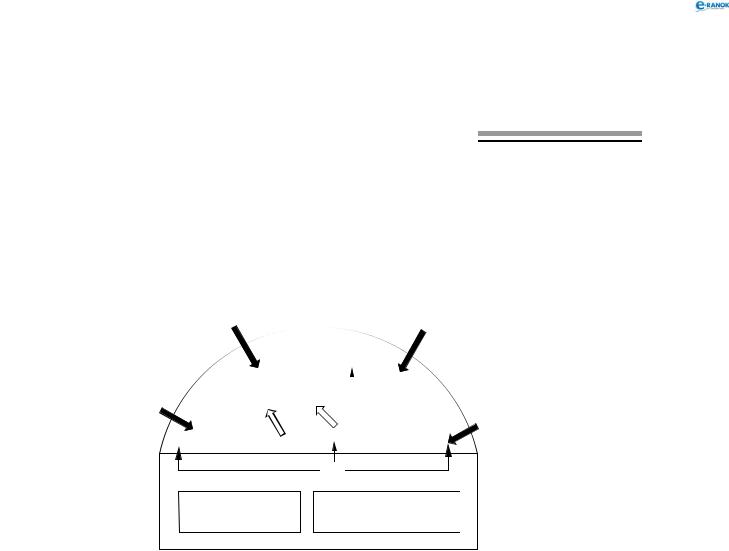
Схематично процеси, які відбуваються на поверхні заліза або сталі при контакті з водою, можна подати так:
O2 |
повітря |
|
O2 |
|
|
|
крапля води |
|
|
||
|
Fe2O3·H2O |
іржа |
|
||
|
|
|
O2 |
|
|
O2 |
2OH–+ Fe2+= Fe(OH) |
2 |
O2 |
||
|
|
|
|
||
– |
– |
Fe2+ |
|
|
|
2e + 1/2O2 + H2O = 2OH |
|
|
|
|
|
|
e– |
Fe |
|
e– |
|
потік електронів |
потік електронів |
|
|||
Відновлення: |
|
|
|
||
|
Окиснення: |
|
|||
кисень відновлюється |
залізо окиснюється, |
|
|||
до гідроксид йонів |
і йони переходять у розчин |
|
|||
залізо або сталь
методи захисту від корозії
На сьогодні існує кілька способів запобігання корозії.
Відокремлення металу від агресивного середовища — фарбування, змащування маслами, покриття неактивними металами або емаллю (І). Приведення поверхні металів у контакт із більш активними металами (ІІ). Використання речовин, що сповільнюють корозію (інгібітори корозії), та сплавів, стійких до корозії (ІІІ).
I. Найпростіший спосіб захистити сталь від корозії — це ізолювати метал від атмосферного повітря. Це можна зробити за допомогою масляного, жирового змащування або нанесення захисного шару фарби.
Зараз широко застосовують захисні покриття з органічних полімерів. Покриття можна робити різних кольорів, і це досить гнучке розв’язання проблеми корозії. Навіть побіжний погляд на речі, які оточують нас у побуті, дає масу прикладів такого розв’язання: холодильник, сушарка для посуду, піднос, велосипед тощо.
II. Іноді залізо покривають тонким шаром іншого металу. Деякі виробники виготовляють кузови автомобілів зі сталі з гальванічним цинковим покриттям. При такій обробці утворюється міцно зчеплений з основою шар цинк оксиду, і якщо гальванічне покриття не ушкоджене, воно добре захищає від іржі.
Дуже розповсюдженим розв’язанням проблеми захисту від корозії є використання іржостійких сплавів. Багато зі сталевих виробів, використовуваних у побуті, особливо ті, що перебувають у постійному контакті з водою: кухонний посуд, ложки, виделки, ножі, бак пральної машини тощо — виготовлені з іржостійкої сталі, яка не вимагає додаткового захисту.
89
www.e-ranok.com.ua