Материал: А27631 Бегунов АА методы и средства аналитических измерений
4 5 2





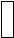




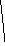

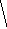










Рис. 6.15. Масс-спектрометр:
1 – ионизационная камера; 2 – камера; 3 – коллектор;
4 – усилитель; 5 – измерительный прибор
Системой введения анализируемое вещество подают в иониза-тор, где молекулы превращаются в ионы. В случае твердых и жидких проб ионизатор включает испаритель, переводящий пробу в газообразное состояние. Для ионизации используют облучение пробы фотонами, ионами, воздействием электрического поля и др. Образующиеся положительно заряженные ионы проходят через пластины, между которыми наводится электрическое поле с разностью потенциалов в несколько тысяч вольт. Остатки неионизированного вещества удаляются вакуумным насосом. Быстро движущиеся ионы попадают в магнитное поле напряженностью Н. При этом в зависимости от массы иона, его заряда и соотношения ускоряющего напряжения и напряженности магнитного поля эти ионы начинают двигаться по траекториям с различными радиусами.
Масс-спектры получают, одновременно регистрируя все ион-ные пучки на одной фотопластинке (масс-спектрография) или непрерывно изменяя радиусы (варьируя H или U) так, что различные пучки ионов достигают улавливающего электрода последовательно (масс-спектрометрия). Спектры регистрируют на ленточном самописце или с помощью осциллографа.
Одна из основных характеристик масс-спектрометра – его разрешающая способность. Она отражает способность прибора разделять линии, относящиеся к ионам с близкой массой. Считается, что два пика равной высоты разрешены, если в промежутке между ними интенсивность не превышает 10 % высоты пика. Отсюда разрешающая способность системы определяется как относительная разность массы для двух ионов, линии которых можно разрешить. Более же принято разрешающую способность выражать обратной величиной.
Значение необходимого разрешения зависит от задачи, которую необходимо решить: при увеличении разрешающей способности масс-спектр становится более сложным и его интерпретация затрудняется. Разрешающая способность простейших приборов лежит в пределах 200–2000. Масс-спектрометры высокого разрешения обладают разрешающей способностью 20 000–200 000.
Для точных измерений массы элементов одновременно регистрируют спектры образца и калибровочного соединения. Это соединение, обычно фторсодержащее, должно давать в масс-спектре линии ионизированных фрагментов известного состава, которые можно лег-ко идентифицировать.
В последнее время разработаны устройства, передающие ин-формацию с детектора на компьютер, что ускоряет обработку данных и дает возможность непосредственно получать концентрационные характеристики. Масс-спектры многих веществ подробно изучены и представлены в специальных атласах в виде спектрограмм или таблиц.
6.6.5. Методы электронного парамагнитного резонанса
Методы электронного парамагнитного резонанса (ЭПР) относятся к радиоспектроскопическим (спинорезонансным) методам анализа, с помощью которых изучают взаимодействие вещества с излучением в радиочастотном диапазоне.
Методы ЭПР и ЯМР имеют много сходных черт. Оба основа-ны на явлении магнитного резонанса – избирательном поглощении электромагнитного излучения в радиочастотном диапазоне и обусловлены магнитными свойствами частиц (электронов – в методе ЭПР и ядер – в методе ЯМР).
Магнитный резонанс
можно истолковать с квантово-механиче-ских
и классических позиций. Согласно
классическим представле-ниям, заряженная
частица, имеющая собственный механический
мо-мент (спин), при движении создает
магнитное поле, т. е. характеризуется
собственным магнитным моментом
![]() .
.
При помещении
заряженной частицы в постоянное магнитное
поле Н0
ее магнитный момент взаимодействует
с полем с энергией Е
= –![]() .
В результате такого взаимодействия
частица получает вращательный момент,
вызывая прецессию вектора вокруг Н0
под неизменным углом φ с частотой 0.
Такая прецессия создает переменный
магнитный момент, вращающийся с частотой
ν0
перпендикулярно
направлению поля Н0.
Если в той же плоскости в том же направлении
вращается переменное магнитное поле
Н1
с частотой 1,
то это поле взаимодействует с немагнитным
моментом. Взаимодействие тем больше,
чем частота 1
ближе к 0.
При 1 = 0
наступает резонанс, сопровождающийся
перекачкой (поглощением) энергии
переменного магнитного поля Н1
в исходную систему.
.
В результате такого взаимодействия
частица получает вращательный момент,
вызывая прецессию вектора вокруг Н0
под неизменным углом φ с частотой 0.
Такая прецессия создает переменный
магнитный момент, вращающийся с частотой
ν0
перпендикулярно
направлению поля Н0.
Если в той же плоскости в том же направлении
вращается переменное магнитное поле
Н1
с частотой 1,
то это поле взаимодействует с немагнитным
моментом. Взаимодействие тем больше,
чем частота 1
ближе к 0.
При 1 = 0
наступает резонанс, сопровождающийся
перекачкой (поглощением) энергии
переменного магнитного поля Н1
в исходную систему.
С позиций квантово-механической модели состояния спина (электронного и ядерного) и магнитного момента квантованы. При отсутствии магнитного поля состояния частицы, характеризующиеся спиновыми квантовыми числами ±1/2, вырождены, т. е. имеют одну и ту же энергию. При помещении частицы в постоянное магнит-ное поле Н0 вырождение снимается и энергии уровней с тs = +1/2 и ms = –1/2 оказываются неравными. Магнитный резонанс возникает вследствие переходов частицы из нижнего энергетического состоя-ния в более высокое, индуцируемое переменным полем Н1 с час-тотой 1.
Условие перехода ΔE = hl = gβH0 является условием резонанса. Поглощение энергии магнитного поля Н1 системой определяется избытком магнитных частиц в нижнем энергетическом состоянии. Этот избыток невелик из-за малых значений величины ΔE и близости заселенности верхнего и нижнего состояний. При поглощении энергии нарушается термодинамическое равновесие в системе спинов и разность заселенности уменьшается. Однако существуют релаксационные процессы, возвращающие систему в равновесное состояние вследствие наличия безызлучательных процессов.
Различают два типа релаксационных процессов: спин-решеточ-ную (продольную) релаксацию, характеризующуюся временем Т1, и спин-спиновую (поперечную) релаксацию, характеризующуюся вре-менем Т2. Спин-решеточная релаксация связана с передачей энергии ядер окружающей среде (решетке) и превращением ее в тепловую. Чем больше время релаксации, тем меньше разность заселенности уровней, а следовательно, и меньше сигнал. В предельном случае он может совсем исчезнуть, когда достигнуто равенство заселенности уровней (явление насыщения). Малое время релаксации исключает возможность насыщения, однако при малых Т1, что соответствует малому времени жизни системы в возбужденном состоянии, линия поглощения сильно уширяется. Уменьшение времени жизни системы в возбужденном состоянии Δτ влечет увеличение ΔE, что приводит к уширению линии. Например, ширина линии ЭПР для свободных органических радикалов составляет ~1 Э. Для парамагнитных ионов переходных металлов вследствие большого вклада орбитального момента характерно малое время релаксации, и линии уширяются до 10 Э. По тем же причинам спектры ЭПР-ионов элементов, для которых спин-орбитальное взаимодействие велико, вообще не наблюдаются, даже при температуре жидкого азота 77 К.
Спин-спиновая релаксация заключается в обмене энергии между спинами частиц. При этом ядра одного атома с высокой энергией передают часть своей энергии другому атому, находящемуся в более низком энергетическом состоянии.
Для экспериментального наблюдения резонансного поглощения существует две возможности. В обоих случаях соблюдается условие резонанса h1 = gβH0. Можно варьировать частоту l при постоянном магнитном поле H0, а можно изменять напряженность магнитного поля H0, оставляя неизменной частоту 1. В спектрометрах ЭПР и в большинстве ЯМР-спектрометрах реализуется вторая возможность.
Принцип работы установки ЭПР: электромагнитные колебания от генератора (клистрона) поступают в резонатор (поглощающую ячейку). Резонатор и помещенное в него исследуемое вещество находятся в постоянном магнитном поле, создаваемом магнитом. Напряженность магнитного поля сканируется. При достижении резонанса исследуемое вещество поглощает энергию, количество которой детектируется, усиливается и поступает на регистрирующее устройство. Регистрация спектра осуществляется либо в виде линии поглощения, либо в виде ее производной. Чаще всего если в ЯМР-спектро-метрии высокого разрешения регистрируют сигнал поглощения, то в ЭПР – ее первую или вторую производную. При обычно применяемых магнитных полях (103–104) Э частота ЯМР попадает в диапазон коротких радиоволн (106–108) Гц, а ЭПР – в микроволновый диапазон (108–1010) Гц.
Большинство стандартных ЭПР-спектрометров работают на частоте 9400 МГц (λ = 3,2 см), что соответствует напряженности магнитного поля H0 = 3300 Э для g = 2. В ряде случаев используют более длинные (до 100 см) и более короткие (8 и 4 мм) волны. Чувствительность оценивается числом детектируемых частиц на 1 Э. Если ширина линии составляет 1 Э, то предел обнаружения методом ЭПР составляет n · 1010 частиц.
Сигнал ЭПР наблюдается для веществ, в атомах или молекулах которых имеются неспаренные электроны. К ним относятся:
– органические и неорганические свободные радикалы;
– ионы с частично заполненными внутренними уровнями (3d- и 4d-переходные элементы и некоторые 4f-элементы);
– атомы и молекулы с нечетным числом электронов, например атомы водорода, азота, молекулы NO, ClО2 и др.;
– кристаллы, имеющие центры окраски;
– металлы и полупроводники, имеющие электроны проводимости.
При химическом анализе чаще имеют дело с первыми двумя группами веществ.
Исследования ЭПР проводят с жидкими и твердыми образцами, реже – с газообразными. При работе с жидкими образцами целесообразнее использовать неполярные органические растворители, так как увеличение диэлектрической проницаемости приводит к ухудшению аналитического сигнала. Для твердых образцов наиболее перспективно использование монокристаллов, однако из-за трудности их получения чаще работают с замороженными растворами (стеклами) или с поликристаллическими порошками. Для снижения спин-спинового взаимодействия часто используют совместную кристаллизацию парамагнитного вещества с диамагнитными, образующими с ним изоморфные кристаллы.
Симметричная линия поглощения ЭПР характеризуется ее положением в магнитном поле, интенсивностью, шириной и формой. Положение линии в магнитном поле определяется g-фактором, являющимся мерой эффективного магнитного момента электрона. Величина g-фактора – индивидуальное свойство каждого вещества. Угол расхождения энергетических уровней при увеличении магнитных полей зависит от g-фактора, и для различных веществ он разный. С другой стороны, g-фактор зависит от структуры атома, свойств его ядра и его химического окружения, что позволяет исследовать строение молекул вещества.
Ограничением метода ЭПР является малое число объектов исследования, поскольку большинство ионов металлов и органических веществ диамагнитно. К тому же линии парамагнитных ионов широки вследствие вклада орбитальной составляющей в магнитный момент. Часто их трудно использовать для чувствительных аналитических определений. Избежать эти недостатки позволяет использование комплексообразования диамагнитных ионов с органическими лигандами, являющимися стабильными свободными радикалами (спин-меченые реагенты). В этом случае концентрацию диамагнитного иона определяют по парамагнетизму органической части компонентов соединения. Использование спин-меченых реагентов делает метод ЭПР универсальным, метод становится пригодным для определения ионов в любой степени окисления, как парамагнитных, так и диамагнитных. Кроме того, спектры ЭПР с реагентом-радикалом характеризуются более узкими линиями, что существенно повышает чувствительность определения металлов.
7.3. Преобразователи
В биологических измерительных устройствах, содержащих электрохимический преобразователь, при взаимодействии биоэлемента с определяемыми молекулами генерируется изменение потенциала действия системы (потенциометрические электроды, ионоселективный полевой транзистор) или тока (амперометрическая и кондуктометрическая ячейки).
Рассмотрим более подробно потенциометрические биосенсоры, как имеющие наибольшее практическое значение.
В состав потенциометрического биосенсора входит внутренний ионоселективный электрод; обычно используют ферменты, иммобилизованные на гидрофильной мембране. В качестве специфических химических реакций, лежащих в основе работы потенциометрических биосенсоров, можно применять биохимические реакции, протекающие в клетках или срезах биологических тканей, прикрепленных к ионоселективному электроду (обычно стеклянный), и соединенном с ним активном гидрофильном слое. В этом слое один из компонентов анализируемого вещества превращается в форму, пригодную для потенциометрического измерения с помощью внутреннего ионоселективного электрода.
В настоящее время существует несколько видов электродов с использованием биологических элементов. Рассмотрим наиболее распространенные виды таких электродов.
Бактериальные электроды. В них между измерительным электродом и мембраной, непроницаемой для высокомолекулярных веществ, помещают слой бактерий. Определяемое вещество под действием соответствующего штамма бактерий превращается в продукт, к которому чувствителен данный электрод. С помощью биологических измерительных устройств (БИУ) можно определять аргинин, глутамин, аспаргиновую кислоту, гистидин и нитрат-ион.
Существуют гибридные бактериально-ферментные электроды. В этих биосенсорах специфическая химическая реакция осуществляется с участием штамма бактерий и фермента одновременно.
Электроды на основе биологической ткани. Основным элементом конструкции этих БИУ является тонкий слой биологической ткани, прикрепленной к поверхности внутреннего электрода. В результате ферментативной реакции, происходящей в ткани, выделяются продукты, потенциалообразующие для этого электрода. В биологических измерительных устройствах, содержащих термический преобразователь, используется универсальное свойство выделения тепла 25–100 кДж/моль при протекании ферментативных реакций.
Оптические преобразователи. Данные преобразователи служат для детекции изменения окраски или люминесцентных свойств среды, возникающего при действии биокатализатора. Преобразователи, основанные на ячейках поверхностных электромагнитных волн и поверхностных плазмонов, регистрируют изменения коэффициента преломления на поверхности оптического элемента, обусловленные взаимодействием определяемых молекул с молекулами антитела, рецепторов, ДНК и другими биомолекулами.
При погружении биоанализатора в исследуемый раствор прида-ющее вкус вещество связывается с пленкой, что вызывает изменение флуоресцентных характеристик. Измерение этих изменений позволяет определять концентрацию глутаминовой кислоты и МР в растворе.
За рубежом создан новый высокоэффективный биоанализатор вкуса, который может обнаруживать глутаминовую кислоту и СМР одновременно. Биоанализатор изготавливается нанесением на стеклянную подложку пленок Ленгмюра–Биоджетт стеариновой кислоты, содержащей два флуоресцирующих вещества – пирен и периллен. Пьезоэлектрический преобразователь является частью высокочастотного генератора (9–14 МГц), частота которого меняется при изменении массы пьезокристалла. Это изменение обусловлено взаимодействием находящегося на поверхности пьезокристалла биоэлемента с молекулами определяемого вещества. Преобразователи на поверхностных акустических волнах используются в подобной пьезоэлектрическим преобразователям конфигурации. Они действуют при частоте в несколько сот мегагерц. Теоретически это должно было бы увеличить чувствительность, но практически чувствительность уменьшается из-за необходимости использовать очень тонкие (молекулярные) слои биоэлемента. Параметры БИУ зависят от температуры, кислотности и других физических свойств среды. Чувствительность БИУ изменяется во времени.