Материал: А27137 Проверить Рогов Б.А. Пищевая инженерия производства жировой про
Продолжение табл. 3.1
|
Наименование аминокислоты |
Формула |
Свойства |
||||
|
Температура плавления, ˚C |
Растворимость в воде при 25 ˚C, г/100г |
Удельное вращение, град/дм |
||||
|
Амид аминоянтарной кислоты (аспарагин) |
NH2–CH–COOH || CH2–CNH2 |
236 |
2,5 |
+34,3 (3,4 н. HCl) |
||
|
Амид аминоглутаровой кислоты (глутамин) |
NH2–CH–COOH || CH2–CH2 –CNH2 |
185 |
4,2 |
+6,1 (H2O)
|
||
|
Монокарбоновые диаминокислоты |
||||||
|
α-,ε- Диаминокапроновая (лизин) |
NH2–CH–COOH | CH2 / CH2–CH2 –CH2– NH2 |
– |
– |
+25,9 (5 н. HCl) |
||
|
Осксиаминокислоты |
||||||
|
α-Амино-β-окси-пропионовая (серин) |
NH2–CH–COOH \ CH2OH |
228 |
5,0 |
+15,1 (5 н. HCl) |
||
|
α-Амино-β-окси-масляная (треонин) |
NH2–CH–COOH | CH(OH)–CH3
|
253 |
20,5 |
–30,0 |
||
|
Аминокислоты, содержащие серу |
||||||
|
α-Амино-β-тиопро-пионовая (цистеин) |
NH2–CH–COOH | CH2SH |
178 хлоргид-рат |
– |
+13,0 |
||
|
ди-α-Амино-β-тио-пропионовая (цистин) |
NH2–CH–COOH | CH2–S | CH2–S | NH2–CH–COOH |
260 |
0,01 |
–232 (5 н. HCl) |
||
|
α-Амино-γ-метил-тиомасляная (метионин) |
NH2–CH–COOH | CH2–CH2–S–CH3 |
283 |
3,5 |
+20,0 |
||
Продолжение табл. 3.1
|
Наименование аминокислоты |
Формула |
Свойства |
|||||||
|
Температура плавления, ˚C |
Растворимость в воде при 25 ˚C, г/100г |
Удельное вращение, град/дм |
|||||||
|
Гуанидокислоты |
|||||||||
|
α-Амино-δ-гуани-динвалериановая (аргинин) |
NH2–CH–COOH | CH2 NH / || CH2–CH2–NH–C | NH2 |
238 |
15,0 |
+29,4 |
|||||
|
Ароматические аминокислоты |
|||||||||
|
|
NH2–CH–COOH | CH2– |
–
|
3,0 |
–7,5 |
|||||
|
|
NH2–CH–COOH | CH2– – OH
|
344 |
0,05 |
–10,0 (5 н. HCl) |
|||||
|
Гетероциклические аминокислоты |
|||||||||
|
|
NH2–CH–COOH | H2C–
│ NH |
282 |
1,14 |
–34,0 |
|||||
|
Пирролидин-α-кар- боновая (пролин) |
H2C–CH2 | | H2C CH–COOH \ / NH |
222 |
162 |
–80,0 |
|||||
Окончание табл. 3.1
|
Наименование аминокислоты |
Формула |
Свойства |
|||||||||
|
Температура плавления, ˚C |
Растворимость в воде при 25˚C, г/100г |
Удельное вращение, град/дм |
|||||||||
|
γ-Оксипирролидин-α- карбоновая (окси- пролин) |
НО–CН–CH2 | | H2C CH–COOH \ / NH |
270 |
36,1 |
–77,0 |
|||||||
|
ε-Амино-β-имидазол- пропионовая |
NH2–CH–COOH | H2C–C–N || || HC CH \ / NH |
277 |
4,3 |
+7,5 |
|||||||
Аминокислоты – бесцветные кристаллические вещества; они растворимы в воде, но нерастворимы в органических растворителях; имеют высокую температуру плавления, легко кристаллизуются. Аминокислоты содержат одновременно основную (аминную) NH2 и кислую (карбоксильную) COOH –группы.
Аминокислоты могут быть нейтральными, кислыми и основными, о чем можно судить по их изоэлектрической точке. Для рассмотренных 22 аминокислот она меняется от 2,77 для аспарагиновой кислоты до 10,76 для аргинина. Аминокислоты являются амфолитами: они способны взаимодействовать в растворах как с кислотами, так и со щелочами. Аминокислоты содержат асимметрический атом углерода и могут существовать в виде оптических изомеров. Часто природные аминокислоты вращают плоскость поляризации влево.
Ферментативному расщеплению, происходящему в организме, подвергаются преимущественно L-аминокислоты и их производные. D-ами-нокислоты организмом не усваиваются.
При получении аминокислот синтетическим путем образуются рацематы, которые содержат примерно равное количество L- и D-изомеры.
При нагревании α-аминокислот с нингидрином они окисляются с образованием альдегида, CO2 и NH3. Эта реакция применяется для качественного обнаружения и количественного определения α-аминокислот методом хроматографии на бумаге.
Аминокислоты образуют внутренние соли с катионами тяжелых металлов. Для α-аминокислот характерна внутримолекулярная соль меди, дающая синие кристаллы.
Аминокислоты способны к декарбоксилированию с образованием аминов и выделением CO2, взаимодействуют с альдегидами, реакция идет в щелочной среде, способны взаимодействовать также с кетокислотами.
Аминокислоты способны к дезаминированию. При окислении от аминокислот может отщепляться аммиак с образованием кетокислоты, далее кетокислота может распадаться на альдегид и диоксид углерода.
При нагревании α-аминокислот или их эфиров образуются циклические ангидриды, называемые декетопиперазинами.
Многие из перечисленных выше реакций могут происходить при переработке пищевых продуктов под влиянием влаготепловых воздействий. Эти реакции имеют очень важное значение в технологии пищевых производств, ведущихся с применением тепловых воздействий, так как оказывают большое влияние на качество получаемых продуктов. Например, в результате взаимодействия аминокислот с редуцирующими сахарами образуются темно-окрашенные, так называемые меланоидиновые соединения.
Аминокислоты способны соединяться между собой в длинные цепи посредством пептидной связи (–CO–NH–), которая образуется за счет карбоксилов и аминных групп. При взаимодействии двух аминокислот получается дипептид. В зависимости от числа аминокислотных остатков, образующих молекулу пептида, различают дипептиды, трипептиды, тетрапептиды и т. д. Полипептиды различаются между собой числом аминокислотных остатков, их строением, а также порядком расположения аминокислот в полипептидной цепи.
Полипептидные цепи могут замыкаться в циклы в результате образования пептидной связи между концевыми амино- и карбоксильными группами. Замыкание цепи происходит также в результате образования дисульфатной связи между боковыми цепями.
3.2. Классификация белков
Классифицировать белки, исходя из химического строения, чрезвычайно сложно, так как число белков, полученных из различных объектов (растений, микроорганизмов, органов и тканей животных) очень велико. В настоящее время белки подразделяют на две большие группы – простые и сложные. К простым (протеины) относят белки, состоящие только из аминокислот. Сложные белки (протеиды) содержат кроме аминокислот небелковые (простетические) группы.
3.2.1. Простые белки (протеины)
Условная классификация простых белков основана на их физико-химических свойствах, главным образом на растворимости в различных растворителях (воде, растворах солей, щелочей, спирте). К ним относятся проламины, гистоны, альбумины, глобулины и некоторые другие.
Альбумины растворимы в воде, выпадают в осадок при кипячении и высаливаются насыщенными растворами солей. Они содержатся в яичном белке, сыворотке крови, молоке и семенах растений.
Глобулины в разбавленных растворах нейтральных солей, выпадающие в осадок при разбавлении растворов водой. Они являются основными белками растений, являются антителами сыворотки крови (гамма глобулины) и др.
Глютелины растворимые в слабых растворах щелочей (массовой долей в растворах примерно 0,2 %).
Проламины растворимые в этиловом спирте (объемной долей 70…80 %). Они содержатся в семенах злаков. Вместе с глютеинами образуют запасные белки эндосперма семян. Хлебопекарные качества пшеницы зависят от содержания в зерне проламина, глиадина и глютина, образующих клейковину.
К простым белкам относят также протамины – белки, содержащие 80…90 % (по массе) диаминокарбоновых кислот (лизина, гистидина, аргинина), и гистоны. Протамины (щелочные белки) имеют сравнительно небольшую молекулярную массу, входят в состав спермы и икры рыб.
Гистоны имеют щелочной характер, они входят в состав многих сложных белков: гемоглобина, нуклеопротеидов, лейкоцитов. Они участвуют в поддержании и изменении структуры хромосом на разных стадиях клеточного цикла, в регуляции активности генов.
3.2.2. Сложные белки (протеиды)
К сложным белкам относят: липопротеиды, глюкопротеиды, хромопротеиды, фосфопротеиды, нуклепротеиды и ферменты.
Липопротеиды – белки, связанные с жирами или жироподобными веществами. Известна возможность образования в биологических условиях следующих соединений белка:
белок – ненасыщенные и насыщенные жирные кислоты;
белок – глицериды;
белок – стериды;
белок – стеролы;
белок – фосфолипиды;
белок – цереброзиды;
белок – ретинол (витамин А).
Характер связи при этом может быть различным. Считается, что белки образуют с липидами как устойчивые, так и неустойчивые соединения. Прочность связей зависит как от природы молекул, входящих в состав липопротеина, так и от характера упаковок молекул липопротеина в мицеллах.
В условиях влаготепловой обработки материала, содержащего белки и липиды, возможно образование липопротеиновых комплексов. Кроме того, при переработке масличных семян возможно также высвобождение фосфолипидов масличных семян, находящихся в связанном с белками состоянии, и переход их в масло.
Липопротеиды являются структурными компонентами биологических мембран животных и растительных клеток. Кроме того, они содержатся в плазме крови и нервной ткани человека и животных.
Глюкопротеиды – белки, связанные с высокомолекулярными углеводами. Главными их представителями являются муцины и мукоиды, входящие в состав животных тканей, хрящей, костей.
Хромопротеиды – белки, соединенные с хромофорами – окрашенными соединениями небелкового характера. Окрашенная небелковая (простетическая) группа хромопротеидов может принадлежать к различным классам органических соединений. Например, соединение хлорофилла с белком, осуществляющее фотосинтез в растениях; гемоглобин крови, в котором гем связан с белком глобином. Гем является сложным азотистым основанием, содержащим железо. Хромопротеидами являются ферменты каталаза, пероксидаза, цитохромы.
 О
О О
О


 α-Амино-β-фенил-
пропионовая
(фенилаланин)
α-Амино-β-фенил-
пропионовая
(фенилаланин) α-Амино-β-параокси-фенилпропионовая
(тирозин)
α-Амино-β-параокси-фенилпропионовая
(тирозин)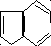 α-Амино-β-индолил-
пропионовая (триптофан)
α-Амино-β-индолил-
пропионовая (триптофан)