Материал: А27137 Проверить Рогов Б.А. Пищевая инженерия производства жировой про
10.3.2. Метаболизм жирных кислот
Свободные жирные кислоты после всасывания в тонкий кишечник и поступления в печень участвуют в различных путях метаболизма (рис. 10.2). Они являются субстратом энергетического обмена в печени. Свободные жирные кислоты прежде всего подвергаются активации и окислению с образованием ацетил-СоА и АТФ.
Избыток ацетил-СоА, не использованный печенью, превращается в кетоновые тела: ацетоацетат и β-D-гидрооксибутират. Эти соединения переносятся кровью в периферические ткани, где окисляются в цикле Кребса.
Свободные жирные кислоты участвуют в биосинтезе холестерина и желчных кислот. Определенная часть ацетил-СоА является основным предшественником в биосинтезе холестерина, который участвует в синтезе желчных кислот, ускоряющих переваривание и всасывание жиров
Свободные жирные кислоты участвуют в биосинтезе липопротеинов плазмы крови, переносящих липиды в жировую ткань.
Свободные жирные кислоты способны связываться с сывороточным альбумином и по кровяному руслу доставляться в сердце и скелетные мышцы, в которых жирные кислоты всасываются и используются в качестве энергетического материала
Рассмотрим более подробно окисление продуктов гидролиза жиров.
Глицерин фосфорилируется аденозинтрифосфатом (АТФ), превращаясь в глицерофосфат, который затем окисляется НАД-содержащим ферментом в диоксиацетонфосфат, который появляется и на одной из стадий окисления глюкозы.
Липиды печени
Липопроте-ины
плазмы
Жирные
кислоты
Свободные
жирные
кислоты плазмы

Цикл
окисления жирных кислот

АТФ
Соли желчных
кислот
Кетоновые тела
Кровь


Холестерин

Ацетил-СоА
АТФ
Цикл
Кребса
Окислительное
фосфорилирование
СО2
+ Н2О
Рис. 10.2. Схема метаболизма жирных кислот в печени.
Прямоцепочечные жирные кислоты окисляются таким образом, что от их молекул в один прием сразу отщепляется по два атома углерода, пока не образуется ацетоуксусная кислота, содержащая всего 4 атома углерода, и та, в свою очередь, расщепляется на два ацетильных (двууглеродных) фрагмента. Процесс отщепления от жирной кислоты одновременно пары атомов углерода получил название β-окисления, так как при этом происходит окисление углеродного атома, находящегося в β-положении по отношению к карбоксильной группе жирной кислоты
R–СН2–СН2–СН2–СООН
γ β α
Подобно окислению глюкозы, β-окисление жирных кислот самопроизвольно не протекает. Для его осуществления необходимо затратить некоторое количество энергии (энергия активации). И здесь энергия поставляется за счет АТФ, но при активировании одной молекулы жирной кислоты расходуются сразу две макроэнергетические фосфатные связи одной молекулы АТФ, которая превращается в аденозинмонофосфат (АМФ). Кроме того, процесс β-окисления жирных кислот в начальной стадии отличается от процесса окисления глюкозы еще и тем, что энергия от АТФ к жирной кислоте переходит не за счет фосфорилирования молекулы субстрата, а путем образования продукта взаимодействия жирной кислоты с коферментом А. Этот процесс катализирует фермент тиокиназа.
Дальнейшее окисление жиров протекает довольно сложно. Так, ацилкофермент А (все остатки жирных кислот типа RСО называются ацилами) окисляется затем ферментом дегидрогеназой флавопротеинового ряда, после чего под действием фермента лиазы по месту двойной связи, образовавшейся в предыдущей реакции, присоединяется молекула воды и образуется β-оксиацилкофермент А.
Далее еще один фермент, на этот раз НАД-содержащий, превращает β-оксиацил-КоА в β-кетоацил-КоА. Последняя реакция заключается в расщеплении углеводородной цепи продукта превращения исходной жирной кислоты. Из отщепляющегося при этом осколка, состоящего из двух атомов углерода и кофермента А образуется ацетил-КоА, а из остатка жирной кислоты – новое ацилпроизводное кофермента А и жирная кислота, в которой на два углеродных атома меньше, чем в исходной молекуле, вступившей в цепь превращений. Эту реакцию называют процессом тиолиза, ее отличительная особенность заключается в том, что молекула кофермента А образует соединение с остатком жирной кислоты RСН2СО без затраты энергии, обычно получаемой за счет АТФ.
Помимо ацетил-КоА, в реакции образуется также активированная форма жирной кислоты – ацил-КоА, которая может превращаться далее, минуя требующую затраты АТФ стадию. Эта новая молекула активированной жирной кислоты вполне подготовлена к тому, чтобы пройти всю серию таких же превращений.
Таким образом, каждая молекула жирной кислоты подвергается в клетке нескольким сериям превращений, состоящим из четырех последовательно протекающих реакций, причем в результате одной такой серии она укорачивается на два атома углерода, которые выделяются в виде ацил-КоА.
Однако окисление жирных кислот все же не столь эффективно, как это кажется на первый взгляд. В приведенных выше материалах мы исходим из того, что вся жирная кислота расщепляется на ацетил-КоА, который далее подвергается окислению. Но, как уже отмечалось, жирные кислоты являются основным поставщиком энергии только во время голодания организма или при диабете, когда в организме образуется в большом количестве ацетоуксусная кислота. Источником этого продукта служит реакция между двумя молекулами ацил-КоА, получающихся при окислении жирных кислот.
Следовательно, образование каждой молекулы ацетоуксусной кислоты сначала накапливается в печени, а затем выбрасывается из нее. Это означает, что две молекулы ацетил-КоА с запасенной в них потенциальной энергией, которая должна была бы выделиться при окислении, не входят в цикл. Выделение из организма ацетоуксусной кислоты является ни чем иным, как выбрасыванием топлива, которое сгорело лишь наполовину.
Причины этого лежат в том, что для работы цикла необходима щавелево-уксусная кислота, получающаяся из пировиноградной кислоты. Но пировиноградная кислота – продукт метаболизма глюкозы, а не окисления жирных кислот. Это означает, что при углеводном голодании организма дополнительное снабжение клеток щавелево-уксусной кислотой резко понижено. Иначе говоря, когда отсутствуют углеводы, клетка, вынужденная искать источник энергии в жировых запасах организма, оказывается не в состоянии использовать это горючее эффективно, как если бы имела дело с глюкозой – источником необходимой щавелево-уксусной кислоты. Этот пример позволяет еще раз подчеркнуть важность углеводов для энергетического обмена веществ.
Таким образом, свободные жирные кислоты в печени используются как энергетический материал, участвуют в синтезе триацилглицеринов, холестерина, липопротеинов плазмы, кетоновых тел, поставляемых по кровяному руслу в другие ткани организма.
10.3.3. Метаболизм аминокислот
Аминокислоты после всасывания в тонкий кишечник и поступления в печень транспортируются через систему кровообращения в другие органы и ткани, где они участвуют в биосинтезе тканевых белков, белков печени и плазмы.
Аминокислоты, не использованные в печени и других органах для синтеза белков, подвергаются дезаминированию, распадаются с образованием ацетил-СоА и промежуточных продуктов цикла Кребса. Эти соединения могут участвовать в синтезе глюкозы и гликогена.
Ацетил-СоА может подвергаться окислению в цикле Кребса с запасанием энергии в форме АТФ или превращаться в жирные кислоты и липиды, откладывающиеся в запас.
Клетка получает энергию за счет белков путем окисления углеродного скелета аминокислот, из которых состоят белки. Поскольку в клетке много разных аминокислот, сильно различающихся по структуре, нет ничего удивительного в том, что существует несколько схем окисления аминокислот. Во всех этих схемах, впрочем, принцип деструкции аминокислот один и тот же: аминокислота сначала лишается своей аминогруппы, а образующееся соединение тем или иным способом превращается в вещества, лежащее на прямом пути окисления глюкозы или жирных кислот, где запасенная в нем энергия утилизируется клеткой по одной из уже рассмотренных серий реакций.
Аминокислоты, поставляющие таким путем субстраты в схему окисления глюкозы или в цикл лимонной кислоты, называются глюкогенными, те же аминокислоты, которые перед окислением образуют вещества, лежащие на пути метаболизма жирных кислот, называются кетогенными.
Живая клетка располагает несколькими способами отщепления аминного азота от аминокислот. Одним из таких способов, например, является прямое окисление, то есть процесс, когда аминокислота сначала утрачивает два атома водорода – дегидрогенизируется (они переходят к акцептору), а затем гидролизуется водой, в результате чего образуется аммиак:
R–СНСООН ↔ R–ССООН + 2Н
│ ║
NН2 NН
аминокислота иминокислота
R– ССООН + Н2О → NН3 + R–СОСООН
║
NН
иминокислота кетокислота
Второй продукт реакции представляет собой α-кетокислоту, дальнейшая судьба которой зависит от породы радикала R в ее молекуле. Процессы данного типа катализируются специфическими ферментами – оксидазами аминокислот, тогда как реакции гидролиза иминокислот, в результате которых образуются кетокислоты, протекают самопроизвольно, без участия ферментов.
В результате распада аминокислот путем дезаминирования выделяется аммиак. Но аммиак – сильно действующее отравляющее вещество для клеток. В связи с этим в организме животных выработалась система, обеспечивающая безопасное выведение аммиака: аммиак превращается в безвредное для организма вещество – мочевину, которая поступает в кровь, оттуда в почки, а затем в мочу, не вызывая при этом никаких вредных эффектов. Процесс превращения белкового азота в мочевину протекает почти исключительно в клетках печени.
При нормальных условиях в организме поддерживается «азотный баланс»: количество азота, поступающего из кишечника в виде аминокислот, строго эквивалентно количеству азота, выбрасываемого в виде мочевины. В условиях голодания баланс нарушается: количество азота в моче повышается, так как белки организма, из которых образуется мочевина, окисляются с выделением энергии быстрее, чем восполняются их потери за счет поступающей в организм пищи. Если количество азота, выделяемого таким путем, возрастает изо дня в день, то в конечном итоге может завершиться летальным исходом, когда организму не удается сохранить даже незначительную часть своего белка.
Тот факт, что моча всегда содержит значительное количество мочевины, даже когда тело вполне здорово и нормально функционирует, указывает на постоянно протекающее в организме расщепление белка. Разумеется, клетка учитывает, какое количество энергии образуется при расщеплении белка, вследствие чего этот процесс, как и расщепление жиров, постоянно вносит свой вклад в общий энергетический баланс клетки, даже при поступлении в нее остаточных количеств углеводов. В нормальных условиях, однако, роль жиров и белков, как источников энергии, необходимой для организма, совсем незначительна.
Кроме того, аминокислоты участвуют в цикле «глюкоза-аланин». При недостатке уровня глюкозы в крови в печень из мышц поступает аминокислота аланин. Она образуется в результате частичного протеолиза мышечных белков до аминокислот и их пререаминирования. Аланин в печени дезаминируется с образованием пирувата, который превращается в глюкозу крови путем глюконеогенеза. Недостаток аминокислот, возникающий при этом в мышцах, восполняется за счет всасывания аминокислот пищи.
Аминокислоты принимают участие также в синтезе нуклеотидов, различных гормонов и других азотсодержащих соединений.
Таким образом, аминокислоты в печени используются для синтеза белков печени, плазмы, тканей, могут превращаться в глюкозу и гликоген, подвергаться дезаминированию с образованием аммиака, участвующего в цикле мочевины, превращаться в нуклеотиды и другие азотсодержащие вещества (рис. 10.3).
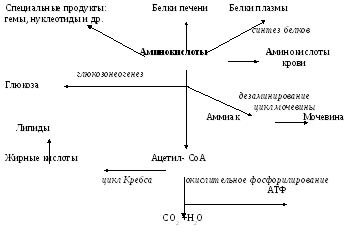
Рис. 10.3. Схема метаболизма аминокислот в печени