Материал: А27137 Проверить Рогов Б.А. Пищевая инженерия производства жировой про
Газообразные
продукты
Рис. 2. Схема превращения жиров
В топленых жирах автолитического (ферментативного) расщепления жиров не наблюдается, так как в процессе вытопки при температуре около 60 °С липаза, содержащаяся в жировой ткани, инактивируется. Гидролитическая порча топленого жира происходит при наличии влаги, в результате обсеменения микрофлорой, неполной денатурации белков при вытопке жира из жировой ткани, или под воздействием катализаторов.
Окислительные изменения. В процессе переработки и хранения жиров возможно ухудшение их качества в результате окислительных процессов, глубина и скорость которых зависят от природных свойств жира, температуры, наличия кислорода и света. Эти факторы могут вызвать окислительную порчу жиров.
Различают автоокисление и термическое окисление жиров. Автоокисление жиров протекает при низких температурах в присутствии газообразного кислорода. Термическое окисление происходит при температуре 140200 °С. Между термическим и автоокислением есть много общего, однако состав образующихся продуктов несколько различается.
Продукты, образующиеся при автоокислении и термоокислении, подразделяются на три группы:
1. Продукты окислительной деструкции жирных кислот, в результате которой образуются вещества с укороченной цепью.
2. Продукты изомеризации, а также окисленные ацилглицерины, которые содержат то же количество углеродных атомов, что и исходные ацилглицерины, но отличаются от последних наличием в углеводородных частях молекул жирных кислот новых функциональных групп, содержащих кислород.
3. Продукты окисления, содержащие полимеризованные или конденсированные жирные кислоты, в которых могут находиться и новые функциональные группы, имеющие в своем составе кислород.
Кроме того, продукты окисления делятся на термостойкие и нетермостойкие.
Первичными продуктами окисления являются перекиси, активирующие окисление других молекул. Благодаря этому реакция окисления носит цепной характер. Механизм окисления жиров в настоящее время изучен. Теория цепных реакций разработана академиком Н. Н. Семеновым и его учениками при изучении кинетики химических процессов. Процессы окисления жиров подробно изложены в ряде учебников, поэтому в данном разделе подробно не излагаются.
Окислению подвергаются в первую очередь ненасыщенные жирные кислоты, но могут окисляться также и насыщенные кислоты с образованием гидроперекисей. При глубоком окислении жиров возможно образование циклических перекисей СНСНСНСН2 и
О – О
эпоксидных соединений СНСНСН2
\ / О
Содержание перекисных соединений в жире оценивают по величине перекисного числа. Это довольно чувствительный показатель, и по его значению судят о начале и глубине окисления жира. В свежем жире перекисей нет. На начальных стадиях окисления в течение некоторого времени химические и органолептические показатели жира почти не изменяются. Этот период, имеющий различную продолжительность, называется индукционным. После индукционного периода жир начинает портиться. Обнаруживается это по увеличению перекисного числа и изменению органолептических свойств жира.
Наличие индукционного периода объясняется тем, что в начале процесса молекул с повышенной кинетической энергией (возбужденных или свободных радикалов) очень мало. Обусловлено это также содержанием в жире естественных антиокислителей: каротиноидов, токоферолов, лецити-нов, которые более активно взаимодействуют со свободными радикалами и с кислородом воздуха и тем самым препятствуют окислению жиров. Продолжительность индукционного периода зависит от концентрации антиокислителей, природы жира и условий переработки и хранения.
Животные жиры, в составе которых меньше ненасыщенных жирных кислот, более устойчивы, чем растительные.
Процесс автоокисления жиров значительно ускоряется в присутствии влаги, света и катализаторов. Такими катализаторами могут быть легкоокисляющиеся металлы (окислы или соли железа, меди, свинца, олова), а также органические соединения, содержащие железо, белки, гемоглобин, цитохромы и другие.
Каталитическое действие металлов основано на способности их легко присоединять или отдавать электроны, что приводит к образованию свободных радикалов из гидроперекисей жирных кислот.
Активными катализаторами являются ферменты, главным образом ферменты микроорганизмов. Поэтому загрязнение жиров, особенно бактериальное обсеменение, ускоряет процесс окисления жиров.
Перекиси и гидроперекиси являются неустойчивыми соединениями, поэтому происходит их распад с образованием свободных радикалов, например, RООН RО + ОН и других.
При этом протекают последующие разнообразные реакции, в результате которых накапливаются вторичные продукты: оксисоединения, альдегиды, кетоны, низкомолекулярные кислоты и другие.
При окислении жиров обнаружен ряд альдегидов, представляющих собой продукты распада цепи жирных кислот: нониловый, азолаиновый, гептиловый, малоновый. Дальнейшее превращение низкомолекулярных альдегидов ведет к появлению низкомолекулярных спиртов, жирных кислот и к новому разветвлению окислительной цепи.
Кетоны, как и альдегиды, образуются окислительным путем в результате дальнейших превращений перекисей, например, в результате их дегидратации.
СН2СНСН2 СН2ССН2 + Н2О
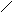
![]()
ООН О
Предполагают, что в присутствии ферментов микроорганизмов кетоны могут образовываться по типу -окисления, т. е. с участием воды.
5.6. Окислительная порча жиров
При окислении жиров теряется естественная окраска; специфический вкус и запах продукта; появляется посторонний, иногда неприятный привкус, аромат; теряется биологическая ценность.
Первичные продукты окисления перекиси органолептически не обнаруживаются, однако, по их содержанию можно судить о глубине порчи жира, пригодности его для длительного хранения и употребления в пищу.
Вторичные продукты окисления ухудшают органолептические показатели жира. При этом различают два основных вида порчи жира прогоркание и осаливание.
Прогоркание происходит в результате накопления в жирах низкомолекулярных продуктов: альдегидов, кетонов, низкомолекулярных жирных кислот. В этом случае жир приобретает прогорклый вкус и резкий, неприятный запах. Прогоркание жиров может происходить вследствие химических и биохимических процессов.
При химическом прогоркании, протекающем в жире под действием кислорода воздуха, накапливаются свободные жирные кислоты, иногда низкомолекулярные, не свойственные данному жиру, увеличивается перекисное число, образуются летучие карбонильные соединения альдегиды и кетоны. Именно эти соединения придают запах прогорклости жиру.
При биохимическом прогоркании, протекающем с участием ферментов плесеней, образуются кетокислоты и метилалкилкетоны в результате -окисления свободных жирных кислот, образующихся при гидролизе под действием липаз. При этом из кислот образуются кетоны, содержащие на один атом углерода меньше, чем в исходной кислоте: из капроновой метилпропилкетон, каприновой метилгептилкетон, лауриновой метилонилкетон и т. д.
Кетонное прогоркание иногда называют "душистым прогорканием" в связи со своеобразным запахом продуктов окислительной порчи.
Осаливание
жиров сопровождается исчезновением
окраски, уп-лотнением жира и появлением
салистой консистенции в результате
окислительных изменений жира. При
осаливании образуется значительное
количество оксисоединений в результате
распада на свету первичных органических
перекисей и появления свободных радикалов
![]() ОН
и НО
ОН
и НО![]() при фотохимическом воздействии на
жир.
при фотохимическом воздействии на
жир.
Возникающие радикалы, взаимодействуя с молекулами жирных кислот, образуют оксикислоты. Количество их определяют по ацетильному числу, которое возрастает с увеличением количества оксигрупп.
Образовавшиеся оксикислоты вовлекаются в процесс полимеризации, в результате чего образуются высокомолекулярные соединения и жир приобретает характерную салистую, мазеобразную консистенцию. Осалившийся жир характеризуется также специфическим неприятным запахом и вкусом.
Изменение окраски жиров связано с разрушением каротиноидов, которое наступает до начала окислительных изменений. При этом жир обесцвечивается, иногда принимает зеленоватую окраску, изменяется его спектр поглощения. Эти изменения каротиноидов позволяют обнаружить окислительные изменения жиров на ранних стадиях. При этом происходит распад токоферолов.
Наиболее интенсивно окислительная порча происходит из-за продолжительного нагрева жиров при высоких температурах 180300 °С. Такой нагрев сопровождается снижением содержания ненасыщенных жирных кислот и накоплением перекисей, карбонильных соединений, летучих кислот и продуктов сополимеризации.
При температуре свыше 200 °С может произойти термическое разложение жира с выделением дыма (пиролиз). Температура, при которой на-чинается выделение дыма, называется температурой (или точкой) дымообразования, или пиролиза. На эту температуру оказывают влияние вид жира, содержание свободных жирных кислот, материал и размер посуды, наличие металлов и другие факторы. Например, увеличение в свином жире содержания свободных жирных кислот с 0,02 до 0,81 % уменьшает температуру пиролиза с 221 до 150 °С. Железо и медь катализируют пиролиз жира.
Продукты пиролиза ухудшают цвет жира при жарке пищевых продуктов. Потемнение жира происходит за счет загрязнения его веществами пиролитического распада, образующихся при обугливании мелких частиц, реакций меланоидинообразования и карамелизации, а также накопления темноокрашенных продуктов окисления самого жира.
Изменение запаха жира при длительной жарке продуктов вызвано образованием акролеина. Образующиеся при жарке карбонильные соединения, содержащие 3, 5, 7 атомов углерода, ухудшают запах и вкус жира, а содержащие 4, 6, 10, 12 атомов углерода придают жиру приятный запах жареного.
Изменение биологической ценности жира. В результате окисления изменяются не только органолептические свойства жира, но и снижается его пищевая, в том числе биологическая ценность. Это связано с окислением жизненно необходимых ненасыщенных жирных кислот, а также с разрушением каротиноидов, токоферолов, фосфатов и других биологически активных веществ. Кроме того, первичные продукты окисления, перекиси оказывают токсическое действие на организм. Перекиси в процессе разнообразных реакций образуют вещества, содержащие карбонилы, а также полимерные соединения, ухудшающие усвояемость жира, снижающие биологическую ценность, а иногда обладающие канцерогенными свойствами. Накопление таких продуктов специфического состава и строения происходит наиболее интенсивно при продолжительном нагревании жира при высоких температурах (выше 180 °С).
Для предотвращения окислительных процессов в жирах необходимо уменьшить или исключить контакт жира прежде всего с кислородом воздуха. Без доступа кислорода даже длительное нагревание при 180190 °С не вызывает заметных окислительных изменений жира. Увеличению контакта с воздухом способствует нагревание жира тонким слоем, жарка продуктов пористой структуры, сильное вспенивание и перемешивание жира.
Сравнительно недавно для стабилизации фритюрных жиров стали применять кремнийорганические жидкости (полиметилсилоксаны). Эти соединения, образуя на поверхности жира тонкую пленку и подавляя его вспенивание, затрудняют взаимодействие жира с кислородом.
Жир целесообразно хранить в герметичной таре, в вакуумной упаковке или в атмосфере инертного газа при отрицательных температурах. В жирах не должно быть легкоокисляющихся металлов (меди, железа, марганца), их солей или органических производных соединений свинца, олова и других металлов. Для замедления окислительных процессов в жирах применяют антиоксиданты.
6. Витамины
Витамины – низкомолекулярные органические соединения различной химической природы, необходимые в незначительном количестве для нормального обмена веществ и жизнедеятельности. Они необходимы для процессов усвоения всех пищевых веществ, для роста и восстановления клеток и тканей. Многие витамины являются предшественниками коферментов, в составе которых участвуют в различных ферментативных реакциях. Человек и животные или не синтезируют витамины, или синтезируют их в недостаточном количестве и поэтому очень важно получать витамины с пищей. Источником витаминов обычно служат растения. Некоторые витамины образуются микрофлорой кишечника. Многие витамины, используемые как лекарственные препараты, получают химическим или микробиологическим синтезом.
Длительное употребление пищи, лишенной витаминов, приводит к серьезным заболеваниям (авитаминозам). Поэтому витамины относятся к незаменимым факторам питания животных организмов.
Вначале витамины условно обозначали буквами латинского алфавита. В дальнейшем были приняты единые международные названия, отражающие их химическую структуру. Все витамины делятся на водорастворимые, жирорастворимые и витаминоподобные соединения.
6.1. Водорастворимые витамины и витаминоподобные вещества
Аскорбиновая кислота (витамин С) представляет собой ненасыщенное соединение, не содержащее свободной карбоксильной группы. Кислый характер ее водных растворов обусловлен освобождением водородных ионов при растворении в воде благодаря диссоциации фенольных гидроксилов.
С
=
О С =
О
│ │
НОС
–2Н О =
С
║ │
НОС
О О =
С
│ +2Н
│ О
НС
НС
│ │
НОСН
НОСН
│ │
СН2ОН
СН2ОН
аскорбиновая
дегидроаскорбиновая
кислота
кислота
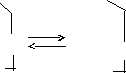
Аскорбиновая кислота легко подвергается окислению. Продукт ее окисления – дегидроаскорбиновая кислота – при восстановлении превращается в аскорбиновую кислоту. Она представляет собой белое кристаллическое вещество, легко растворимое в воде; плавящееся при температуре 190…193 °C; оптически активное ([α] = +24 гр/дм в воде).
Аскорбиновая кислота довольно неустойчивое соединение. Она легко окисляется как в щелочной, так и в кислой среде. Особенно быстро аскорбиновая кислота окисляется в присутствии солей тяжелых металлов.
Аскорбиновая кислота играет определенную роль как переносчик водорода в окислительных процессах, происходящих в организме, а также в превращениях аминокислот — триозина и фенилаланина.
Аскорбиновая кислота широко распространена в продуктах растительного происхождения. Наиболее богаты аскорбиновой кислотой ягоды черной смородины и рябины, апельсины, лимоны, мандарины, шиповник, хвоя, укроп, перец, хрен, капуста и т. д.
Человек должен обязательно получать аскорбиновую кислоту с пищей. Авитаминоз вызывает заболевание цингой, сопровождающееся по-вышенной проницаемостью и хрупкостью кровеносных сосудов, а также повреждением костей и, особенно, зубов. С лечебной целью витамин С принимается при цинге, желудочно-кишечных заболеваниях, атеросклеро-зе и др.