Материал: UnEncrypted

можна поділити на три групи. У першій групі об’єднуються транзисторні аналоги, що складаються з транзисторів однієї структури. Другу групу складають аналоги, виконані на транзисторах різної структури, але не складовий еквівалент p-n-p-n-структури. Третя група складається з транзисторних еквівалентів p-n-p-n-структури. Використання в таких схемах перехресних зв'язків обмежує їхнє застосування частотами до 1 ГГц.
Зокрема, з бурхливим розвитком твердотільної НВЧ-електроніки особливо гостро постало завдання мініатюризації частотовибіркових кіл. Розв’язання завдання шляхом використання об'ємних резонаторів, відрізків лінії передачі, сегнетоелектричних і феритових резонаторів неможливе, тому що їхня добротність зменшується зі зменшенням розмірів. Коливальні контури на базі негатронів таких недоліків не мають, що дозволяє розв’язувати задачу з реалізації в одному кристалі декількох десятків високодобротних коливальних контурів (фільтрів, LC-генераторів і т.д). Крім R-негатронів ведуться дослідження зі створення і застосування C- і L-негатронів. Це прилади або їхні схемотехнічні аналоги, що мають за
певних умов |
негативну |
диференціальну ємність |
C = ∂Q ∂U < 0 |
або |
ндуктивність |
L = ∂ψ ∂i < 0 , |
відповідно. Практичне |
застосування |
таких |
негатронів у наш час не одержало широкого поширення і вимагає подальших досліджень і пошуку напрямків їхнього ефективного використання.
20
2 СТРУКТУРА І ФІЗИКО-МЕХАНІЧНІ ВЛАСТИВОСТІ ТВЕРДИХТІЛ
2.1 Кристалізація і склування
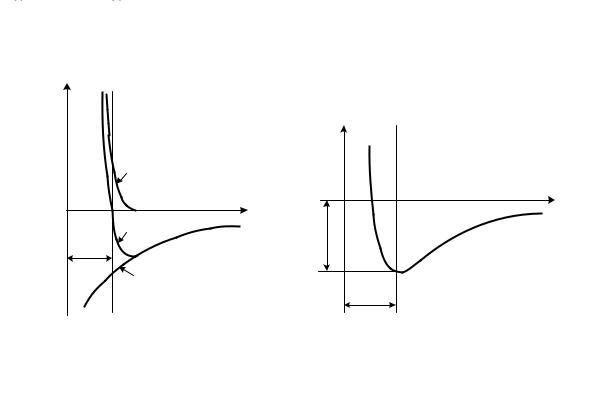
При достатньому зближенні частинок між ними виникають сили взаємодії ( forces interworking). Незалежно від природи цих сил, загальний характер їх залишається однаковим (рис. 2.1,а): на відносно великих відстанях виникають сили тяжіння ( forces interworking) Fпр, що збільшуються із зменшенням відстані між частинками r (крива 1); на невеликих відстанях виникають сили відштовхування Fвід, які із зменшенням r збільшуються значно швидше, ніж Fпр (крива 2). Так, для іонних кристалів Fпр ~1/ r2, а Fвід ~1/ r 9.
На відстані r=r 0 сили відштовхування врівноважують сили тяжіння і
результуюча сила F звертається в нуль (крива 3). Оскільки F=U/r, де U – енергія взаємодії частинок, то при r=r0 величина U досягає мінімального значення, рівного – Uсв (рис. 2.1, б). Тому стан частинок, що зближують на відстань r0, є станом стійкої рівноваги, внаслідок чого під впливом сил взаємодії частинки повинні б розташовуватися в строгому порядку на відстані r0 один від одного, утворюючи тіло з правильною внутрішньою структурою.
Проте крім потенційної енергії (potential energy) взаємодії частинки мають кінетичну енергію (kinetic energy) теплового руху, намагаючись зруйнувати порядок в їх розташуванні. Стан і властивості речовини визначаються відносною роллю цих двох чинників. В газоподібному стані відстані між частинками такі великі, що сили взаємодії між ними практично не виявляються. Тому в проміжках між зіткненнями, що носять випадковий характер, частинки поводяться фактично як вільні, створюючи хаотичний поступальний рух. Фіксованих положень рівноваги вони не мають.
У рідинах, густина яких приблизно на три порядки вища густини їх насиченої пари, відстані між молекулами r зменшуються, а сили взаємодії збільшуються настільки, що молекули не можуть вільно переміщатися в просторі: кожна молекула виявляється мовби укладеною в комірку, створену сусідніми молекулами, в якій вона створює безладні коливання біля тимчасових положень рівноваги (рис. 2.2, а). Позначимо період цих коливань τ0, а висоту потенційного бар'єра, який створює для даної молекули її оточення, U. Вірогідність того, що ця молекула набуває енергії теплового руху, достатньої для подолання потенційного бар'єра і переходу в нове положення рівноваги, рівна ехр (- U / KT ), де К – постійна Больцмана; Т – абсолютна температура. За одиницю часу молекула, що коливається, «підходить» до бар'єра V0 = 1/τ0 раз. Помножуючи це число на вірогідність ехр(- U / KT ), одержуємо середнє число переходів молекули з одних
21
положень рівноваги за інші за одиницю часу; v = 1/ t 0 ехр(- U / KT ).
Величина τ, зворотна ν, виражає середній час «осілого життя» молекули, яке вона проводить, коливаючись біля даного положення рівноваги:
t=t0 exp(U/KT). |
(2.1) |
Для простих рідин, таких, наприклад, |
як розплавлені метали, |
t 

 10-10 с; t0
10-10 с; t0 


 10-10 с. Отже, біля кожного положення рівноваги молекула
10-10 с. Отже, біля кожного положення рівноваги молекула
робить приблизно 103 коливань потім переходить в нове положення рівноваги і т.д.
Рисунок 2.1 – Залежністьсиливзаємодії(а) іпотенціальноїенергіївзаємодії атомів(б) відвідстаніміжними
Подібних переходів вона робить 1010 за секунду, що приводить до інтенсивного руху її по всьому об'єму рідини. Цей рух і обумовлює основну властивість рідини – текучість, за кількісну міру якої приймають в'язкість h. Наведені міркування показують, що в'язке протікання рідин є типовим активаційним процесом, що протікає з енергією активації U. Звичайно цю енергію ( energy) відносять до моля речовини і вираз (2.1) записують так:
t = t 0 exp(Ua / RT ) , |
(2.2) |
де Ua– енергія активації; R – універсальна газова стала.
При зниженні температури і переході речовини в твердий стан відстані між молекулами ще дещо зменшуються і енергетично вигідною стає перебудова частинок з утворенням правильної структури, в якій кожна з частинок виявляється укладеною в комірку постійних розмірів і постійного розташування (рис. 2.2, б). Оскільки така структура є щільнішою, то потенціальний бар'єр, що оточує частинку, підвищується в порівнянні з рідким станом. Разом зі зниженням температури це призводить до того, що частота переходу частинок з комірки в комірку
22
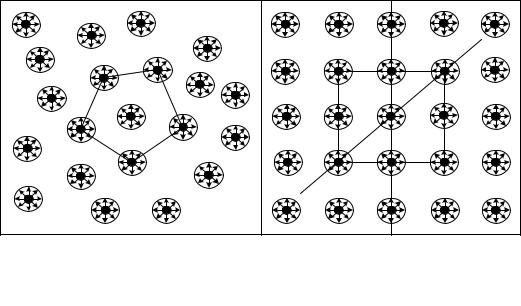
різко зменшується. Частинки фактично закріплюються в певних положеннях рівноваги, роблячи біля них коливання з частотою v = 1018 - 1014 c- 1 , і лише час від часу (приблизно раз протягом декількох діб) можуть переходити з однієї комірки в іншу.
Рисунок 2.2 – Розташуваннячастинокврідинах(а) ітвердих кристалічнихтілах(б)
Із структурної точки зору ці три стани речовини розрізняються порядком розташування частинок одна відносно одної – своєю внутрішньою структурою (structure).
Твердому кристалічному стану властива наявність так званого далекого порядку, тобто строгої повторюваності в будь-яких напрямах, наприклад, АА, ВВ і т. д., одного і того ж елементу структури – атома, групи атомів або молекул (рис. 2.2, б). Геометрично така строга періодичність описується завданням кристалічних граток. У фізичних відношеннях тіла з подібною структурою в загальному випадку анізотропи ( anisotropy) – їх властивості залежать від напряму в гратках.
Для рідкого стану характерна відсутність далекого порядку, але наявність так званого близького порядку – певної взаємної упорядкованості в розташуванні елементів структури (рис. 2.2, а). Проте ця впорядкованість порівняно швидко втрачається і вже на відстані, порівняній з розмірами структурних елементів, зникає майже повністю.
У газоподібному стані відсутній як далекий, так і близький порядок. Близький порядок, властивий рідкому стану, не є стабільним:
впорядковані групи молекул безперервно руйнуються тепловим рухом, створюються знову і т. д. Тому для кожної температури можна говорити лише про деякий усереднений близький порядок і деяку усереднену рівноважну структуру рідини з властивою їй енергією активації процесу руху молекул, що обумовлює в'язкість. При зміні температури відбувається
23
перегруповування молекул і встановлення нового рівноважного стану. |
|||||||||
Подібний процес встановлення в системі рівноваги називається |
|||||||||
релаксацією (relaxation), а час, протягом якого рівновага встановлюється, |
|||||||||
називається часом релаксації τ. За порядком величини він дорівнює часу |
|||||||||
«осілого життя» молекул, визначуваному співвідношенням (2.2); З цього |
|||||||||
співвідношення видно, що із зменшенням енергії активації Ua і |
|||||||||
підвищенням температури Т час встановлення рівноважної структури |
|||||||||
рідини різко зменшується. У низькомолекулярних простих рідинах τ |
|||||||||
настільки мале (10-10с), що встановлення рівноваги в них протікаєпрактично |
|||||||||
миттєво. Зі зниженням температури час релаксації збільшується, проте, аж до |
|||||||||
температури кристалізації (плавлення) він залишається ще настільки малим, |
|||||||||
що не тормозить процес перегруповування частинок і створення з них |
|||||||||
енергетично вигідної при цій температурі просторово впорядкованої |
|||||||||
структури – кристала. Тому процес кристалізації таких рідин протікає |
|||||||||
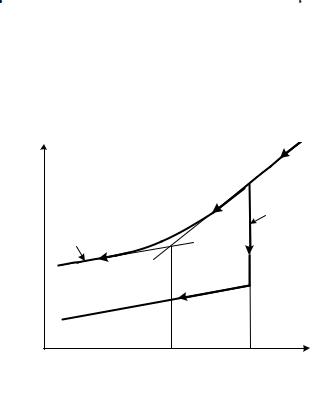
практично стрибкоподібно (крива 1 на рис. 2.3) і одержати їх в |
|||||||||
переохолодженомустанінадзвичайно важко. |
|
|
|
|
|||||
Інакше кажучи, з розплавами високомолекулярних неорганічних і |
|||||||||
органічних сполук типу скла і полімерів (polymer), між великими |
|||||||||
молекулами таких сполук через їх взаємне переплетення вже в рідкому стані |
|||||||||
встановлюється, як правило, сильна взаємодія. Це обумовлює високу |
|||||||||
енергію активації |
Ua і, отже, |
високу в'язкість h і великий час релаксації τ |
|||||||
таких розплавів. Так, поблизу точки плавлення в'язкість заліза приблизно |
|||||||||
дорівнює |
740-3 |
Па с, |
а |
в'язкість |
кварцу |
106 |
Па с. |
Тому |
при |
охолоджуванні розплавів високомолекулярних сполук в'язкість і час |
|||||||||
релаксації збільшуються настільки, що практично запобігають можливості |
|||||||||
перебудови елементів структури в упорядкованому стані за певний час. |
|||||||||
Тому розплав, майже не змінюючи своєї внутрішньої структури, |
|||||||||
переходить в твердоподібне або, як прийнято говорити, склоподібний стан |
|||||||||
(glassy condition). |
|
|
|
|
|
|
|
|
|
Рисунок 2.3 – Зміна питомого об’єму у процесі кристалізації (1) і |
|||||||||
|
|
|
|
склування (2) |
|
|
|
|
|
24