Материал: Polioxialkanoaty_POA__biorazrushaemye_polimery_dlya_meditsiny
Таблица 3.1 Свойства полиоксиалканоатов различного состава (Madison and Huisman, 1999)
|
|
|
Тип полимера |
|
|
||
Параметр |
|
|
|
|
|
|
|
3(ПОБ) |
3(ПОБ-со- |
3ПОБ-со- |
3(ПОО-со- |
Полипропилен |
|||
|
|||||||
|
ПОВ) |
4-ПОБ |
|
ПОГ) |
|||
|
|
|
|
||||
Тпл ( С) |
177 |
145 |
150 |
|
61 |
176 |
|
Тст ( С) |
2 |
–1 |
–7 |
|
–36 |
–10 |
|
Кристалличность (%) |
70 |
56 |
45 |
|
30 |
60 |
|
Растяжение |
|
|
|
|
|
|
|
при разрыве (%) |
5 |
50 |
444 |
|
300 |
400 |
|
Свойства ПОА определяются их строением, прежде всего, они зависят от строения боковых групп в полимерной цепи, а также от расстояния между эфирными группами в молекуле (рис. 3.1).
Уже сейчас на примере только нескольких типов ПОА показано, что свойства ПОА меняются очень значительно в зависимости от типа и соотношения мономеров в полимерной цепи (таблица 3.1). В результате этого на базе ПОА можно иметь спектр материалов с различными физико-механическими свойствами, пригодными для различных применений.
3.1.1. Поли-3-оксибутират (3-ПОБ)
Первым среди выделенных и наиболее полно к настоящему моменту охарактеризованным полиоксиалканоатом является полиоксибутират (ПОБ). Полиоксибутират (С4H6O2) является гомополимером D(-)-3- -оксимасляной кислоты и представляет собой изотактический полиэфир с регулярными, повторяющими единицами (С4H6O2). В отличие от сложных синтетических полиэфиров, полиоксибутират – это стереорегулярный оптически активный полимер, который образует спирали в растворе и кристаллизуется в сферолиты.
Внутри клеток ПОБ, как и другие ПОА, аккумулируется в цитоплазме в виде сферических включений (гранул) (рис. 3.2) и находится в гранулах в подвижном аморфном состоянии. Количество гранул в клетке может составлять от 2–4 до 12. На 98 % гранулы состоят из полимера. В составе гранул присутствуют также фосфолипиды и белки в количестве, соответственно, 2.1 мг и 0.2 μм на 100 г полиме-
ра (Dawes and Senior,1974; Ellar et al., 1973). Гранулы заключены в мембрану толщиной 2–4 мкм.
Гранулы образованы фибриллярными структурами, которые представляют собой двойные нити в виде закрученных вправо лент. Последние образуют мицеллообразные кристаллы полимера (Alper and Lundgren, 1963). Плотность и высокая гидрофобность полимерных цепей в гранулах связана с наличием ограничивающих фосфо-
105
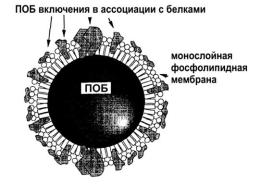
Рис. 3.2. Модель структуры гранул ПОБ in vivo в ассоциации со специфическими белками-фазинами. Соотношение сердцевины и мембраны на рисунке даны не в реальном масштабе (Sudesh et al., 2000).
липидных оболочек, которые расположены монолинейно и укреплены белковыми структурами (Senior, 1984).
В живых клетках ПОБ в гранулах находится в мобильном состоянии, но не в растворенном. Установлено, что вода ассоциирована в части гранул и в какой-то мере выполняет роль пластификатора (Bonthrone et al., 1992), хотя роль воды как пластификатора полимера, не выяснена четко. Выявлено, что ферменты, катализирующие реакции синтеза ПОА, активны только в мобильном гидратированном материале и что в твердых гранулах, характерных для высушенных клеток, они в процессе сушки инактивируются. Белки, ассоциированные в мембране, представлены как ферментами, так и не катализирующими белками, которые названы фазинами (Steinbüchel et al.,1995). На примере Bacillus megaterium более 30 лет назад установлено, что гранулы ПОБ состоят на 97.7 % из полимера, а также белка и липидов; на долю которых приходится 1.87 и 0.46 % соответ-
ственно (Lundgren et al., 1964; Griebel et al.,1968). Внутренняя часть гранулы образована гидрофобным аморфным ПОБ, монослойной фосфолипидной мембраной, содержащей ферменты (рис. 3.2).
3.1.2. Кристаллизация 3-ПОБ
Только после экстракции полимера из клеточной массы неполярными растворителями начинается процесс кристаллизации поли-
оксибутирата (Anderson, Dawes, 1990; Doi, 1995). Кристаллизация полимера находится под кинетическим контролем и ингибируется субмикронными частицами, в которых ассоциированы белки и фос-
фолипиды (Bonthrone et al., 1992).
Полиоксибутират представляет собой бесцветное полукристаллическое гидрофобное вещество. Плотность аморфной фазы ПОБ составляет 1.177 г/см3, кристаллической – 1.23–1.26 г/см3 (Brandl et al., 1988; Waddington, 1994). В ПОБ кристаллическая фаза доминирует над аморфной. Изотактический полиоксибутират по строению сходен с изотактическим полипропиленом; у обоих пендантные метиловые группы прикреплены и ориентированы в полимерной цепи в единственной конформации (Brandl et al., 1988). Полиоксибутират
106
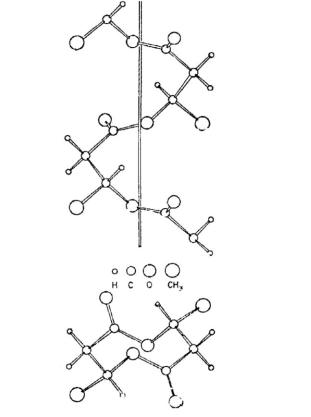
Рис. 3.3. Модель молекулы полиоксибутирата, построенная на базе рентгеноструктурного и конформационного анализа
(Cornibert and Marchessault, 1972).
представлен плотно упакованными двойными спиралями, повторяющимися на расстоянии 5.95 Ă и двукратно закрученными вправо вокруг оси. Конформация спирали стабилизируется взаимодействием карбонил-метильных групп и не зависит от гидроксильных групп. Цепь оксибутирата имеет 21 спиральную конформацию, орторомбические ячейки в решетке при пространстве группы P212121 характеризуются следующими параметрами: а=5.76 Ẫ, в=13.20 Ả, с=5.96А
(Yokouchi et al., 1974).
Кристаллическая структура ПОБ исследована рентгеноструктурным анализом ориентированных полимерных волокон. Рентгенограммы волокон показали повторение вдоль оси цепи на расстоянии 0.596 мкм плотно упакованных двойных антипараллельных цепей, упакованных в орторомбические ячейки решетки (Okamura and Marchessault, 1967; Yokouchi et al., 1973; Brückner et al., 1988) (рис.3.3).
Изолированные монокристаллы ПОБ имеют сетчатую структуру со следующими параметрами осей: короткая 0.3–2.0, длинная 5.10 мкм. Толщина одного кристалла составляет 4–10 нм в зависимости от молекулярного веса полимера, типа растворителя и температуры кристаллизации. Одиночные кристаллы ПОБ представляют собой моноламелярные системы, в отличие от них массивы ПОБ (пленки, диски и др.) являются мультиламелярными системами, которые аггрегируются в мультиориентированные ламелярные кристаллы. ПОБ в кристалле формируют сферолиты при кристаллиза-
107
ции из расплавов в твердофазное состояние (Barham et al., 1984). В сферолитах ламелярные кристаллы ПОБ растут радиально, располагаясь один над другим. Кристаллографически ось a располагается радиально b и c осям, которые вращаются вокруг нее. В результате скручивания ПОБ-ламелярных кристаллов сферолиты полиоксибутирата обычно формируют ленточную текстуру. Периодичность и регулярность ленточной текстуры ПОБ зависит от температуры кристаллизации, а также молекулярного веса полимера. Максимальный объем кристаллизации полимера происходит при 90 С, а скорость кристаллизации ПОБ максимальна при 50–60 С.
С использованием рентгеноструктурного анализа выявлено доминирование в полиоксибутирате кристаллической фазы над аморфной. Степень кристалличности различных образцов ПОБ мало зависит от условий получения и лежит в диапазоне 0.62–0.76 (Lee, 1996; Madison and Huisman, 1999).
Структура полиоксиалканоатов, синтезированных бактериями Ralstonia eutropha В-5786 и очищенных до гомогенного состояния, исследована рентгеноскопией и методами ЯМР и ЭПР высокого разрешения (Волова с соавт., 1992, 1994; Фалалеев с соавт., 1994; Петраковская с соавт., 1995; Волова с соавт., 2000).
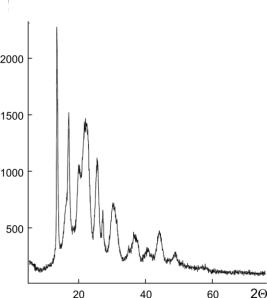
Рентгеноструктурный анализ и определение степени кристалличности образцов полимеров выполнены в Институте физики им. Л. В. Киренского СО РАН Васильевым А. Д. на рентгеноспектрометре D8 ADVANCE (Bruker) (графитовый монохроматор на отраженном пучке). Для определение степени кристалличности материала сняты спектры в пошаговом режиме (scan-step) с шагом 0.04 и 2-секундной выдержкой для измерения интенсивности в точке (режим работы прибора 40 кВ х 40 μА) На рис. 3.4 приведен типич-
Рис. 3.4. Рентгеновский спектр полиоксибутирата, синтезированого
Ralstonia eutropha B 5786;
степень кристалличности (Сх) 72 % (Volova et al., 2002).
108
ный спектр ПОБ. Рентгеноструктурный анализ различных образцов ПОБ свидетельствует о достаточно постоянных для данного материала значениях степени кристалличности (Хс). Разброс величин, полученных на серии из нескольких десятков образцов, лежит в диапазоне 0.66–78 %.
Молекулярная структура ПОБ исследована под руководством профессора Э. П. Зеера методом ЯМР высокого разрешения (Фалалеев с соавт. 1994; Петраковская с соавт., 1995). Полученные спектры ЯМР 13С (125 МГц) и 1Н (500 МГц) образцов ПОБ, синтезированного бактериями R. eutropha В5786 при использовании ими в качестве источника энергии водорода и углерода углекислоты совпали с высокой точностью с аналогичными спектрами, снятыми на образцах ПОБ, синтезированных R. eutropha Н16 при росте на фруктозе и
Bacillus megaterium KM – на глюкозе (Doi et al., 1986a, b).
3.1.3. Молекулярная структура и радиационная устойчивость ПОА
Полиоксибутират представляет собой изотактический полиэфир с регулярными, одинаково ориентированными (head-to-tail) последовательными единицами D-(-)-3- -оксимасляной кислоты:
[ O CH(CH3) CH2 C ]n.
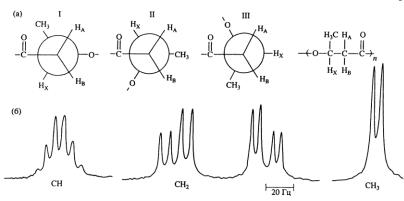
1Н (500 МГц) спектр раствора ПОБ в дейтерохлороформе при комнатной температуре (рис. 3.5б) иллюстрирует форму мультиплетов для СН-, СН2- и СН3-групп протонного спектра. Полученная форма линии для СН-группировки строго согласуется с теорией, согласно которой все приведенные на рис. 3.5б мультиплеты должны быть симметричными. Анализ констант-дипольного взаимодействия между протонами НА, НВ и НХ в магнитно-изолированном фрагменте, показанном на рисунке, позволил получить данные, усредненные по трем возможным конформациям, обозначенным через I, II и III (рис.3.5а), обусловленным поворотами вокруг связей Н3СНХС–СНАНВ. С учетом общепринятых теоретических значений для констант, характеризую-
Рис. 3.5. Три возможные изомерные конформации (I – транс; II
– гош; III – противоположная гош) (а) и прецизионная регистрация отдельных линий спектра 1Н (500 МГц) полиоксибутирата (б), синтезированого
Ralstonia eutropha B 5786 (Фалалеев с со-
авт., 1994).
109