Материал: Obmen_i_funktsii_aminokislot_Osnovy_molekulyarnoi_774_genetiki
42. Связь орнитинового цикла с циклом трикарбоновых кислот.
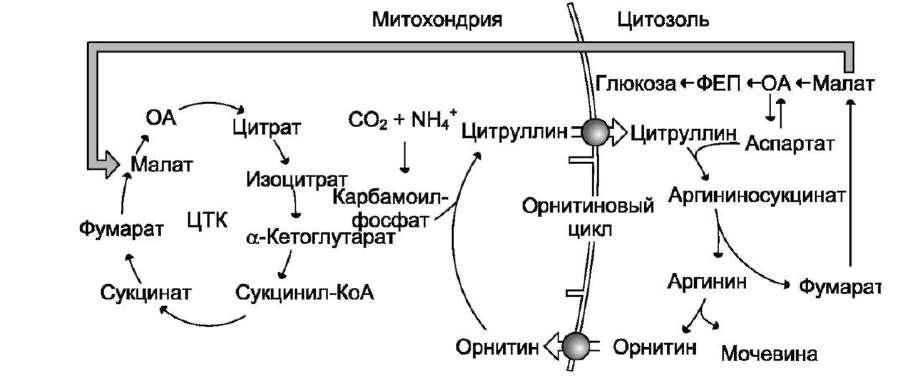
Фумарат, образующийся в результате расщепления аргининосукцината, превращается в малат, который затем переносится в митохондрии, включается в ЦТК и дегидрируется с образованием оксалоацетата. Эта реакция сопровождается выделением 3 молекул АТФ, которые и компенсируют затраты энергии на синтез одной молекулы мочевины.
43. Нарушение синтеза и выведения мочевины. Гипераммониемия, про-
исхождение.
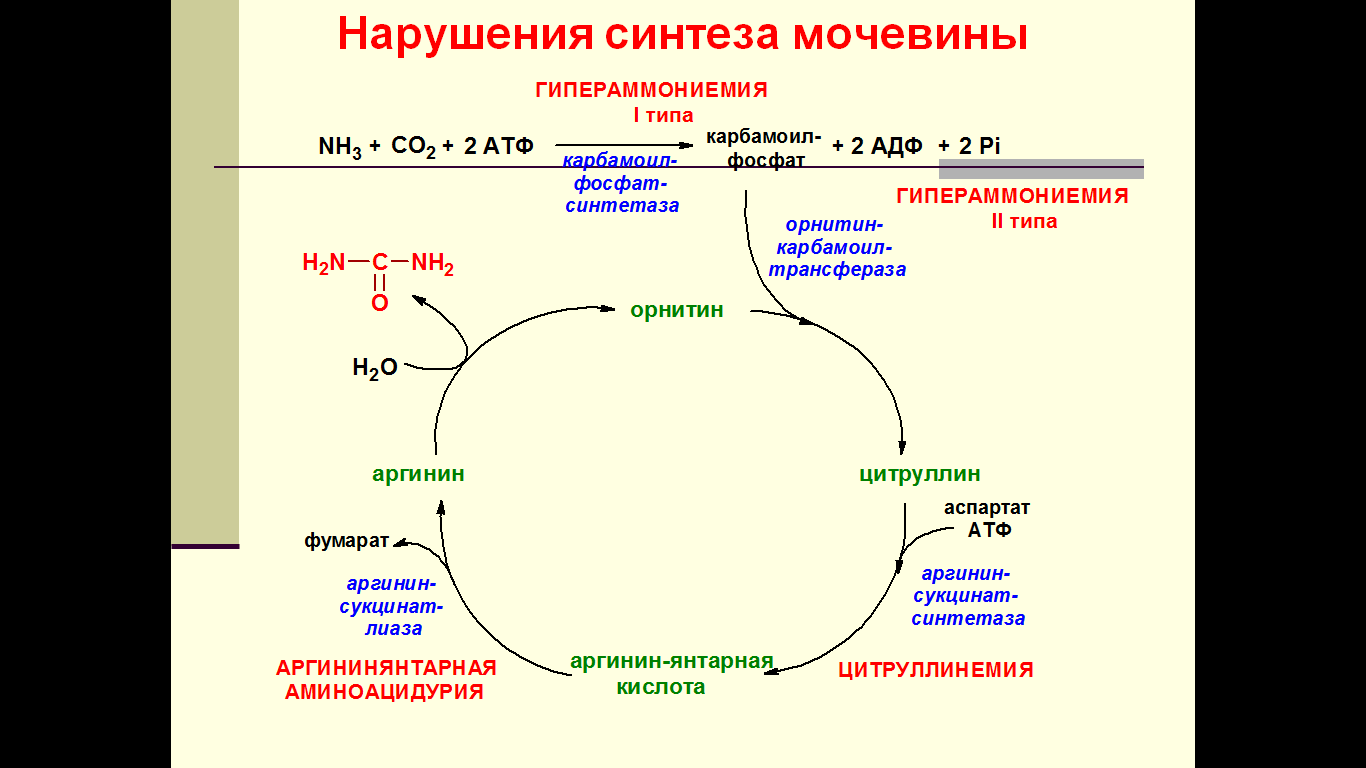
Нарушение реакций обезвреживания аммиака может вызвать повышение содержания аммиака в крови - гипераммониемию, что оказывает токсическое действие на организм. Причинами гипераммониемии могут выступать как генетический дефект ферментов орнитинового цикла в печени, так и вторичное поражение печени в результате цирроза, гепатита и других заболеваний. Известны пять наследственных заболеваний, обусловленных дефектом пяти ферментов орнитинового цикла
Нарушение орнитинового цикла наблюдается при гепатитах различной этиологии и некоторых других вирусных заболеваниях. Например, установлено, что вирусы гриппа и других острых респираторных вирусных инфекций снижают активность карбамоилфосфатсинтетазы I. При циррозе и других заболеваниях печени также часто наблюдают гипераммониемию.
Снижение активности какого-либо фермента синтеза мочевины приводит к накоплению в крови субстрата данного фермента и его предшественников.
Все симптомы гипераммониемии - проявление действия аммиака на ЦНС.
Для диагностики различных типов гиперам-мониемии производят определение содержания аммиака в крови, метаболитов орнитинового цикла в крови и моче, активности фермента в биоптатах печени.
Основной диагностический признак - повышение концентрации аммиака в крови. Содержание аммиака в крови может достигать 6000 мкмоль/л (в норме - 60 мкмоль/л).
Уремия (uraemia; греческий uron моча + haima кровь; синонимы мочекровие) — синдром аутоинтоксикации, развивающийся при выраженной почечной недостаточности в результате задержки в организме азотистых метаболитов и других токсических веществ, расстройства водно-солевого, кислотно-щелочного и осмотического гомеостаза, сопровождающийся вторичными обменными и гормональными нарушениями, общей дистрофией тканей и дисфункцией всех органов и систем. (Источник: Леди Википедия.)
44. Определение мочевины в сыворотке крови, принцип метода,
диагностическое значение.
Принцип метода основан на определении количества аммиака, высвобождаемющегося при разложении мочевины сыворотки или цельной крови под действием уреазы, колориметрическим методом с использование метода Несслера.
Диагностическое значение имеет повышение концентрации мочевины, которое встречается при хронических поражениях почек, усиленном распаде белков в тканях, непроходимости кишечника, закупорке мочевыводящих путей. Снижение уровня мочевины встречается при голодании, безбелковой диете, ферментных дефектах мочевинообразования.
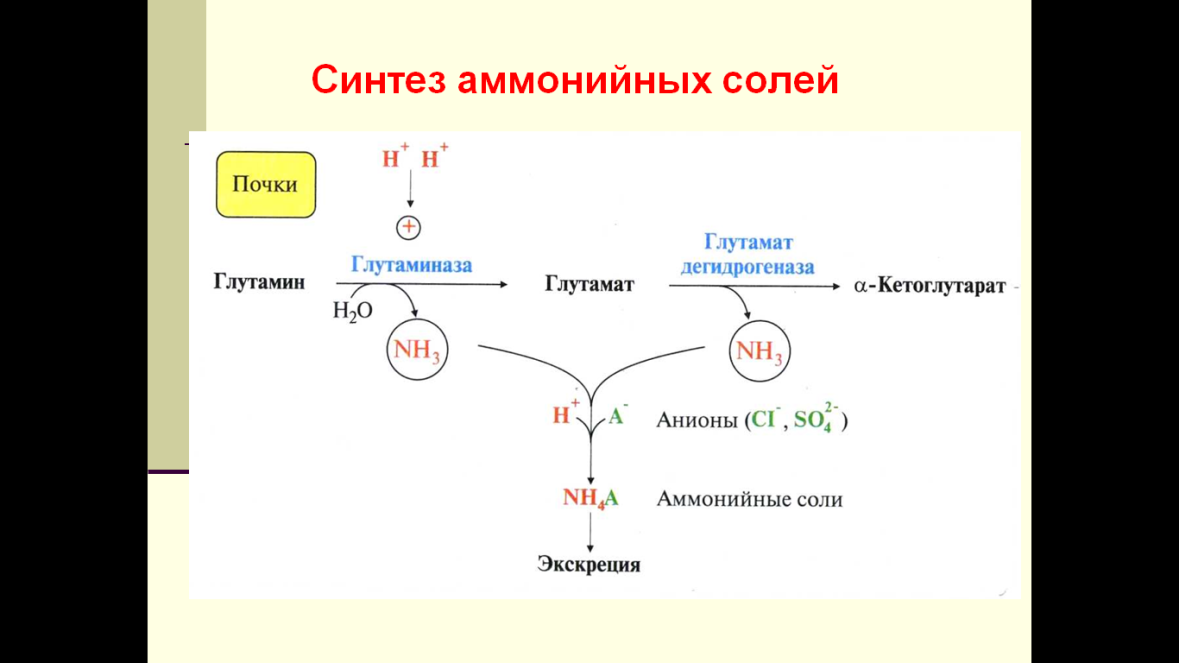
45. Образование и выведение солей аммония. Глутаминаза почек.
46. Распад нуклеиновых кислот, нуклеазы пищеварительного тракта и
тканей.
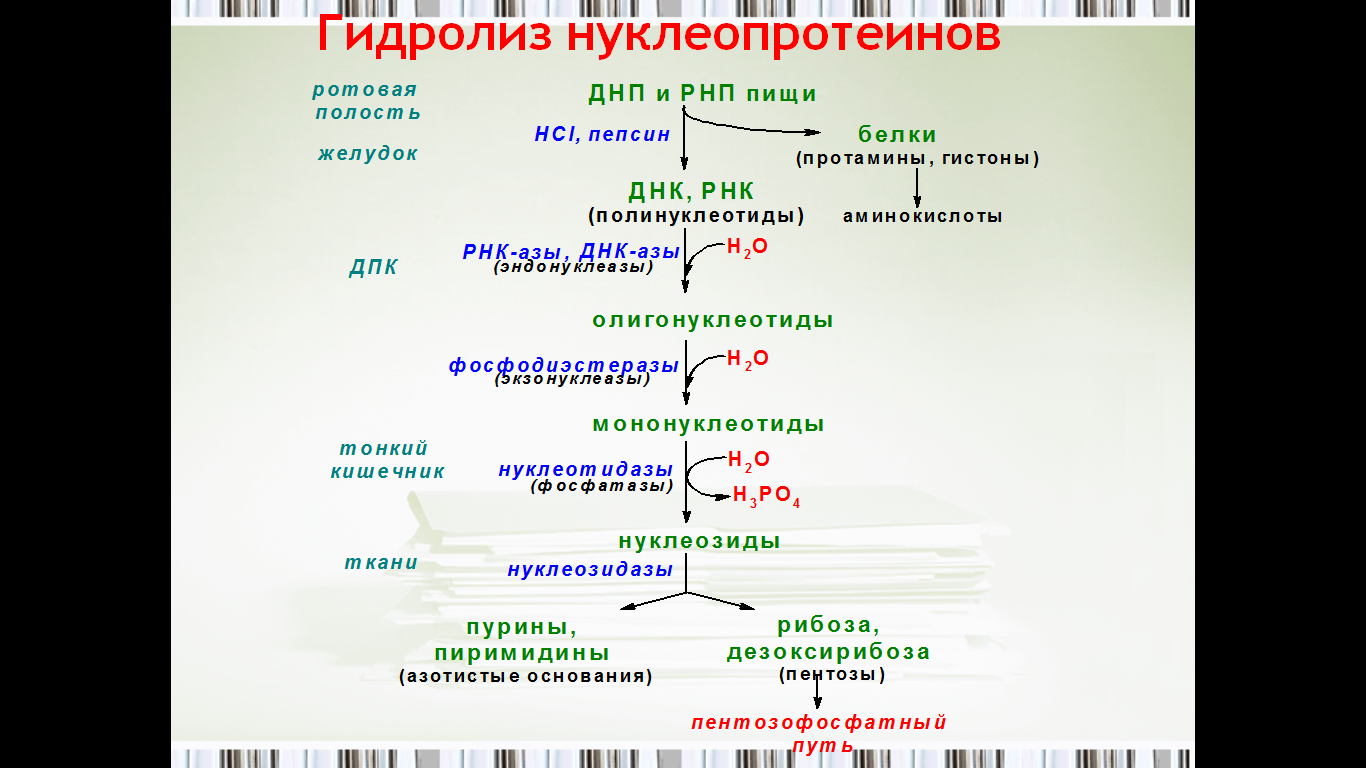
Схема говорит о многом. Съели курочку, её надо разобрать. ДНП и РНП чрез пищевод попадает в желудок, там, под действием агрессивных агентов - соляной кислоты и пепсинов расщепляются до полинуклеотидов. Дальше в ход вступают эндонуклеазы, образуются олигонуклеотиды и экзонуклеазы, ура, получили мононуклеотиды.
Продукт мигрирует тонкий кишечник, нуклеотидазы синтезируют нуклеозиды.
Парам-пам-пам, в тканях нуклеозидазы образуют строй материалы - азотистые основания и пентозы (а их могут пустить пентозофосфатный путь) Усё.
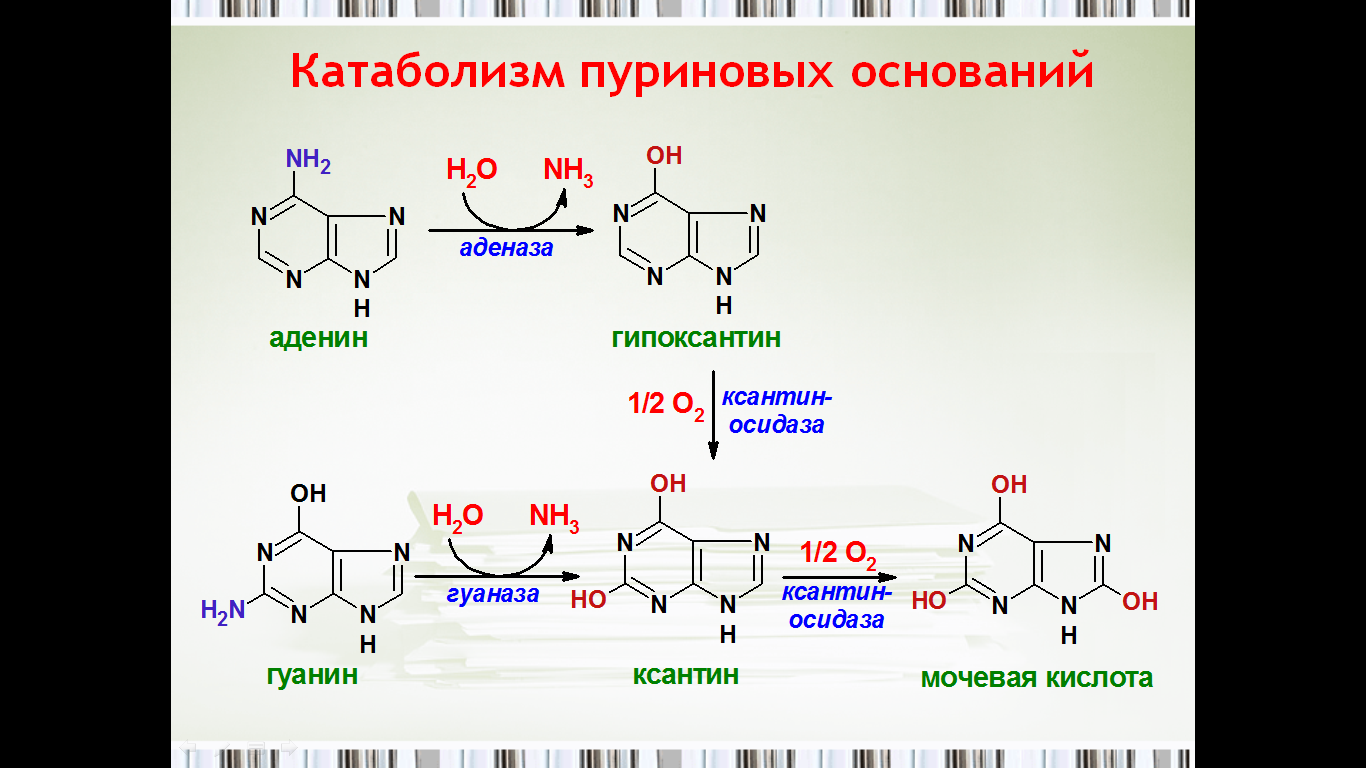
47. Распад пуриновых нуклеотидов.
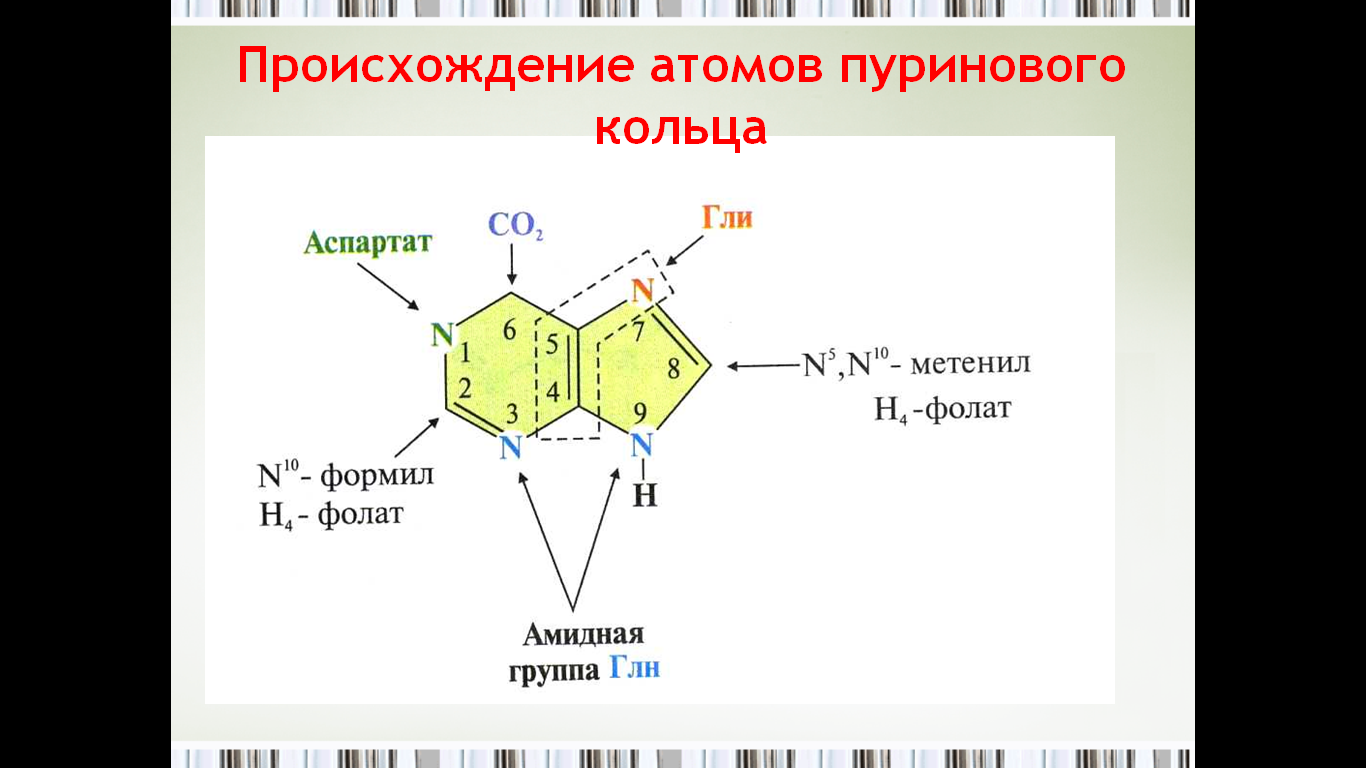
48. Биосинтез пуриновых нуклеотидов, происхождение атомов «с» и «n» в пуриновом кольце.
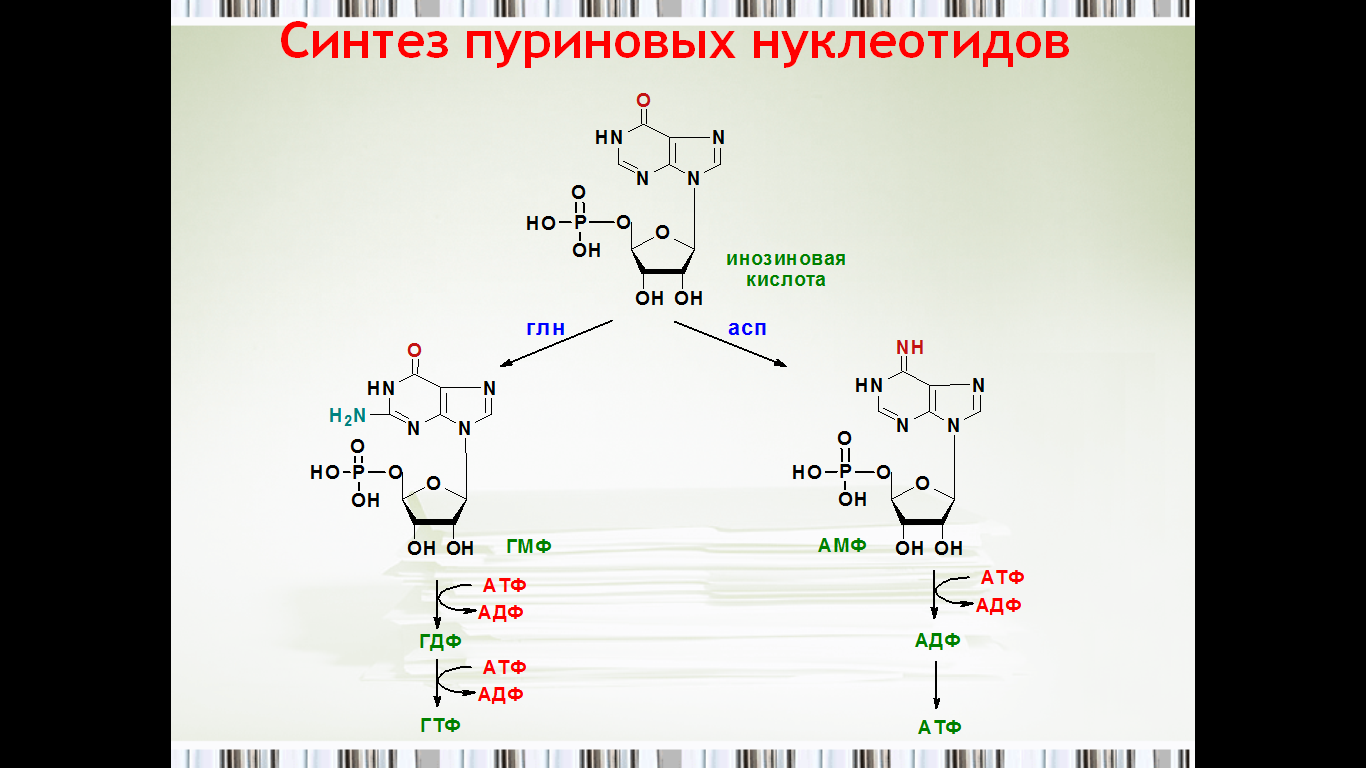
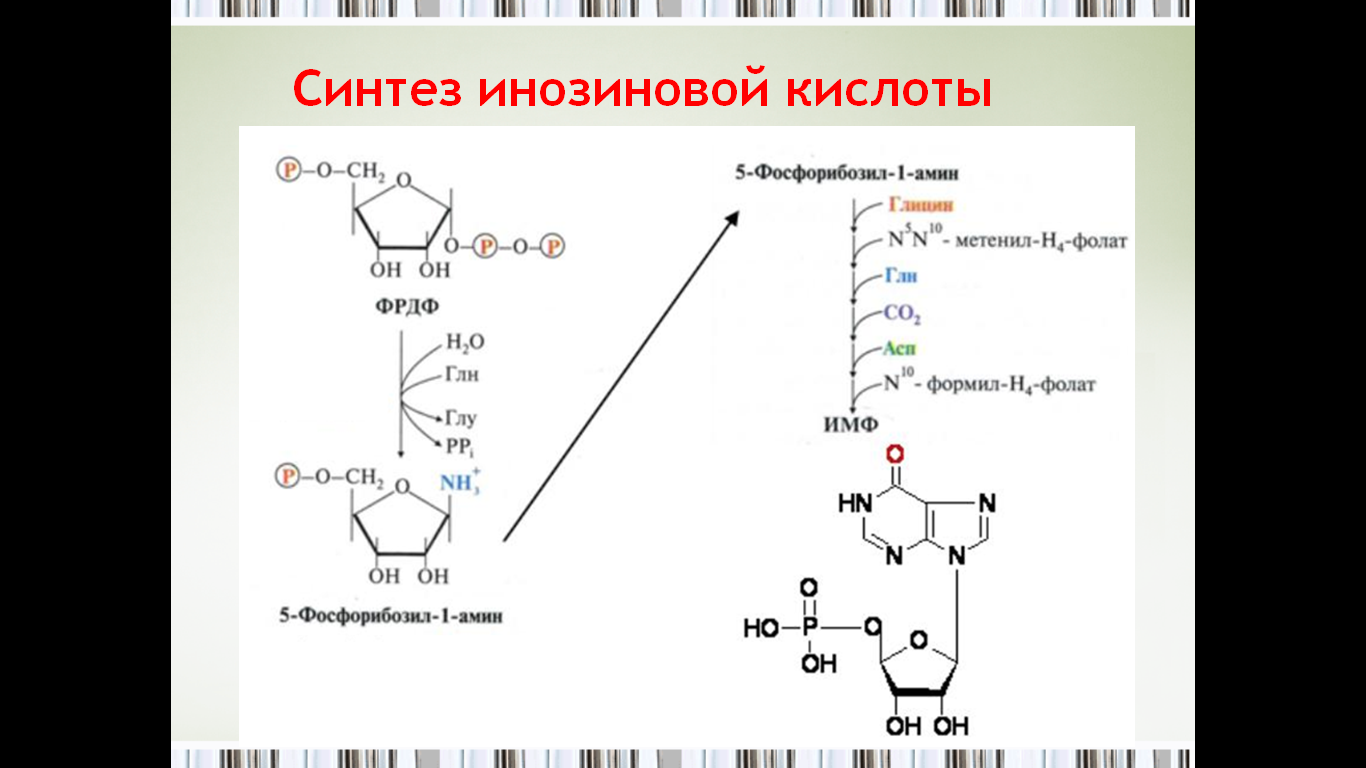
49. Инозиновая кислота как предшественник пуриновых мононуклеотидов.
Образование пуриновых нуклеотидов (адениловой и гуаниловой кислот, АМФ и ГМФ) осуществляется из инозиновой кислоты (ИМФ). Причем в синтезе обоих мононуклеотидов участвуют по два фермента, отличных по своему механизму действия. Образование ГМФ из ИМФ катализируют ИМФ-дегидрогеназа и ГМФ-синтетаза, а образование АМФ из того же предшественника катализируется последовательным действием аденилосукцинатсинтетазы и аденилосукцинатлиазы.
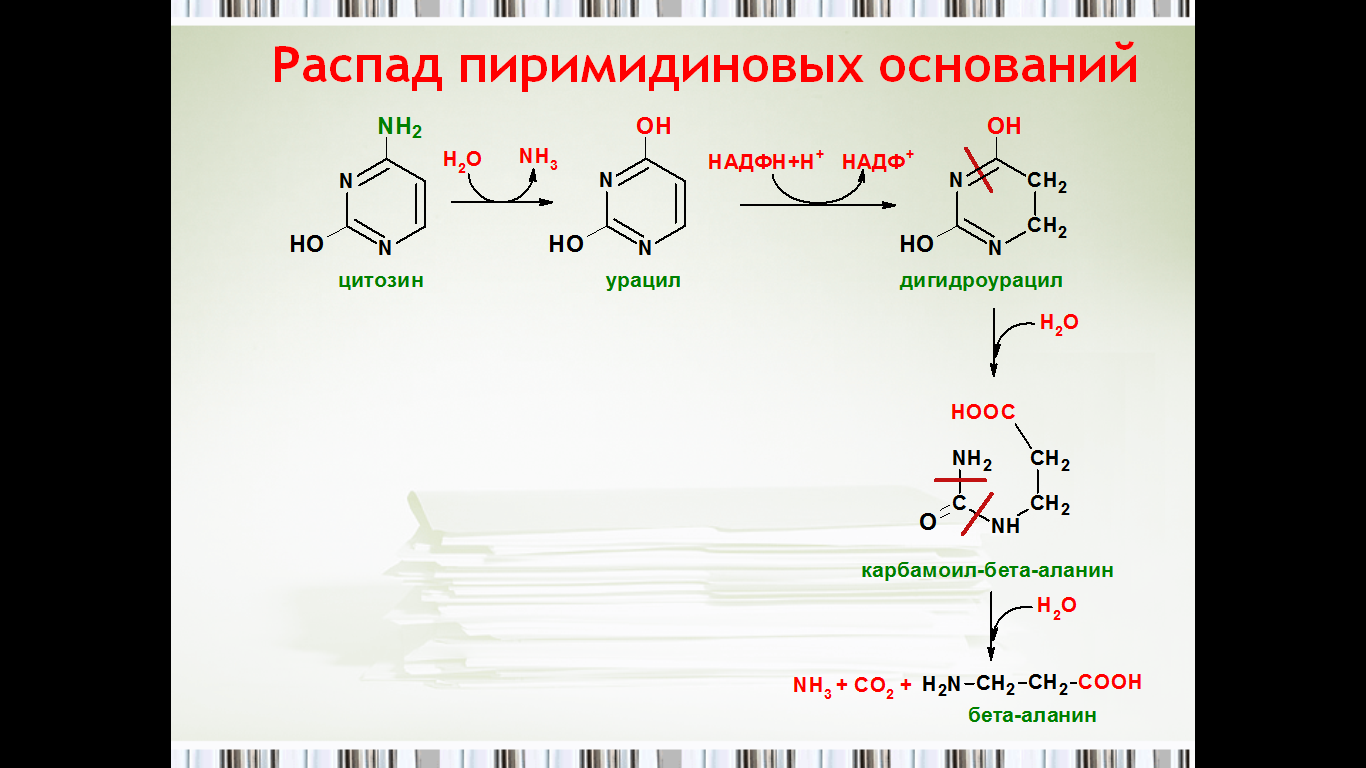
50. Распад пиримидиновых нуклеотидов.
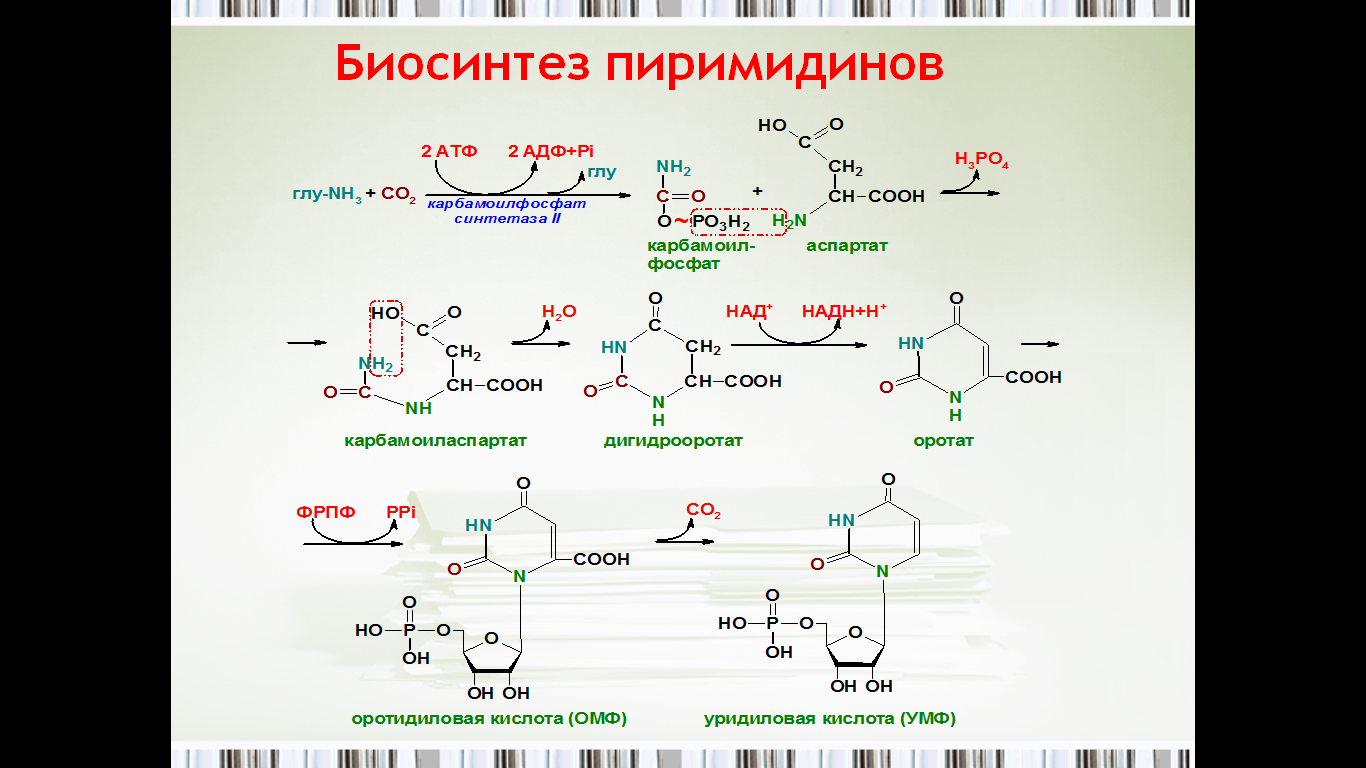
51. Биосинтез пиримидиновых нуклеотидов.
52. Регуляция биосинтеза пуриновых и пиримидиновых мононуклеотидов.
Регуляция синтеза пиримидиновых нуклеотидов
Регуляторным ферментом в синтезе пири-мидиновых нуклеотидов является полифункциональный КАД-фермент. УМФ и УТФ ал-лостерически ингибируют, а ФРДФ активирует его карбамоилсинтетазную активность, тогда как активность аспартаттранскарбамоилазного домена ингибирует ЦТФ, но активирует АТФ
Этот способ регуляции позволяет предотвратить избыточный синтез не только УМФ, но и всех других пиримидиновых нуклеотидов и обеспечить сбалансированное образование всех четырёх основных пуриновых и пиримидиновых нуклеотидов, необходимых для синтеза РНК.
Регуляция синтеза пуиновых нуклеотидов
Основным показателем, от которого зависит синтез пуриновых нуклеотидов, служит концентрация ФРДФ, которая, в свою очередь, зависит от скорости его синтеза, утилизации и разрушения. Количество ФРДФ определяется доступностью рибозо-5-фосфата и активностью ФРДФ синтетазы - фермента, чувствительного к концентрации фосфата и пуриновых нуклеотидов.
Внутриклеточная концентрация ФРДФ строго регулируется и обычно низкая. ФРДФ синтета-за - аллостерический фермент. Он активируется неорганическим фосфатом (Pi) и ингибируется пуриновыми нуклеозидмоно-, ди- и трифосфатами, которые по эффективности ингибирования распределяются в следующем порядке: НМФ > НДФ > НТФ. ФРДФ служит не только субстратом, но и аллостерическим активатором второй реакции синтеза пури-нонуклеотидов de novo, которую катализирует амидофосфорибозилтрансфераза.
Пуриновые нуклеотиды, особенно АМФ и ГМФ по механизму отрицательной обратной связи ингибируют амидофосфорибозилтрансфе-разу, которая катализирует первую специфическую реакцию синтеза пуриновых нуклеотидов de novo.
53. Биосинтез дезоксирибонуклеотидов.
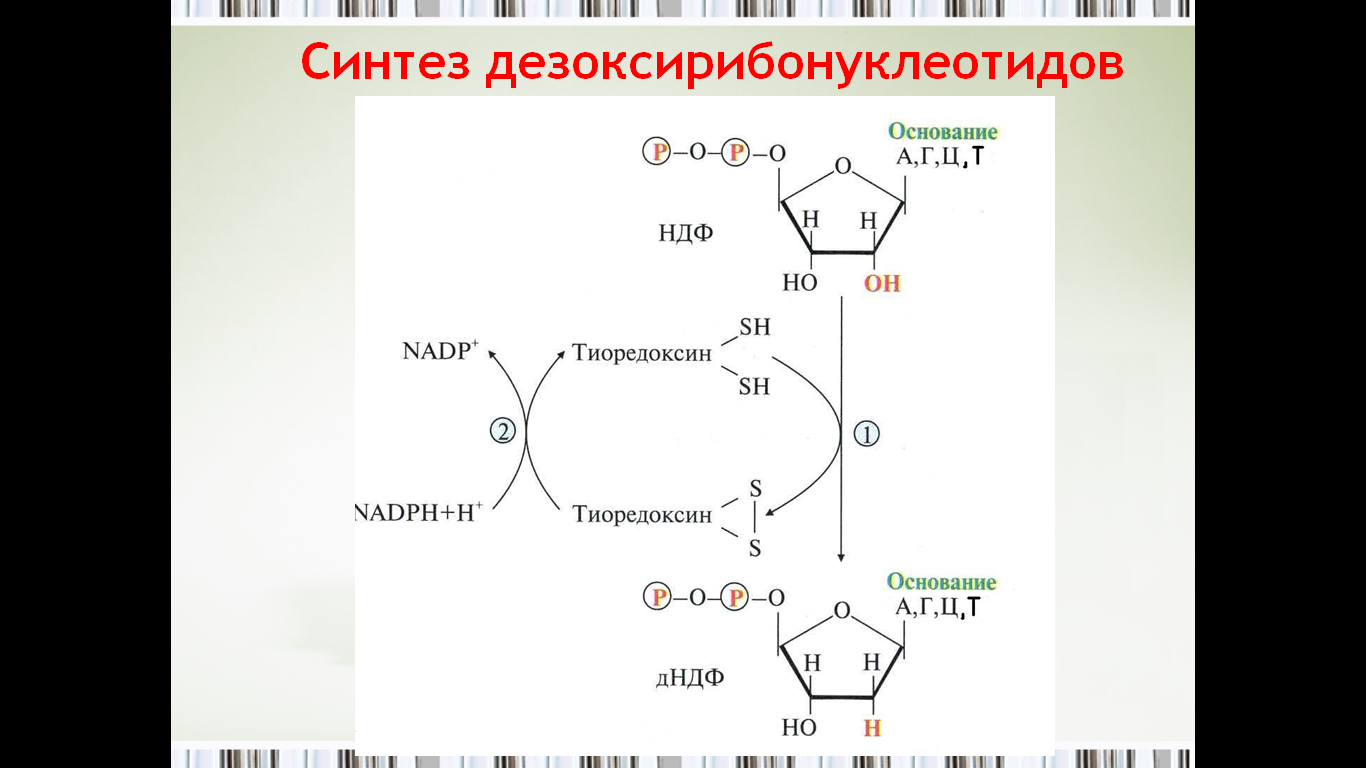
Синтез дезоксирибонуклеотидов идёт с заметной скоростью только в тех клетках, которые вступают в S-фазу клеточного цикла и готовятся к синтезу ДНК и делению. В покоящихся клетках дезоксинуклеотиды практически отсутствуют. Все дезоксинуклеотиды, кроме тимидиловых, образуются из рибонуклеотидов путём прямого восстановления ОН-группы у второго углеродного атома рибозы в составе рибонуклеозидди-фосфатов до дезоксирибозы.
Реакцию восстановления НДФ в дезокси-про-изводные катализирует рибонуклеотидредуктаз-ный комплекс, в состав которого входят: собственно рибонуклеотидредуктаза (РНР), белок тиоредоксин и фермент тиоредоксинредуктаза, обеспечивающий регенерацию восстановленной формы тиоредоксина Рибонуклеотидредуктаза - олигомерный белок, состоящий из двух В1- и двух В2-субъеди-ниц, и содержит негеминовое железо в качестве кофактора.
Непосредственным донором водорода в реакции восстановления рибозы служит низкомолекулярный белок тиоредоксин. В рабочую часть этого белка входят 2 SH-группы, которые, отдавая водород, окисляются с образованием дисульфидного мостика. Второй фермент комплекса - тиоредоксинредуктаза - катализирует гидрирование окисленного тиоредоксина с использованием NADPH.
54. Применение ингибиторов синтеза дезоксирибонуклеотидов для лечения злокачественных опухолей.
В терапии инфекционных и онкологических болезней, научных исследованиях в области медицины и биологии часто используют синтетические аналоги пуринов и пиримидинов. Введение в организм животного или человека аналога, имеющего изменения в структуре гетероциклического кольца или углеводной компоненты, угнетает активность ферментов, участвующих в метаболизме нуклеотидов, скорость синтеза РНК или ДНК из-за нарушения комплементарных взаимодействий азотистых оснований и роста полинуклеотидных цепей. Аналоги пуринов, пиримидинов и их нуклео-зиды нашли применение в качестве антибактериальных, противовирусных и химиотерапевти-ческих средств.
Синтезировано очень много аналогов дНТФ, которые включаются ДНК полимеразами в ДНК и ингибируют репликацию. К числу мощных противоопухолевых препаратов принадлежит 5-фторурацил (5-FU) - аналог урацила.
Цитозинарабинозид (или цитарабин) представляет собой соединение, в котором остаток рибозы замещён на стериоизомер - арабинозу. Оно используется в химиотерапии рака, в частности, при острой миелоцитарной лейкемии.
В организме препарат может превращаться в дНТФ, ингибировать ДНК полимеразы и снижать скорость репликации.
Аналоги фолиевой кислоты. В обмене нуклеотидов производные Н4-фолата как доноры одно-углеродных групп участвуют в формировании пуринового гетероциклического кольца и в ключевой реакции синтеза дТМФ из дУМФ, катализируемой тимидилатсинтазой.
В последнем случае N5, N10-метилен-Н4-фолат служит донором метильной группы и в ходе реакции превращается в Н2-фолат. Для активного синтеза тимидиловых нуклеотидов Н2-фолат должен повторно использоваться, проходя стадию восстановления в Н4-фолат.
55. Нарушения обмена нуклеотидов: оротацидурия, ксантинурия.
ОРОТАЦИДУРИЯ
Это единственное нарушение синтеза пирими-динов de novo. Оно вызвано снижением активности УМФ-синтазы, которая катализирует образование и декарбоксилирование ОМФ. Поскольку в эмбриогенезе от образования пиримидинов de novo зависит обеспечение синтеза ДНК субстратами, то жизнь плода невозможна при полном отсутствии активности этого фермента. Действительно, у всех пациентов с оротацидурией отмечают заметную, хотя и очень низкую активность УМФ-синтазы. Установлено, что содержание оротовой кислоты в моче пациентов (1 г/сут и более) значительно превосходит количество оротата, которое ежедневно синтезируется в норме (около 600 мг/сут). Снижение синтеза пирими-диновых нуклеотидов, наблюдающееся при этой патологии, нарушает регуляцию КАД-фермента по механизму ретроингибирования, из-за чего возникает гиперпродукция оротата.
Клинически наиболее характерное следствие оротацидурии - мегалобластная анемия, вызванная неспособностью организма обеспечить нормальную скорость деления клеток эритро-цитарного ряда. Её диагностируют у детей на том основании, что она не поддаётся лечению препаратами фолиевой кислоты
Недостаточность синтеза пиримидиновых нуклеотидов сказывается на интеллектуальном развитии, двигательной способности и сопровождается нарушениями работы сердца и ЖКТ. Нарушается формирование иммунной системы, и наблюдается повышенная чувствительность к различным инфекциям.
Ксантинурия(xanthinuria; ксантин +греч. uron моча) -- наследственная болезнь, обусловленная недостаточностью фермента ксантиноксидазы и характеризующаяся нарушением пуринового обмена; проявляется рецидивирующей гематурией и болями в поясничной области, повышением содержания ксантина в плазме крови и моче.
Симптомы Ксантинурии:
Ксантин является непосредственным предшественником мочевой кислоты. Он образуется из некоторых пуринов, в то время как гипоксантин относится к промежуточным продуктам. Окисление гппоксантипа в ксантин, а последнего в мочевую кислоту опосредуется ксантиноксидазой, выявленной в печени и слизистой оболочке кишечника.
Ксантинурия встречается редко.Уровень мочевой кислоты в сыворотке больных (1 - 8 мг/л) обычными методами не выявляется. Низкий уровень гипоксантина отмечается как в крови, так и в моче. При потреблении продуктов, не содержащих пуринов, мочевая кислота прекращает экстретироваться. Ксантин даже менее растворим в моче, чем мочевая кислота; соответственно у некоторых больных с ксантинурией образуются мочевые камни, состоящие из чистого ксантина.
56. Подагра, причины возникновения. Применение аллопуринола для
лечения подагры.
Слишком просто не бывает, и бывают нарушения ходе их существования.
Гиперурикемия - увеличение концентрации мочевой кислоты в крови. И вследствие может развиться подагра - заболевание, при котором кристаллы мочевой кислоты и уратов откадываются в суставных хрящах, синовиальной оболочке, подкожной клетчатке, с образование подагрических узлов, или тофусов.
Сопровождается повторением приступов острого воспаления суставов -острого подагрического артрита.
Но это еще не всё! Лейкоциты устраивают НОМ-НОМ-НОМ кристаллам урата. Те, в свою очередь, способны разрушать мембраны лизосом. Лизосомальные ферменты, подобно динозаврам "Мира Юрского Периода", выбираются в цитозоль и начинают РАЗРУШЕНИЕ КЛЕТКИ, а продукты клеточного катаболизма вызывает воспаление.
ФРДФ синтетаза - фермент-стахановец, который смутно понимает, что все должно быть в меру. И поэтому он синтезирует мочевую кислоту в ОГРОМНЫХ количествах, не смотря на потребности клетки. И возникает подагра.
Гипоксантин-гуганинфосфорибозилтрансфераза, фермент-инвалид, а вот это звено не справляется со своей работы и происходит накопление мочевой кислоты в клетке, что также вызывает подагру.