Материал: Obmen_i_funktsii_aminokislot_Osnovy_molekulyarnoi_774_genetiki
11.Всасывание аминокислот, поступление аминокислот в клетки тканей.
Аминокислоты, образовавшиеся при переваривании белков, быстро всасываются в кишечнике. Транспорт их осуществляется двумя путями: через воротную систему печени, ведущую прямо в печень, и по лимфатическим сосудам, сообщающимся с кровью через грудной лимфатический проток. Максимальная концентрация аминокислот в крови достигается через 30- 50 мин после приёма белковой пищи (углеводы и жиры замедляют всасывание аминокислот). Всасывание L-аминокислот (но не D-изомеров) - активный процесс, требующий затраты энергии. Аминокислоты переносятся через кишечную стенку от слизистой её поверхности в кровь. Перенос через щёточную кайму осуществляется целым рядом переносчиков, многие из которых действуют при участии Na+-зависимых механизмов симпорта, подобно переносу глюкозы.
В настоящее время известно по крайней мере пять специфических транспортных систем, каждая из которых функционирует для переноса определённой группы близких по строению аминокислот:
• нейтральных, с короткой боковой цепью (аланин, серин, треонин);
• нейтральных, с длинной или разветвлённой боковой цепью (валин, лейцин, изолей-цин);
• с катионными радикалами (лизин, аргинин);
• с анионными радикалами (глутаминовая и аспарагиновая кислоты);
• иминокислот (пролин, оксипролин). Причём к числу Na+-зависимых относятся
переносчики аминокислот, входящих в первую и пятую группы, а также переносчик метионина. Независимые от Na+ переносчики специфичны для некоторых нейтральных аминокислот (фенилаланин, лейцин) и аминокислот с катион-ными радикалами (лизин).
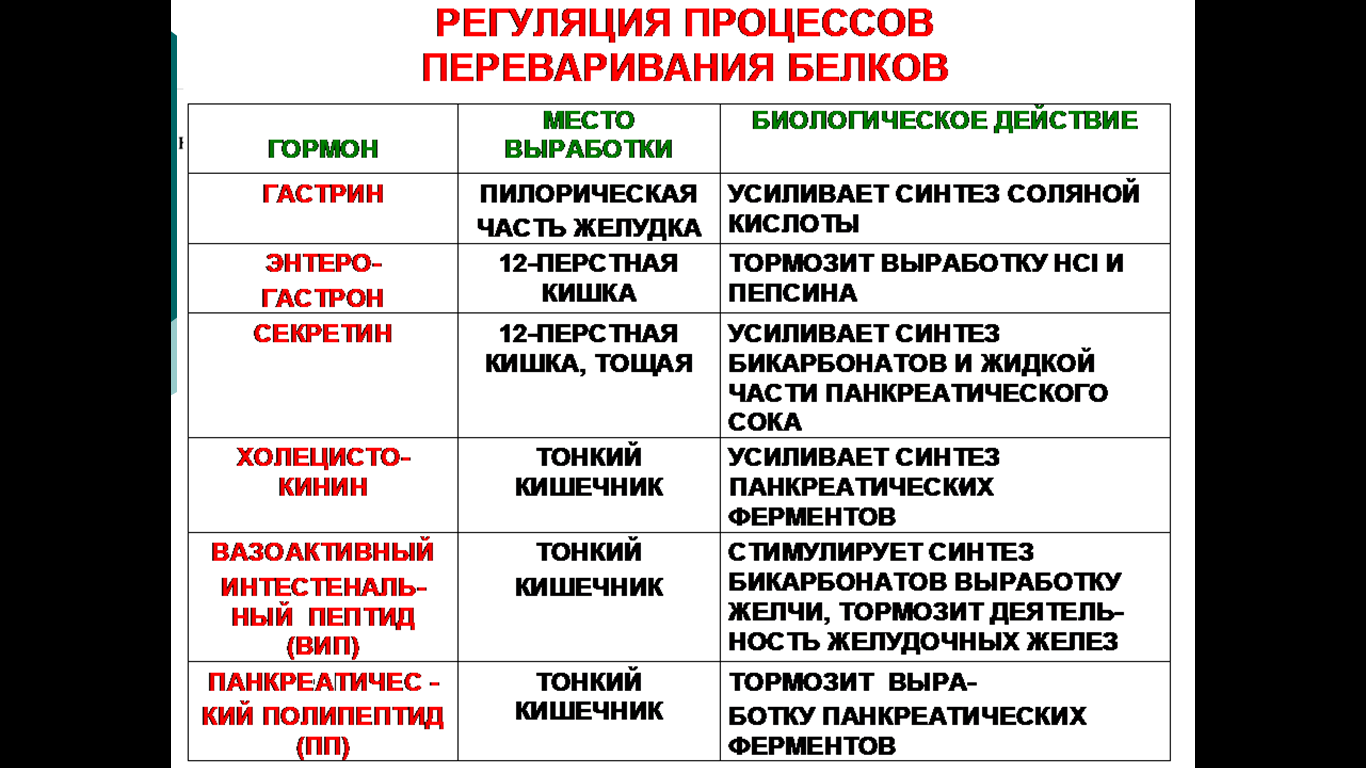
12. Биохимические механизмы регуляции пищеварения, гормоны
желудочно-кишечного тракта.
Выбирайте тот тип гормонов, который вам нравится больше всего и поведайте о нем на итоговой!
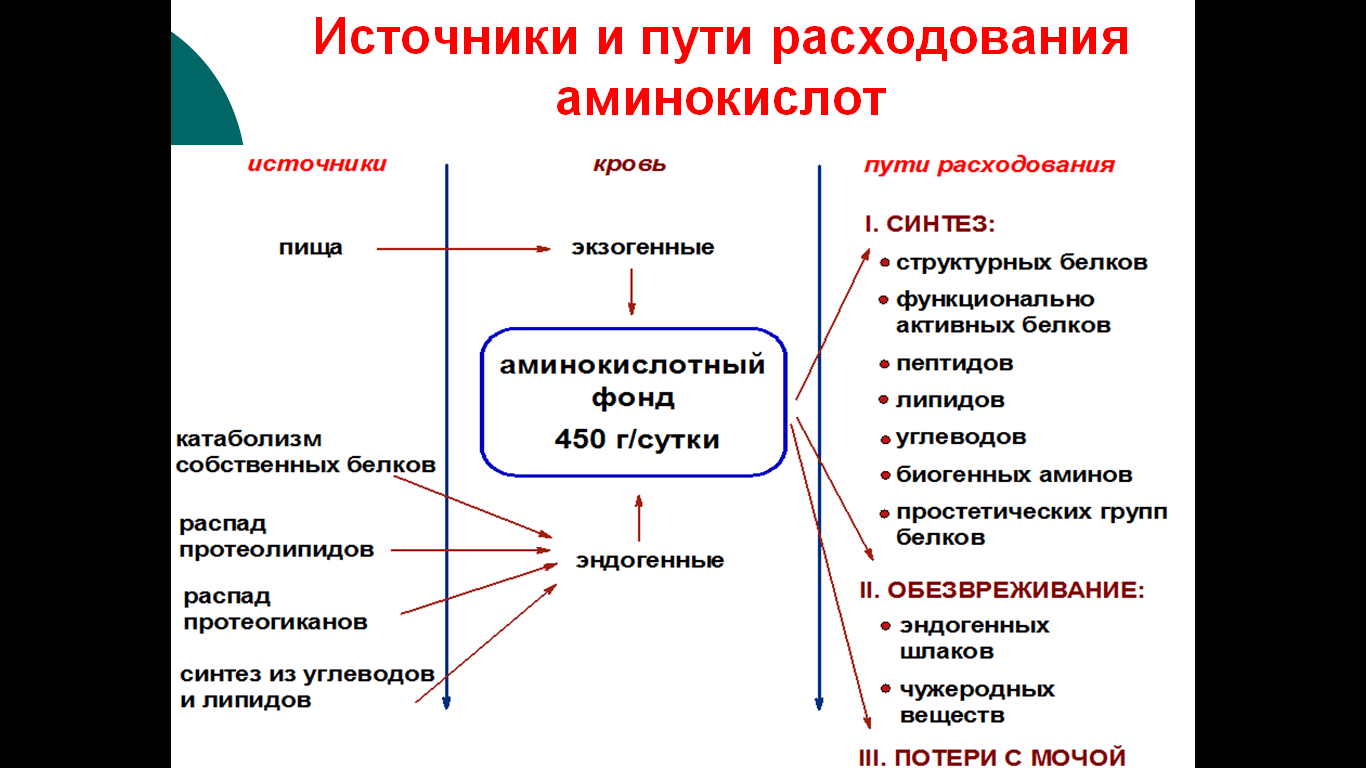
13. Общая схема источников и путей расходования аминокислот в тканях.
14. Трансаминирование аминокислот, химизм, ферменты. Аминокислоты,
участвующие в трансаминировании.
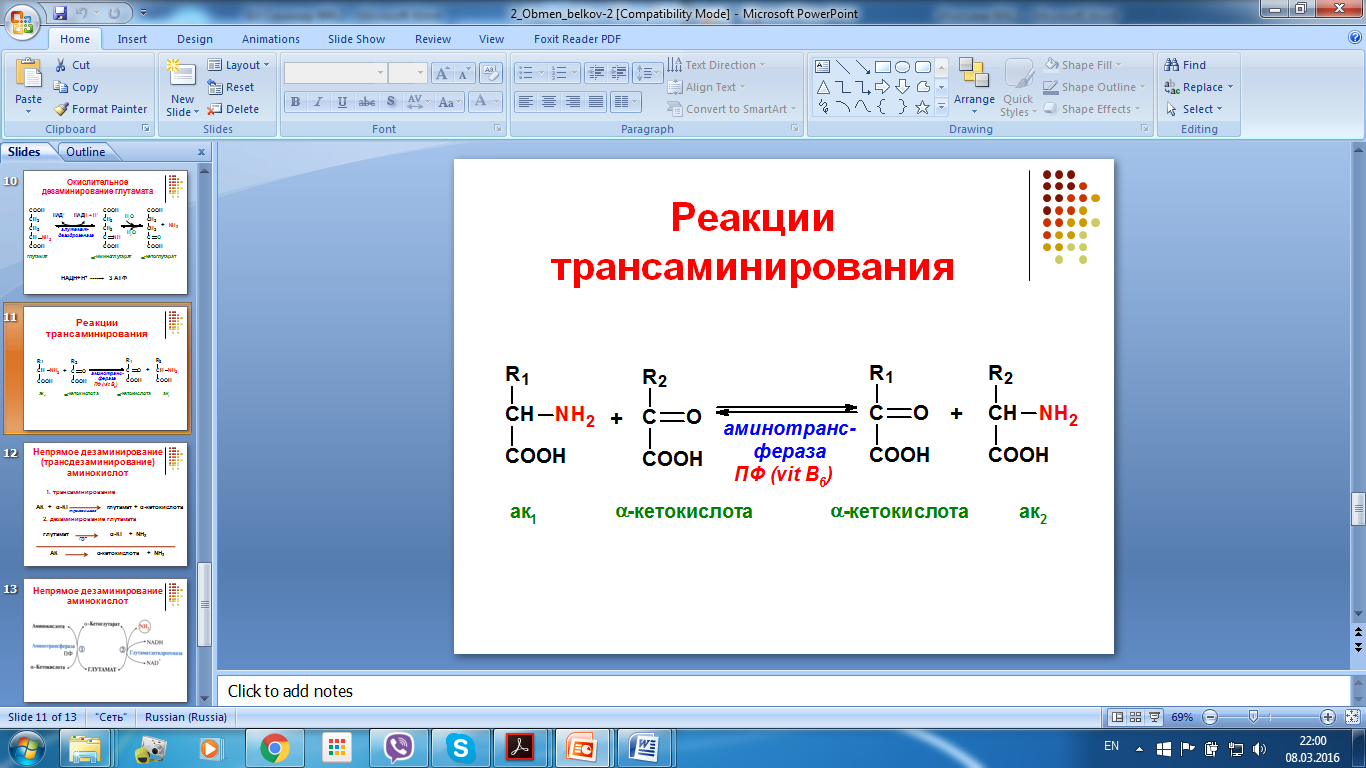
Трансаминирование есть подразумевают реакции межмолекулярного переноса аминогруппы от аминокислоты на альфа-кетокислоту без промежуточного образования аммиака.
Реакция трансаминирования являются обратимыми и универсальными для всех жиых организмо. Эти реакции протекают при участии специфических ферментов, аминотрансферазы или трансаминазы.
Аминотрансферазы обладают субстратной специфичностью к разным аминокислотам. В тканях человека более 10 разных аминотрансфераз.
Топовые ферменты.
- аланиаминотрансфераза (АЛТ);
- глутамат-пируватаминотрансфераза (ГПТ);
- аспартатаминотрансфераза (АСТ);
- по обратной реакции глутама-оксалоацетатаминотрансфераза (ГОТ).
В переносе аминогруппы активное участие принимает кофермент трансаминаз пиридоксальфосфат, производное витамина В6, который процессе реакции обратимо превращается в пиридоксаминфосфат.
Трансамиеировании могут подвергаться все аминокислоты, кроме трех: пролин, треонин, лизин
15. Специфичность трансаминаз, коферментная функция витамина в6.
Специфичность субстрата- абсолтная, в одну сторону
|
Специфичность трансаминаз обеспечивается белковым компонентом. Ферменты трансаминирования катализируют перенос NH2-группы не на а-кетокислоту, а сначала на кофермент — пиридоксальфосфат; образовавшееся промежуточное соединение (шиффово основание) подвергается внутримолекулярным превращениям (лабилизация ос-водородного атома, перераспределение энергии связи), приводящим к освобождению а-кетокислоты и пиридоксаминфосфата; последний на второй стадии реакции реагирует с любой другой альфа-кетокислотой, что через те же стадии образования промежуточных соединений (идущих в обратном направлении) приводит к синтезу новой аминокислоты и освобождению пиридоксальфосфата. Витамин БЭ-ШЕСТЬ!!! Пиридоксальфосфат (АКТИВНАЯ ФОРМА) служит переносчиком аминогрупп. При этом наиболее важную роль играет его альдегидная группа, которая может обратимо присоединять различные амины с образованием шиффовых оснований. Реакции трансаминирования проходят в 2 стадии, во время которых пиридоксальфосфат претерпевает обратимые превращения между свободной альдегидной формой (ПФ) и ами-нированной формой (пиридоксаминфосфат).
|
16. Особая роль глутамата в реакциях трансаминирования.
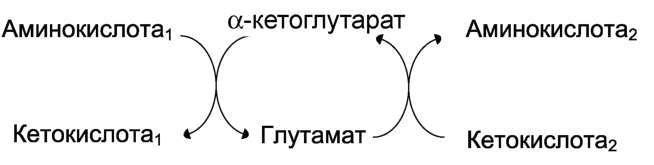
Чаще всего в реакциях трансаминирования участвуют аминокислоты, содержание которых в тканях значительно выше остальных - глу-тамат, аланин, аспартат и соответствующие им кетокислоты - α-кетоглутарат, пируват и оксалоацетат. Основным донором аминогруппы служит глутамат.
Акцептором аминогруппы любой аминокислоты, подвергающейся трансаминированию (аминокислота 1), служит α-кетоглутарат. Принимая аминогруппу, он превращается в глутамат, который способен передавать эту группу любой α-кетокислоте с образованием другой аминокислоты (аминокислота 2).
17. Биологическое значение реакций трансаминирования.
Реакции трансаминирования играют большую роль в обмене аминокислот. Поскольку этот процесс обратим, ферменты аминотрансферазы функционируют как в процессах катаболизма, так и биосинтеза аминокислот. Трансаминирование - заключительный этап синтеза заменимых аминокислот из соответствующих α-кетокислот, если они в данный момент необходимы клеткам. В результате происходит перераспределение аминного азота в тканях организма. Трансаминирование - первая стадия дезаминирования большинства аминокислот, т.е. начальный этап их катаболизма. Образующиеся при этом кетокислоты окисляются в ЦТК или используются для синтеза глюкозы и кетоновых тел. При трансаминировании общее количество аминокислот в клетке не меняется.
При трансамиеировании происходит образование новой альфакетокислоты и новой аминокислоты без промежуточного образования аммиака
18. Определение трансаминаз в сыворотке крови, принцип, диагностическое значение.
Ладно, это есть в методичке, но краткий пересказ предыдущих эпизодов.
Аминотрансферазы - ферменты, катализирующие межмолекулярный перенос аминогруппы с аминокислоты на кетокислоту. Наибольшее значение имеет определение активности 2-х ферментов: аспартатаминотрансферазы (АсАТ) и аланинаминотрансферазы (АлАТ). Их много, они везде.
Всего капитально два метода:
1. С использованием стандартных реактивов. В результате реакции пировиноградной кислоты получается... субстанция коричневого-фиолетового цвета.
2. Унифицированный метод.
- Определение активности аспартатаминотрансферазы.
Основан на определении скорости образования НАД за счет окисления НАД+Н. В результате реакции уменьшается оптическая плотность растора.
- Определение активности аспартатаминотрансферазы.
Основан на определении скорости образования НАД за счет окисления НАД+Н. В результате реакции уменьшается оптическая плотность растора.
Диагностическое значение:
Определение активности АсАТ и АлАТ широко используется для диагностики болезней печени и заболеваний сердца.
Актиность АлАТ увеличивается при обострении хронического гепатита, при токсическом поражение сердца.
Активность АсАТ возрастанет при гипертонических кризах, инфарктах.
19. Окислительное дезаминирование аминокислот, химизм, ферменты,
биологическое значение.
Наиболее активно происходит дезаминироание глутаминовой кислоты, процесс катализирует фермент глутаматдегидрогеназа, ну а верный ассистент - кофермент это НАД+.
Реакции идет в 2 этапа.
1. Вначале происходит ферментативное дегидрирование глутамата и образование альфа-иминоглутарата.
2. Неферментативное гидролитическое отщепление иминогруппы в виде аммиака, в результате чего образуется альфа-кетоглутарат.
Глутаматдегидрогеназа очень активна в митохондриях клеток практически всех органов, кроме мышц. Этот фермент- олигомер из 6 субъединиц. Играет важную роль, т.к. является регуяторным ферментом аминокислотного обмена.
Ингибиторы - АТФ, ГТФ и НАДН.
Активаторы - высокая концентрация АДФ.
Биологическая роль - регуляторным ферментом аминокислотного обмена.
20. Окислительное дезаминирование глутаминовой кислоты.
Глутаматдегидрогеназа.
ЭТО ЕСТЬ обратимая реакция и при повышении концентрации аммиака в клетке может протекать в обратном направлении, как восстановительное аминирование α-кетоглутарата.
Глутаматдегидрогеназа очень активна в митохондриях клеток практически всех органов, кроме мышц. Этот фермент - олигомер, состоящий из 6 субъединиц. Глутаматдегидрогеназа играет важную роль, так как является регуляторным ферментом аминокислотного обмена. Аллостерические ингибиторы глутаматдегидрогеназы (АТФ, ГТФ, NADH) вызывают диссоциацию фермента и потерю глутаматдегидрогеназной активности. Высокие концентрации АДФ активируют фермент. Таким образом, низкий энергетический уровень в клетках стимулирует разрушение аминокислот и образование α-кетоглутарата, поступающего в ЦТК как энергетический субстрат. Синтез глутаматдегидрогеназы может индуцироваться стероидными гормонами (кортизолом).
21. Непрямое дезаминирование, транс-дезаминирование, химизм, био-
логическая роль.
Большинство аминокислот не способно де-заминироваться в одну стадию, подобно Глу. Аминогруппы таких аминокислот в результате трансаминирования переносятся на α-кетоглу-тарат с образованием глутаминовой кислоты, которая затем подвергается прямому окислительному дезаминированию. Такой механизм дезаминирования аминокислот в 2 стадии получил название трансдезаминирования, или непрямого дезаминирования.
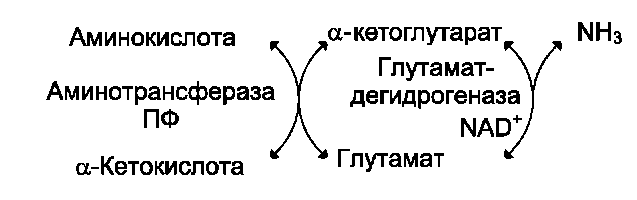
Непрямое дезаминирование аминокислот происходит при участии 2 ферментов: амино-трансферазы (кофермент ПФ) и глутаматдегид-рогеназы (кофермент NAD+).
Значение этих реакций в обмене аминокислот очень велико, так как непрямое деза-минирование - основной способ дезаминирования большинства аминокислот. Обе стадии непрямого дезаминирования обратимы , что обеспечивает как катаболизм аминокислот, так и возможность образования практически любой аминокислоты из соответствующей α-кетокислоты.
22. Декарбоксилирование аминокислот.
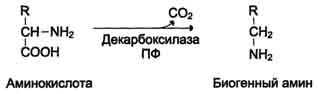
Декарбоксилирование - процесс отщепления карбоксильной группы аминокислот в виде СО2. Зачем нам это надо? В результате этих процессов в животных тканях образуются биогенные амины.
Реакции декарбоксилирования необратимы катализируются ферментами декарбоксилаза. Их простетическая группа - пиридоксальфосфат.
Механизм реакции напоминают РЕАКЦИЮ трансаминирования с участием пиридоксальфостфат и также осущестляется путем образования шиффова основания ПФ и аминокислоты.
23. Биогенные амины, происхождение, функции.
Что такое биогенные амины? Это амины, образовавшиевся при декарбоксилировании аминокислот! Они играют ряд физиологически ролей:
- нейромедиаторы (серотонин, дофамин, ГАМК и др.);
- гормоны (норадреналин, адреналин);
- регуляторные факторы местного действия (гистамин, карнозин, спермин и др.);
Накопление биогенных амино может сказаться паршивым образом на физиологическом статусе и вызывать нарушения функций в организме. Затим, есть ряд механизмов по их обезвреживанию, и усё сводится к окислительному дезаминированию этих аминов с образование соответствующих альдегидов и освобождению аммиака.
Ферменты, катализирующие эту реакцию называются моноамин- и диаминоксидазы.
И сноаа, две стадии:
- анаэробная стадия, характеризуется образованием альдегида, аммиака и восстановленного фермента.