Материал: Obmen_i_funktsii_aminokislot_Osnovy_molekulyarnoi_774_genetiki
31. Тетрагидрофолиевая кислота, роль в синтезе и использовании одно-
углеродных радикалов. Метилирование гомоцистеина.
В превращениях серина и глицина главную роль играют ферменты, коферментами которых служат производные фолиевой кислоты. Этот витамин широко распространён в животных и растительных пищевых продуктах. Молекула фолиевой кислоты (фолата) состоит из 3 частей: птеринового производного, парааминобензойной и глутаминовой кислот.
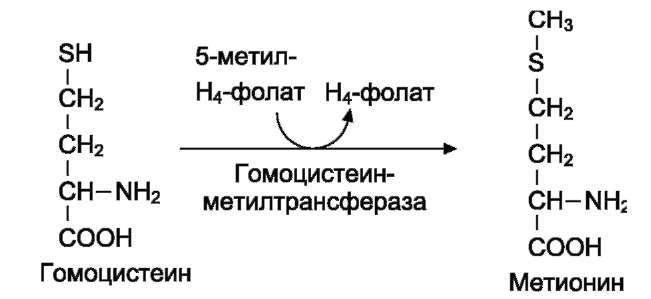
Гомоцистеин может снова превращаться в метионин под действием гомоцистеинметил-транс-феразы. Донором метильной группы в этом случае служит N5-метил-Н4-фолат:
32. Недостаточность фолиевой кислоты и витамина в12. Антивитамины
фолиевой кислоты. Механизм действия сульфаниламидных препаратов.
Недостаточность фолиевой кислоты у человека возникает редко Гиповитаминоз фолиевой кислоты приводит к нарушению обмена одноуглеродных фрагментов. Такое же нарушение наблюдается и при недостаточности витамина В12, использование которого связано с обменом фолиевой кислоты
Первое проявление дефицита фолиевой кислоты - мегалобластная (макроцитарная) анемия. Она характеризуется уменьшением количества эритроцитов, снижением содержания в них гемоглобина, что вызывает увеличение размера эритроцитов.
Мегалобластная анемия возникает чаще всего в результате недостаточности фолиевой кислоты и/или витамина В12.
Фолиевая кислота является витамином для человека и животных. Однако многие патогенные бактерии способны синтезировать это соединение, используя парааминобензойную кислоту (ПАБК) - одну из составных частей фолата. ПАБК поступает в бактериальные клетки из внешней среды. Сульфаниламидные лекарственные препараты - производные сульфаниламида (белого стрептоцида), похожи по строению на парааминобензойную кислоту. Отличаются они только радикалами.
Эти препараты подавляют синтез фолиевой кислоты у бактерий, потому что:
• конкурентно ингибируют бактериальные ферменты синтеза фолата, так как являются структурными аналогами парааминобен-зойной кислоты - одного из субстратов процесса;
• могут использоваться как псевдосубстраты из-за относительной субстратной специфичности ферментов, в результате чего синтезируется соединение, похожее на фолиевую кислоту, но не выполняющее её функции.
В обоих случаях в клетках бактерий нарушается обмен одноуглеродных фрагментов и, следовательно, синтез нуклеиновых кислот, что вызывает прекращение размножения бактерий.
В клетках больного сульфаниламидные лекарственные вещества не вызывают подобных изменений, поскольку человек получает с пищей готовую фолиевую кислоту.
33. Обмен фенилаланина и тирозина. Все пути превращения в норме.
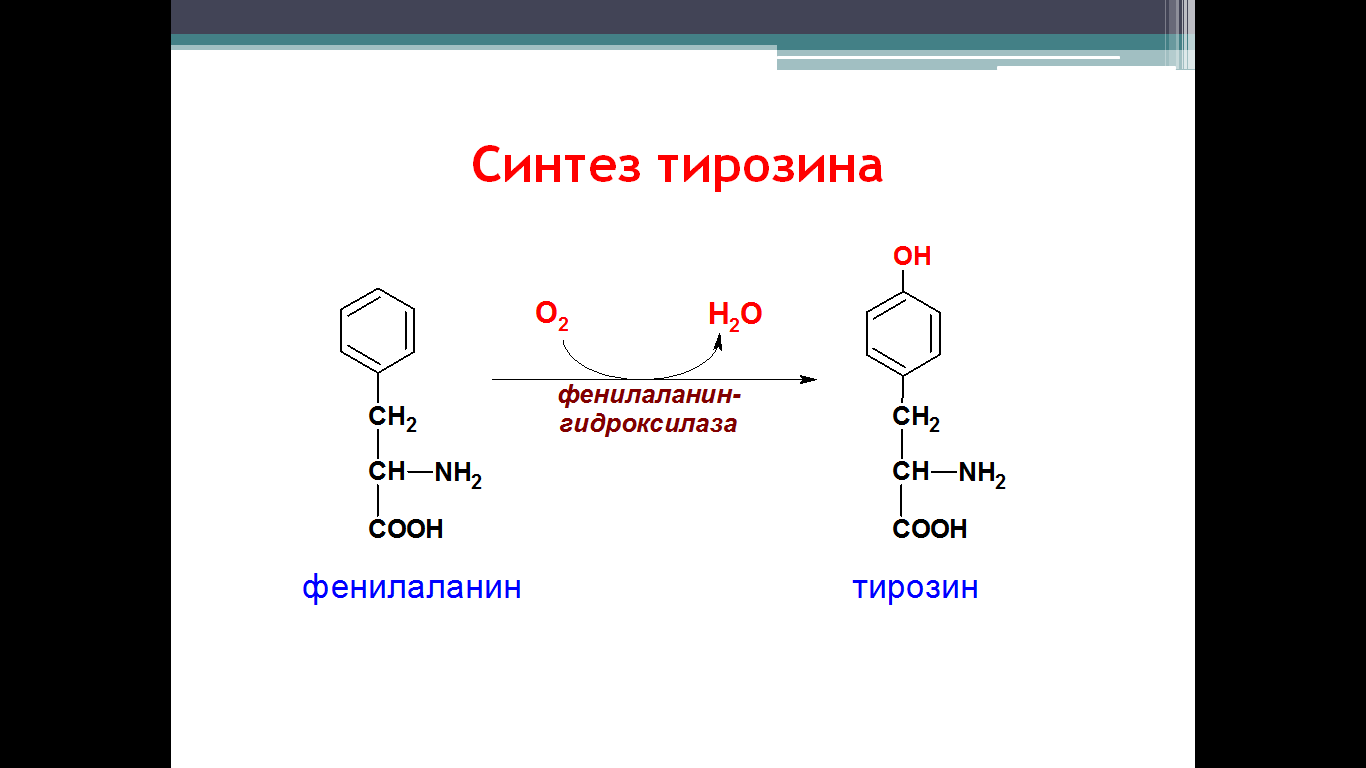
Метаболизм фенилаланина
Основное количество фенилаланина расходуется по 2 путям:
• включается в белки;
• превращается в тирозин. Превращение фенилаланина в тирозин прежде
всего необходимо для удаления избытка фени-лаланина, так как высокие концентрации его токсичны для клеток. Образование тирозина не имеет большого значения, так как недостатка этой аминокислоты в клетках практически не бывает.
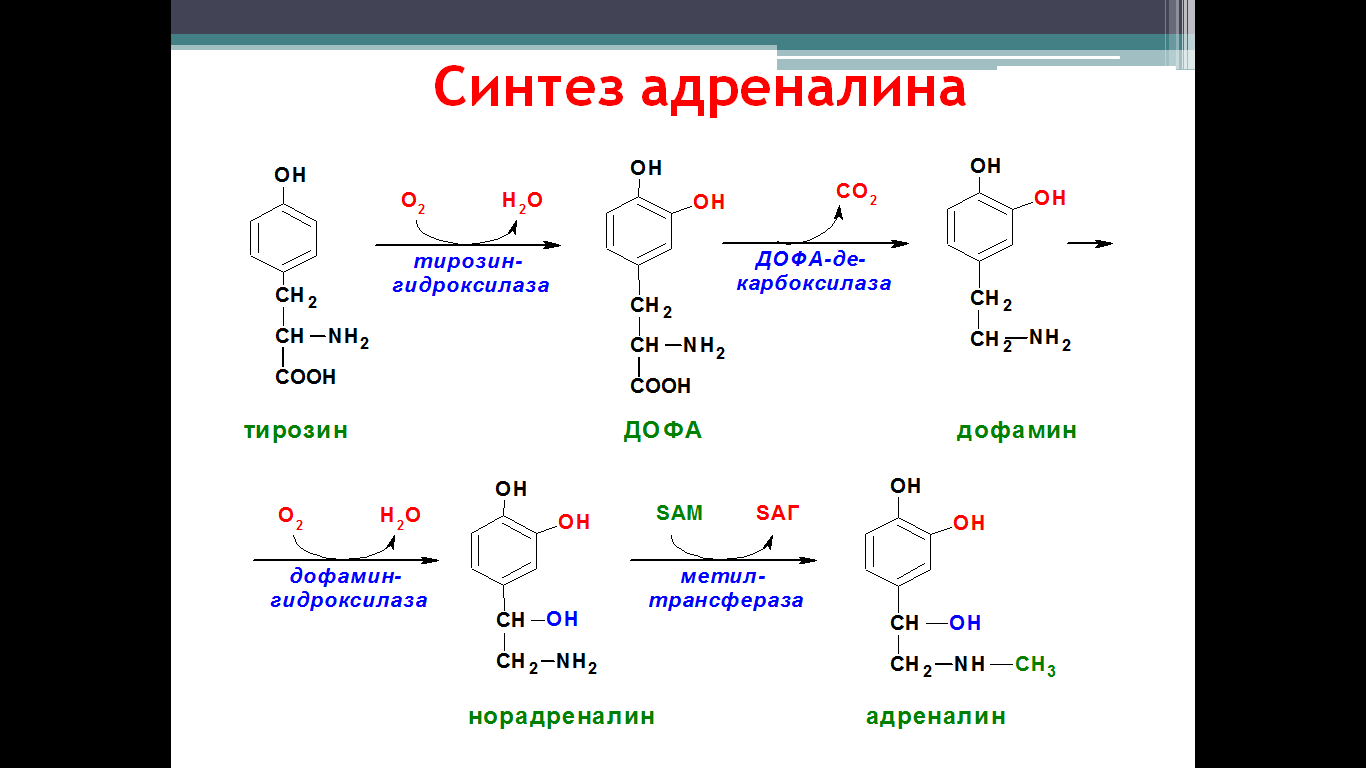
Обмен тирозина значительно сложнее, чем обмен фенилаланина. Кроме использования в
синтезе белков, тирозин в разных тканях выступает предшественником таких соединений, как катехоламины, тироксин, меланины, и катаболизируется до СО2 и Н2О.
37. Конечные продукты азотистого обмена: соли аммония и мочевина.
Наиболее значительные количества аммиака обезвреживаются в печени путём синтеза мочевины. В первой реакции процесса аммиак связывается с диоксидом углерода с образованием карбамоилфосфата, при этом затрачиваются 2 молекулы АТФ.
Мочевина - основной конечный продукт азотистого обмена, в составе которого из организма выделяется до 90% всего выводимого азота (рис. 9-15). Экскреция мочевины в норме составляет ~25 г/сут. При повышении количества потребляемых с пищей белков экскреция мочевины увеличивается. Мочевина синтезируется только в печени.
... Соли аммония - это сложные вещества, в состав которых входят ионы аммония NH4+, соединённые с кислотными остатками... УСЁ.
38. Основные источники и пути обезвреживания аммиака в организме.
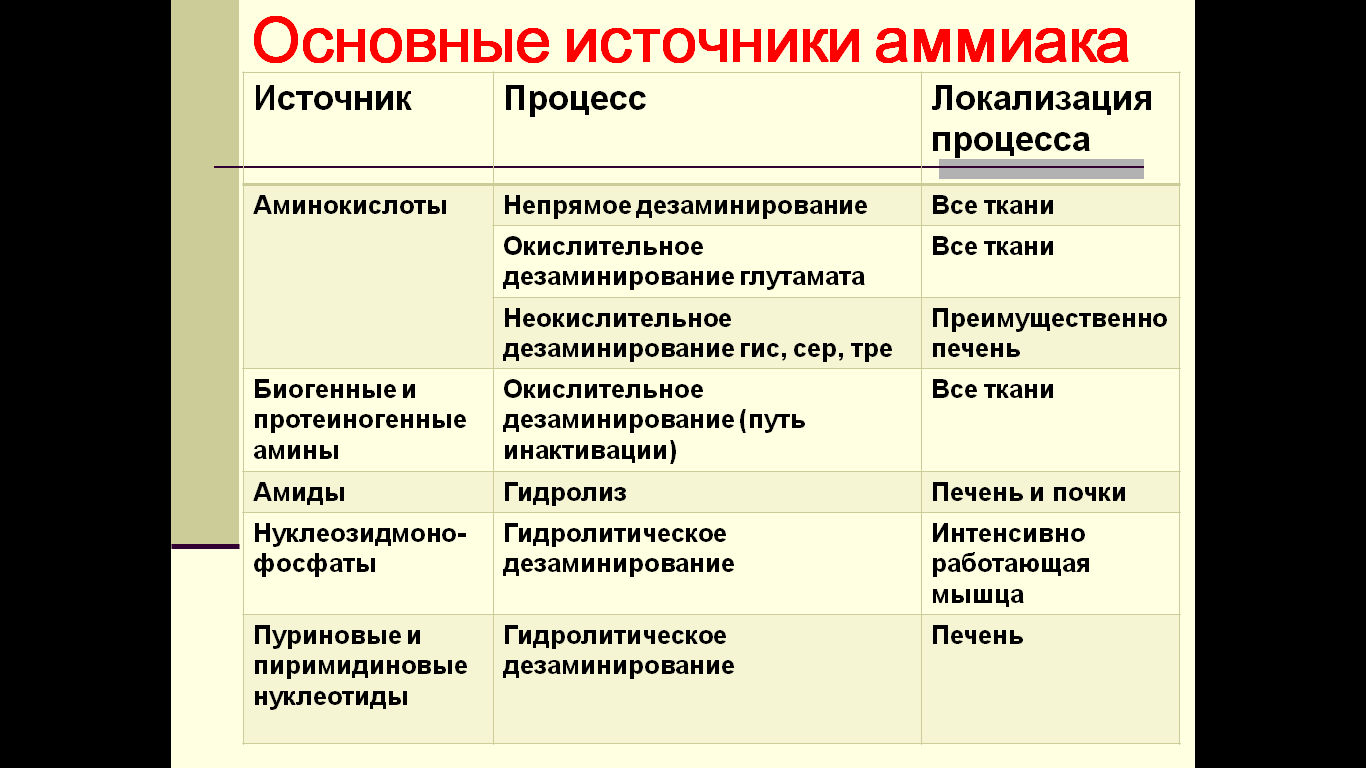
Обезвреживание аммика может быть на месте, так где он собственно образуется, и возможны разные механизмы, такие как.
- Восстановительное аминирование α-кетоглутарата
- Амидирование аминокислот (синтез амидов)
- Амидирование карбоксильных групп белков
- Синтез карбамоилфосфата
- Синтез аммонийных солей
И конечно же, главный способ ликвидации это - синтез мочевины, которы расписан ниже.
39. Роль глутамина в обезвреживании и транспорте аммиака в организме.
Глутами - тот парень, который берет на себя всю основную нагрузку, связанный с работой с аммиаком. Основной реакцией связывания аммиака, протекающей во всех тканях организма, является синтез глутамина под действием глутамин-синтетазы:
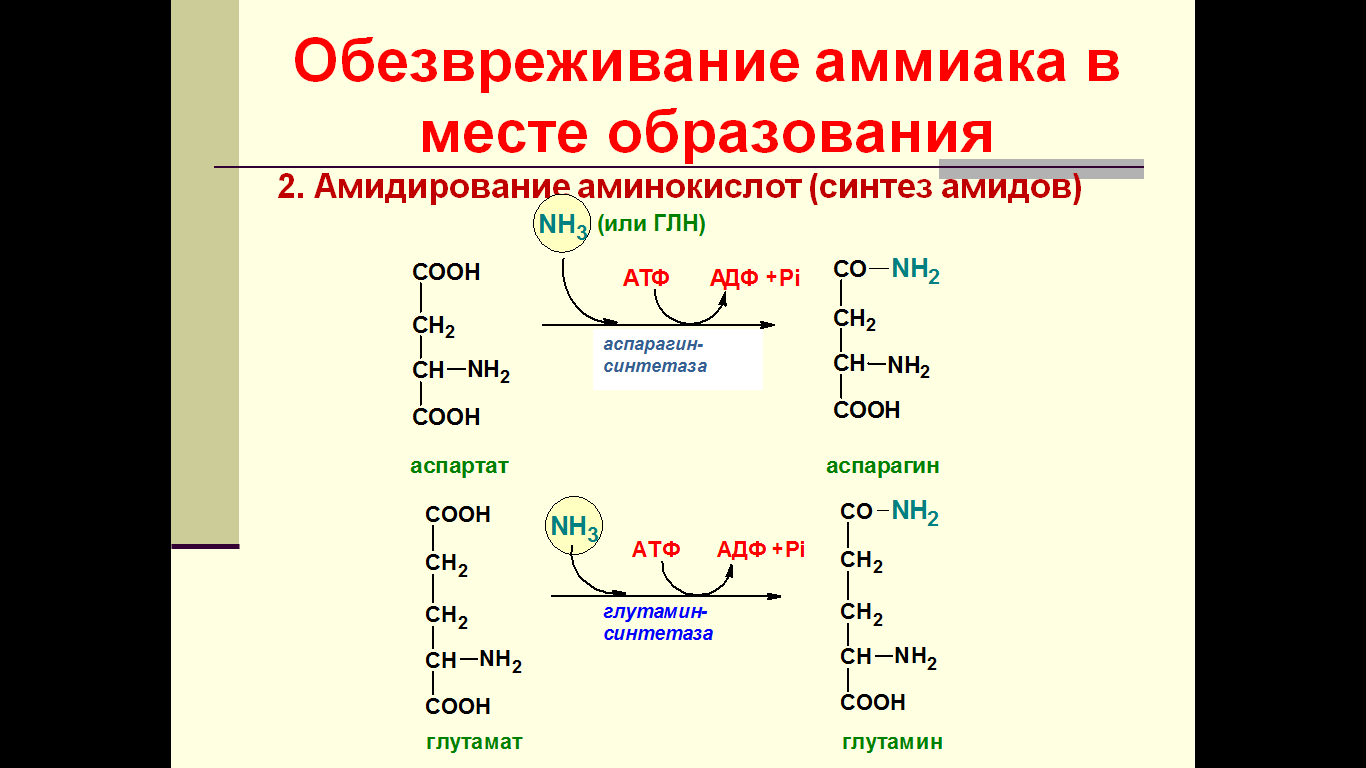
Глутамин легко транспортируется через клеточные мембраны путём облегчённой диффузии (для глутамата возможен только активный транспорт) и поступает из тканей в кровь. Основными тканями-поставщиками глутамина служат мышцы, мозг и печень. С током крови глутамин транспортируется в кишечник и почки.
В клетках кишечника под действием фермента глутаминазы происходит гидролитическое освобождение амидного азота в виде аммиака. В почках тоже самое.
40. Глутамин как донор амидной группы при синтезе ряда соединений.
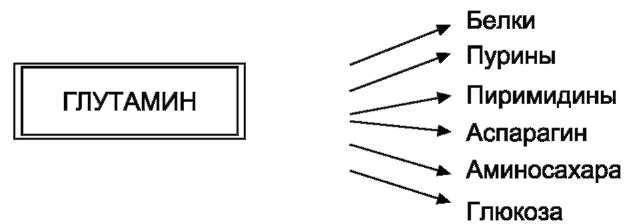
Глутамин - основной донор азота в организме.Амидный азот глутамина используется для синтеза пуриновых и пиримидиновых нук-леотидов, аспарагина, аминосахаров и других соединений
41. Синтез мочевины, химизм, ферменты, энергетика, происхождение атомов азота в мочевине.
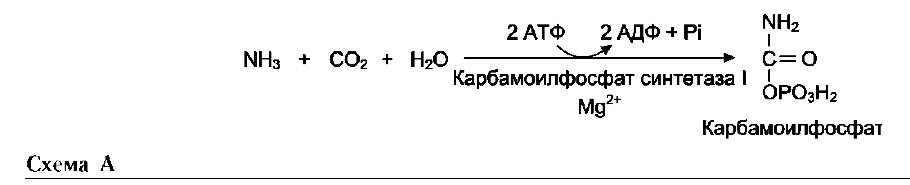
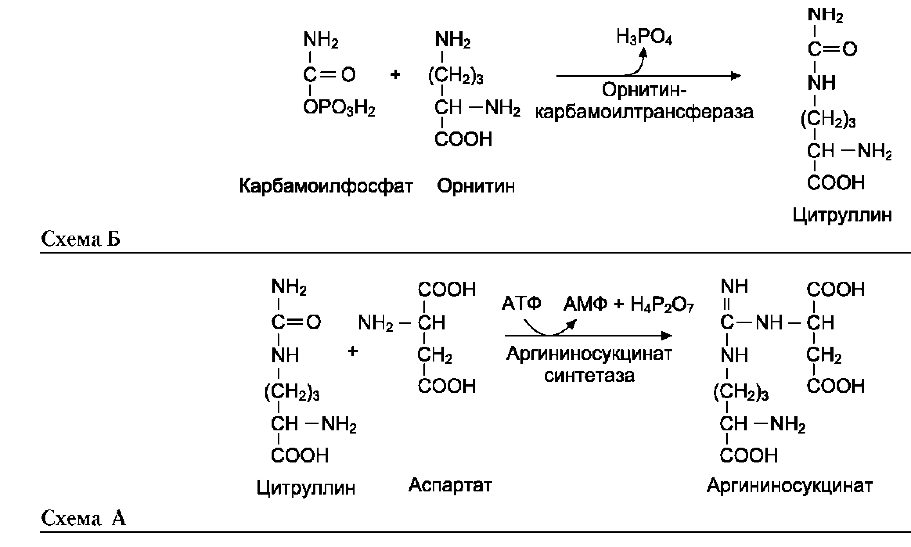
Мочевина (карбамид) - полный амид угольной кислоты - содержит 2 атома азота. Источником одного из них является аммиак, который в печени связывается с диоксидом углерода с образованием карбамоилфосфата под действием карбамоилфосфатсинтетазы I
Далее под действием орнитин-карбамоил-трансферазы карбамоильная группа карбамо-илфосфата переносится на α-аминокислоту орнитин, и образуется другая α-аминокислота - цитруллин.
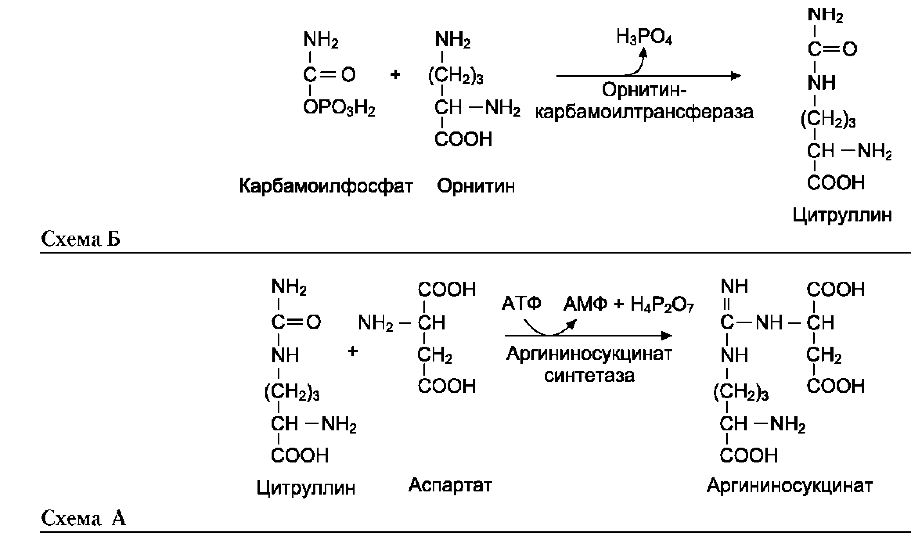
В следующей реакции аргининосукцинат-синтетаза связывает цитруллин с аспартатом и образует аргининосукцинат (аргининоянтарную кислоту). Этот фермент нуждается в ионах Mg2+. В реакции затрачивается 1 моль АТФ, но используется энергия двух макроэргических связей. Аспартат - источник второго атома азота мочевины
34. Фенилкетонурия, биохимический дефект, проявление болезни,
диагностика, лечение.
Классическая ФКУ - наследственное заболевание, связанное с мутациями в гене фенилаланингидроксилазы, которые приводят к снижению активности фермента или полной его инактивации. При этом концентрация фенилаланина повышается в крови в 2030 раз (в норме - 1,0-2,0 мг/дл), в моче - в 100-300 раз по сравнению с нормой (30 мг/дл).
Наиболее тяжёлые проявления ФКУ - нарушение умственного и физического развития, судорожный синдром, нарушение пигментации. При отсутствии лечения больные не доживают до 30 лет
Диагностика:
Производится полуколичественным тестом или количественным определением фенилаланина в крови. При нелеченных случаях возможно выявление продуктов распада фенилаланина (фенилкетонов) в моче (не ранее 10—12 дня жизни ребёнка).
Лечение:
Прогрессирующее нарушение умственного и физического развития у детей, больных ФКУ, можно предотвратить диетой с очень низким содержанием или полным исключением фе-нил-аланина. Если такое лечение начато сразу после рождения ребёнка, то повреждение мозга предотвращается. Считается, что ограничения в питании могут быть ослаблены после 10-летнего возраста (окончание процессов миелинизации мозга), однако в настоящее время многие педиатры склоняются в сторону «пожизненной диеты».
35. Алкаптонурия, альбинизм. Биохимический дефект, проявление болезней.
Алкаптонурия («чёрная моча»)
Причина заболевания - дефект диоксигеназы гомогентизиновой кислоты. Для этой болезни характерно выделение с мочой большого количества гомогентизиновой кислоты, которая, окисляясь кислородом воздуха, образует тёмные пигменты алкаптоны. Клиническими проявлениями болезни, кроме потемнения мочи на воздухе, являются пигментация соединительной ткани (охроноз) и артрит. Частота - 2-5 случаев на 1 млн новорождённых. Заболевание наследуется по аутосомно-рецессивному типу. Диагностических методов выявления гетерозиготных носителей дефектного гена к настоящему времени не найдено.
Альбинизм
Причина метаболического нарушения - врождённый дефект тирозиназы. Этот фермент катализирует превращение тирозина в ДОФА в меланоцитах. В результате дефекта тирозиназы нарушается синтез пигментов меланинов.
Клиническое проявление альбинизма (от лат. albus - белый) - отсутствие пигментации кожи и волос. У больных часто снижена острота зрения, возникает светобоязнь. Длительное пребывание таких больных под открытым солнцем приводит к раку кожи. Частота заболевания 1:20 000.
36. Нарушения синтеза дофамина при паркинсонизме.
Заболевание развивается при недостаточности дофамина в чёрной субстанции мозга. Это одно из самых распространённых неврологических заболеваний (частота 1:200 среди людей старше 60 лет). При этой патологии снижена активность тирозингидроксилазы, ДОФА-декарбоксилазы. Заболевание сопровождается тремя основными симптомами: акинезия (скованность движений), ригидность (напряжение мышц), тремор (непроизвольное дрожание). Дофамин не проникает через гематоэнцефалический барьер и как лекарственный препарат не используется. Для лечения паркинсонизма предлагаются следующие принципы:
• заместительная терапия препаратами-предшественниками дофамина (производными ДОФА) - леводопа, мадопар, наком и др.
• подавление инактивации дофамина ингибиторами МАО (депренил, ниаламид, пиразидол и др.).
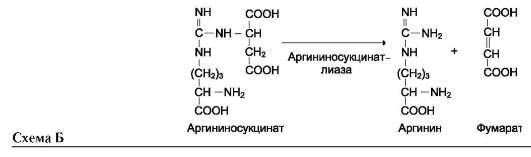
Далее фермент аргининосукцинатлиаза (арги-ниносукциназа) расщепляет аргининосукцинат на аргинин и фумарат, при этом аминогруппа аспартата оказывается в молекуле аргинина.
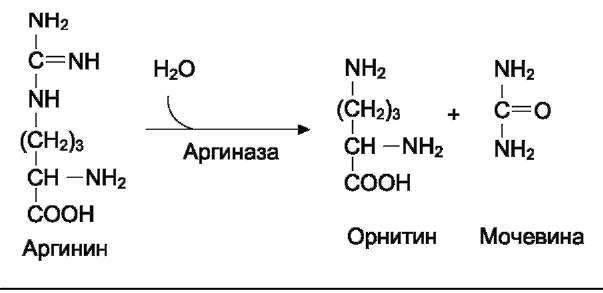
Аргинин подвергается гидролизу под действием аргиназы, при этом образуются орнитин и мочевина. Кофакторами аргиназы являются ионы Са2+ или Мп2+.
Всю эту красотень можно выразить формулой попроще.
СО2 + NH3 + Аспартат + 3 АТФ + 2 Н2О → Мочевина + Фумарат + 2 (АДФ + Н3РО4) + АМФ + Н4Р2О7
Энергетика ... загружаю... снятие грифа секретности...
В результате орнитинового цила расходуются четыре макроэргические связи трех молекул АТФ на каждый оборот цикла. Однако, все неплохо компенсируется:
- при включении фумарата в ЦТК на стадии дегидрирования малата образуется НАДН, который обеспечивает синтез трех молекул АТФ.
- при окислительном дезаминировании глутамата в разных органах также образуется НАДН, и образуется еще три молекулы АТФ.
Биологическая роль, две основные цели:
- превращение азота аминокислот в мочевину, которая экскретируется и предотвращает накопление токсичных продуктов, главным образом аммиака.
- синтез аргинина и пополнение его фонда в организме.
Основной источник аммиака - аминокислоты. Большая часть образовавшегося аммиака обезвреживается в орнитиновом цикле в печени и выделяется в виде мочевины. Основной реакцией обезвреживания аммиака в тканях является синтез глутамина, который затем используется в анаболических процессах и для обезвреживания веществ в печени.