Материал: Metod_Dipl_bak_2017_РВЦ (3)
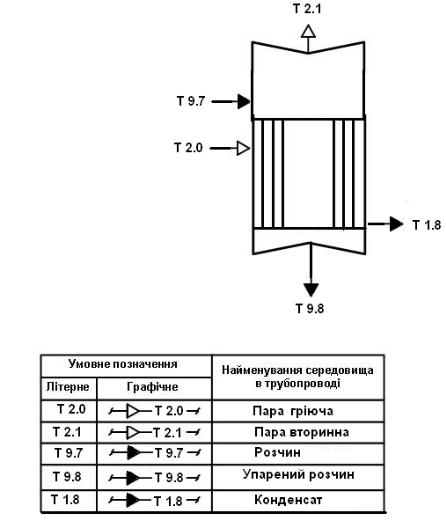
Рис. 5.3. Позначення на апаратурній схемі однокорпусного вакуум-випарного апарату з центральною циркуляційною трубою
Оскільки передбачається виготовлення препарату на основі бактеріоцину у вигляді засобу для зовнішнього застосування, антибактеріальний пептид необхідно частково звільнити не тільки від баластних речовин, а й від супутніх ферментів. Для цього пропонується використовувати метод ультрафільтрації, оскільки він має ряд очевидних переваг: проводиться в "м'яких" умовах, що забезпечують менший відсоток зниження активності ферменту (на відміну від вакуум-упарювання, де необхідне нагрівання розчину бактеріоцину). Крім того, здійснюється очищення від баластних низькомолекулярних домішок і збільшення активності ферменту в 100–150 разів. Процес ультрафільтрації в режимі діалізу дозволяє отримувати високоочищені препарати. Для його здійснення в одержуваний концентрат постійно додають чисту воду. Така п'ятикратна промивка дозволяє в 250–300 разів підвищити активність ферментного розчину, тобто при концентрації 30 % розчин містить практично один білковий ферментний препарат [81].
На практиці процес ультрафільтрації проводять в циркуляційних апаратах періодичної дії. У ході проведення процесу ультрафільтрації в залежності від властивостей одержуваного ферменту розчин постійно охолоджується до температури 4–15 ° С.
Недоліком методу ультрафільтрації слід вважати забивання пор мембрани осадами або адсорбованими молекулами, що призводить до зниження продуктивності мембранного апарату в часі. Останнє вимагає періодичного проведення промивки матеріалу мембрани. Для запобігання забивання пор мембрани осадами передбачено використовувати
31
циркуляційний насос, що забезпечує лінійну швидкість потоку рідини через мембрану близько 2–5 м/с. При таких швидкостях спостерігається значний гідравлічний опір. Для його зниження на практиці застосовують дві конструкції мембранних апаратів: трубчасті мембранні апарати і проточні з плоскими мембранними елементами, що встановлюються паралельно основному потоку [81].
При ультрафільтрації супернатант розділяється на високомолекулярний і низькомолекулярний (фільтрат) розчин. Спочатку пропонується здійснити діаліз на фільтрах із діаметром пор 10 кДа для відділення низькомолекулярних сполук (солей, амінокислот тощо). Фільтрат проходить крізь мембрану і видаляється через дренажну систему, а високомолекулярний продукт концентрується [81]. Внаслідок цього на фільтрі затримується бактеріоцин та інші високомолекулярні сполуки, молярна маса яких перевищує 10 кДа. Наступним етапом є ультрафільтрація на фільтрах із діаметром пор 32 кДа, оскільки встановлено [60], що молекулярна маса бактеріоцину, синтезованого Е. faecium DSH20 становить 32 кДа. Даний процес забезпечить одержання високоочищеного розчину (фільтрату) бактеріоцину та відділення молекул, молекулярна маса яких перевищує 32 кДа.
Отже, для виділення та очищення бактеріоцину передбачено фільтраційне центрифугування культуральної рідини з наступним концентруванням та очищенням розчину антимікробного пептиду двостадійною ультрафільтрацією.
Зверніть увагу! Під час вибору і обґрунтування стадій виділення і очищення цільового продукту необхідно враховувати, що деякі з методів використовуються тільки в лабораторних умовах і не можуть бути реалізовані у промисловому виробництві. До таких методів належать насамперед: гельхроматографія і її різновид гель-фільтрація з використанням як нерухомої фази сефарози і сефадексів відповідно, тонкошарова хроматографія та ін. Такі лабораторні методи препаративного виділення та очищення цільового продукту наводяться зазвичай у наукових статтях, а також у патентній літературі. Потрібно також враховувати, що велика кількість методів використовуються для аналізу, а не для виділення та очищення цільового продукту (наприклад, газо-рідинна хроматографія, більшість різновидів високоефективної рідинної хроматографії).
У процесі обґрунтування вибору стадій виділення і очищення цільового продукту необхідно обов’язково обгрунтувати вибір необхідних для певної технології допоміжних робіт.
До таких допоміжних робіт насамперед відносять:
1.Підготовка вентиляційного повітря (одержання пробіотиків,
вакцин).
2.Приготування розчинів для попередньої обробки культуральної рідини, екстракції, осадження цільового продукту і т.д. (наприклад, приготування 40 % розчину сульфату амонію для осадження ферментів, приготування складових розчину (25–50 % ізопропілового спирту, 25–35 % їдкого натру) для сольволізу біомаси дріжджів у процесі виділення ергостерину, розчину амонію для елюції (десорбції) амінокислот під час іоннообмінної хроматографії тощо).
3.Приготування захисного середовища у технологіях пробіотиків чи заквашувальних композицій тощо.
4.Підготовка повітря для розпилювальних сушарок.
32
Розділ 6. Матеріальний баланс і розрахунок обладнання
Цей розділ виконується згідно вимог до виконання курсових проектів з дисциплін «Основи проектування біотехнологічних виробництв» [2] та «Харчова біотехнологія» [3], а також методичних рекомендацій до практичних занять з дисципліни «Основи проектування біотехнологічних виробництв» [1].
Розрахунок обладнання передбачає розрахунок всього обладнання, передбаченого технологічною і апаратурною схемою (для стадій підготовки посівного матеріалу, виробничого біосинтезу, виділення та очищення цільового продукту).
Для заповнення таблиці матеріального балансу попередньо здійснюють продуктовий розрахунок на підставі проведеного техніко-економічного обгрунтування, даних щодо умов культивування (склад поживного середовища, тривалість культивування), а також концентрації біомаси і цільового продукту в культуральній рідині. Показники росту і синтезу цільового продукту визначаються з літературних джерел (патенти, наукові статті, нормативнотехнологічна документація на дану технологію тощо) та задаються вихідними величинами, що включають концентрацію біомаси та цільового продукту, коефіцієнти заповнення ємнісного обладнання, втрати цільового продукту по стадіях виділення.
Приклад 23. Згідно з ТЕО для забезпечення сільськогосподарських тварин та птиці в ферментованих кормах в Київській області за рік необхідно одержати GГП = 74 умовних тон ферментного препарату Ксилаваморин Г3Х із стандартною активністю Аст = 1000 од.ГцС/г та вмістом вологи Wв = 0,12 (частка). Дану кількість ферменту потрібно отримати за ТРД = 300 робочих днів.
Відомо, що ксиланаза з концентрацією в культуральній рідині Ркр = 1,5 г/л та активністю Акр = 34,5 од од.ГцС/мл утворюється при культивуванні Aspergillus awamori 2B.361 U2/1 при концентрації біомаси Хкр = 3 г/л на середовищі наступного складу, г/л : С1 – пшеничні висівки – 30; С2 – сечовина – 10; С3 – КН2РО4 – 3; С4 – К2НРО4 – 6; С5 – MgSO4 ×
7H2О – 0,2; С6 – CaCl2 × 2H2О – 0,05 [25]. Всього – СΣф = 49,25 г/л.
Для одержання посівного матеріалу використовують середовище такого самого
складу.
Для подальших розрахунків приймаємо наступні показники:
-час циклу роботи ферментера Тцф = Твб + Тпо = 48 + 12 = 60 год, де Твб і Тпо – тривалість виробного біосинтезу і підготовчих операцій відповідно;
-сумарні втрати при виділенні цільового продукту Ев = 0,2 (частка);
-сумарні втрати активності фермента при виділенні цільового продукту Еаф = 0,18 (частка);
-в залежності від виду ферментного препарату ступінь очищення препарату Еоч приймається в межах (0,5…0,9), приймаємо Еоч = 0,7
-втрати культуральної рідини під час біосинтезу і отриманні посівного матеріалу в результаті краплевиносу через колектор відпрацьованого повітря для всіх стадій становлять ЕФ = Еі = 0,1 (частка);
-втратами культуральної рідини під час вирощування посівного матеріалу в колбах на качалках через їх незначну кількість нехтуємо;
-кількість посівного матеріалу для ферментера, інокуляторів і колб обираємо ХФ = Хі = Хколб = 0,1 (частка);
-коефіцієнт запасу, що враховує можливість нестерильних операцій приймаємо К1 = 1,1;
33

-коефіцієнт заповнення ферментера та інокуляторів обираємо КЗ = 0,6;
-коефіцієнт заповнення качалочних колб приймаємо КЗколб = 0,2;
-коефіцієнт заповнення реакторів-змішувачів обираємо Кзр = 0,8;
1.Розрахунок кількості виробничих циклів
1.1.Кількість ферменту за добу в умовних кг :
Gгпд = Gгп /Tрд = 74·1000/300 = 247 кг/добу.
1.2. Кількість ферменту в умовних кг за цикл з врахуванням втрат при його виділенні
Gцк = Gгпд· Тцф·(1–Wв)/24·(1–Есв) = 2477·60·(1–0,12)/24·(1–0,2) = 679 ум.кг/цикл.
1.3.Кількість одиниць активності ферменту, що знаходяться в умовних кг з
врахуванням втрат активності при виділенні за цикл Ацк = Аст·1000/(1–Еа) = 1000·1000/(1–0,18) = 1,2·106 од.ГцС
1.4.Кількість одиниць активності культуральної рідині в товарних кг за цикл
Акрт = Акр·103/Ркр·10-3 = 34,5·103 /1,5·10-3 =2,3·107 од.ГцС/цикл
1.5 Кількість ферменту в товарних кг за цикл
Gцкт = Ацк· Gцк/ Акрт = 1,2·106·679/2,3·107= 35 тов.кг/цикл
1.6. Об’єм культуральної рідини, що зливається за цикл, становитиме:
Vкр = К1· Gцк/Ркр = 1,1· 35/1,5 = 25,6 м3/цикл
1.4. Визначаємо кількість ферментацій (циклів) на рік:
NЦ = Gгп/Gцк·(1- Wв) = 74 000/679·(1-0,12) =123,8. Приймаємо 124 циклів.
2. Приготування та стерилізація поживних середовищ для виробничого культивування та вирощування посівного матеріалу
2.1. Приготування та стерилізація поживного середовища для виробничого біосинтезу
Кількість поживного середовища (ПС) та посівного матеріалу (ПМ) в ферментері до культивування становить:
Vф = Vкр/(1 Еф) = 25,6/(1 0,1) = 28,4 м3.
Кількість поживного середовища в ферментері складе: Vпс = Vф/(1+Хф) = 28,4/(1+0,1) = 25,8 м3.
Необхідна кількість посівного матеріалу для засіву ферментера:
Vпмф = Vф – Vпс = 28,4 – 25,8 = 2,6 м3.
При вибраному коефіцієнті заповнення ферментера Кз = 0,6 його приблизний геометричний об’єм ферментера складе Vгф = Vф/Кз = 28,4/0,6 = 47,3 м3.
За Таблицею 11.1. [1]) обираємо ферментер геометричним об’ємом 50 м3
2.2. Визначаємо кількість стадій вирощування посівного матеріалу
Оскільки кількість посівного матеріала становить Хф = Хі = Хколб = 0,1% від кількості пожиівного середовища визначаємо кількість посівного матреіала для інших стадій. Приблизна кількість посівного матеріала для інших стадій становитиме:
Посівний матеріал з інокулятора геометричним об’ємом Vін = 5м3
Vпмф = 2,6 м3 Vін = Vпмф/Кз = 2,6/0,6 = 4,3 м3
За Таблицею 11.1. [1] обираємо інокулятор геометричним об’ємом 5 м3 Посівний матеріал з інокулятора геометричним об’ємом Vін = 0,4 м3
Vпін1 = Vпмф Хін = 2,6·0,1= 0,260 м3 Vін = Vпін/Кз = 0,260/0,6 = 0,43 м3
За Таблицею 11.1. [1] обираємо інокулятор геометричним об’ємом 0,4 м3 Посівний матеріал з інокулятора геометричним об’ємом 40 л
Vпін2 = Vпін1 Хін= 260·0,1= 26 л Vін = Vпін/Кз = 26/0,6 = 43 л
За Таблицею 11.1. [1] обираємо інокулятор геометричним об’ємом 40 л. Посівний матеріал з качалочних колб
Vпмк = Vпін2 Хін= 26·0,1= 2,6 л ;
34

Всього колб – nколб = Vпмк /Vколб · КЗколб = 2,6/0,75 ·0,2= 18 колб.
Отже, підготовка посівного матеріала включатиме 4 стадії.
2.3. Приготування та стерилізація поживного середовища для виробничого біосинтезу в ферментері геометричним об’ємом 50 м3
Згідно з прийнятим складом поживного середовища для виробничого біосинтезу загальні витрати компонентів на визначений об’єм поживного середовища Vпс складають:
Gзаг = VпсСΣ = 25,8·49,25 = 1 270,7 кг, в тому числі покомпонентно, кг:
Пшеничні висівки – G1 = Gзаг (C1/C∑) = 1 270,7 (30/49,25) = 774,5
Сечовина – |
G2 = Gзаг (C2/C∑) = 1 |
270,7(10/49,25) = 258,0 |
||||
КН2РО4 |
– |
G3 |
= Gзаг (C3/C∑) = 1 |
270,7(3/49,25) |
= |
77,4 |
К2НРО4 |
– |
G4 |
= Gзаг (C4/C∑) = 1 |
270,7(6/49,25) |
= 154,8 |
|
MgSO4·7H2О – |
G5 = Gзаг (C5/C∑) = 1 270,7(0,2/49,25) = |
5,2 |
||||
CaCl2·2H2О – |
G6= Gзаг (C6/C∑) = 1 |
270,7(0,05/49,25) = 1,3 |
||||
Розрахунок кількості води для приготування поживного середовища для виробничого біосинтезу.
Кількість води визначають за такою формулою Vв = Vпс Gзаг 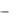 (Vпс Ккон), де Ккон – частка конденсату у загальній кількості води, що йде на приготування середовища, а VпсКкон
(Vпс Ккон), де Ккон – частка конденсату у загальній кількості води, що йде на приготування середовища, а VпсКкон
– загальна кількість утвореного конденсату.
Залежно від способу стерилізації та використовуваного обладнання величина Ккон може становити:
Ккон = 0 при стерилізації в закритих колбах або бутлях в автоклаві; Ккон = 0,1÷0,15 при стерилізації компонентів у реакторах-змішувачах, інокуляторах або ферментері при подачі гострої пари безпосередньо в середовище;
Ккон = 0,2 при стерилізації компонентів в УБС.
Оскільки об’єм поживного середовища для виробничого ферментера (без конденсату) становить Vпс = 20,6 м3, приймаємо рішення щодо використання для стерилізації УБС потужністю 20 м3/год.
Тоді загальна кількість конденсату, що утворюється при стерилізації ПС в УБС становитиме:
Vк = Vпс Ккон = 25,8·0,2 = 5,2 м3.
Загальна кількість води, необхідної для розбавлення компонентів поживного середовища,
буде: Vв = Vпс Vк Gзаг = 25800 5200 1271 = 19 329 л.
Для спрощення розрахунків приймемо, що густина компонентів приблизно дорівнює
густині води, тобто 1 л = 1кг. |
|
|
|
|
|
||
Розраховуємо кількість води для розчинення покомпонентно, л. |
|
|
|||||
Пшеничні висівки V1в =Vв (С1/CΣ) = 19 329(30/49,25) = 11 774 |
|
|
|||||
Сечовина |
V2в =Vв (С2/CΣ) = 19 329(10/49,25) = |
3 925 |
|
|
|||
КН2РО4 |
V3в =Vв (С3/CΣ) = 19 329(3/49,25) = |
1 177 |
|
|
|||
К2НРО4 |
V4в =Vв (С4/CΣ) = 19 329(6/49,25) = 2 355 |
|
|
||||
MgSO4 · 7H2О |
V5в =Vв (С5/CΣ) = 19 329(0,2/49,25) = |
78 |
|
|
|||
CaCl2 · 2H2О |
V6в =Vв (С6/CΣ) = 19 329(0,05/49,25)= |
20 |
|
|
|||
|
|
|
|
Всього: 19 329 л |
|||
Формування композицій: |
|
|
|
|
|
||
|
|
|
|
|
|
Таблиця 2.1. |
|
Склад композицій для стерилізації поживного середовища в УБС |
|||||||
Компонент |
|
|
Кількість для |
|
|
Об’єм |
|
Вміст, |
|
приготування |
|
|
|
||
поживного |
|
Композиція |
композиції, |
|
|||
г/л |
|
25,8 м3 середовища, кг |
|
||||
середовища |
|
|
(л) |
|
|
V, л |
|
|
|
|
|
|
|
|
|
Пшеничні висівки |
30 |
|
774,5 |
А |
12 549 |
|
|
|
|
|
|
|
|
35 |
|