Материал: Melnuchuk_Promuslova biotexnologij
РОЗДІЛ 6. БІОТЕХНОЛОГІЧНІ ОСОБЛИВОСТІ ОТРИМАННЯ МОЛОЧНОКИСЛИХ ПРОДУКТІВ
зокрема, у розчинах кальцію хлориду. У поліпептидному ланцюгу β - казеїну є дуже чутливий до протеолізу ферментами зв’язок, розщеплення якого призводить до дестабілізації міцели казеїну та утворення параказеїнового згустку за наявності іонів кальцію.
Фізичні та хімічні властивості казеїну залежать від його первинної структури, оскільки розташування амінокислотних залишків визначає просторову структуру молекул. Чітке уявлення про амінокислотну послідовність поліпептидних ланцюгів молекул, основних компонентів казеїну, має вирішальне значення для розуміння механізмів утворення міцел, їх структурної організації, дії на них окремих факторів, які є важливими для біотехнологічних процесів, зокрема в питаннях, що стосуються впливу температури або ферментативної взаємодії в процесі виробництва сирів.
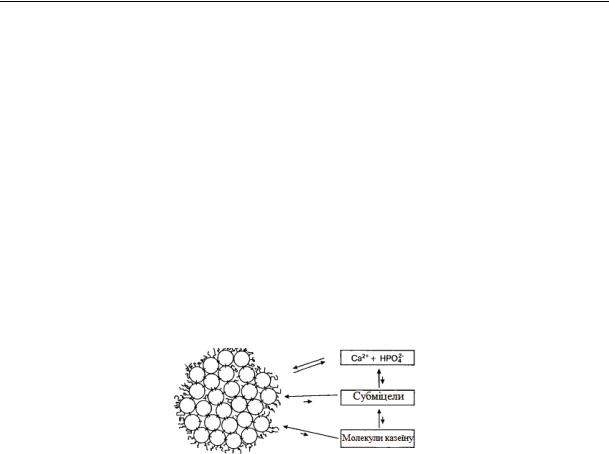
Структypa міцели казеїну остаточно не встановлена, незважаючи на інтенсивне її вивчення (рис.36).
Рис.36. Модель казеїнової міцели, що складається з сферичних субміцел, пов’язаних одна з одною колоїдним фосфатом кальцію, що показує ланцюжки макропептиду казеїну, що виступають назовні.
При зброджуванні молочного цукру молочнокислими бактеріями, під впливом утворюваної молочної кислоти відбувається кислотна коагуляція білків молока. Кислотна коагуляція казеїну лежить в основі отримання структурованого молочного згустку при виробництві кисломолочних продуктів.
При гомоферментативному молочнокислому бродінні з 1 моля лактози утворюється 4 моля молочної кислоти (342 г молочного цукру зброджується до 360 г молочної кислоти). Межа накопичення молочної кислоти залежить від виду застосовуваної закваски, температури сквашування та інших технологічних факторів. Молочнокислі палички мають більш високу межу накопичення молочної кислоти (до 140-250°Т), а лактококи – нижчий (90-130°Т).
В основі отримання казеїну лежить кислотна коагуляція білків молока в ізоелектричній точці (рН = 4,6-4,7). Механізм кислотної коагуляції полягає в тому, що при підкисленні молока відбувається поступова нейтралізація негативних груп (карбоксильних і фосфатних) казеїну і видалення зі складу казеїнових міцел колоїдного фосфату кальцію. При рН 4,9 частинки втрачають весь колоїдний фосфат кальцію і відбувається повне руйнування міцелярної структури. Подальше зниження
136
РОЗДІЛ 6. БІОТЕХНОЛОГІЧНІ ОСОБЛИВОСТІ ОТРИМАННЯ МОЛОЧНОКИСЛИХ ПРОДУКТІВ
рН розчину до ізоелектричної точки (ІТ) призводить до нейтралізації казеїнових частинок і зниження ступеня їх гідратації. Ізоелектричний стан супроводжується конформаційними змінами ланцюгів макромолекул казеїну всередині субміцел, а це призводить до часткової гідрофобізаціі їх поверхні і утворення нерозчинних у водному середовищі агрегатів. Подальше об'єднання субміцел за рахунок гідрофобних, водневих і, меншою мірою, іонних зв'язків призводить до утворення гелю.
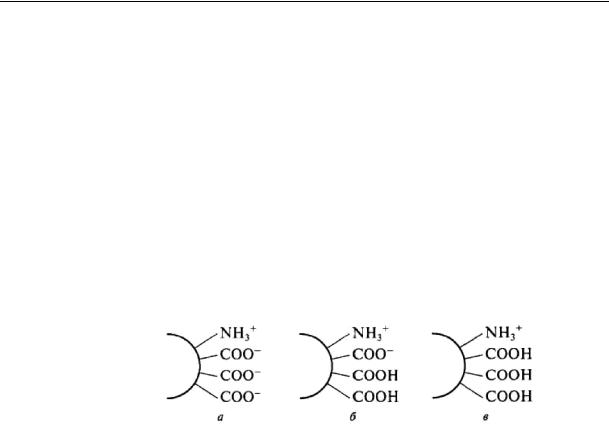
Примітка. Слід пам'ятати, що казеїн осідає тільки в ізоелектричній точці (ІТ). Так, при нестачі кислоти міцели мають негативний заряд і, отже, гідратовані, що перешкоджає їх осадженню. Надлишок кислоти призводить до перезарядження частинок казеїну, їх гідратації і повторному розчиненню. Характер поверхні казеїнових частинок при рН вище (а), нижче (в) і в ІТ (б) представлений на малюнку:
Робота № 26. Виділення та дослідження властивостей казеїну
Мета роботи: Вивчити механізм процесу кислотної коагуляції казеїну в ізоелектричній точці і визначити масу утворюваного білка.
Матеріали та обладнання: колби конічні місткістю 100 і 200 см3; циліндр мірний місткістю 100 см3; бюретка місткістю 25 см3; мірна піпетка місткістю 50 см; воронка; паперовий фільтр; 40%-й водний розчин CaCl2; сичужний фермент; закваска; молоко; віскозиметр; прилад для визначення коефіцієнта розтікання; міліметрівка; скло.
Хід роботи:
Казеїн молока володіє кислими властивостями, тому здатний взаємодіяти з лугом. У зв'язку з чим, масову частку казеїну можна визначити з різниці обсягів лугу, що пішла на нейтралізацію молока і безказеїнової сироватки.
1 етап. У конічну колбу вносять 20 мл молока і 80 мл дистильованої води (20°С). Вміст колби перемішують і титрують розчином сірчаної кислоти 0,05 моль/дм при постійному помішуванні до випадання казеїну в осад великими пластівцями, використовуючи при цьому індикаторний папір до настання значення рН = 4,6-4,7. Об'єм розчину сірчаної кислоти (Vк), що пішла на осадження казеїну, записують.
137

РОЗДІЛ 6. БІОТЕХНОЛОГІЧНІ ОСОБЛИВОСТІ ОТРИМАННЯ МОЛОЧНОКИСЛИХ ПРОДУКТІВ
Через 3-5 хв. після утворення осаду казеїну рідину фільтрують через сухий складчастий фільтр в конічну колбу місткістю 200 см3. Далі 50 мл фільтрату піпеткою переносять у конічну колбу місткістю 100 мл, додають 3-5 крапель 1%-ного розчину фенолфталеїну і титрують розчином гідроксиду натрію 0,1 моль/дм до слабо-рожевого забарвлення, не зникаючого протягом 30 с. Об'єм лугу (V) що пішов на титрування, записують.
2 етап. У конічну колбу вносять 20 мл молока, 80 мл дистильованої води і стільки ж сірчаної кислоти (0,05 моль/дм), скільки було потрібно на осадження казеїну на першому етапі, додають 3-5 крапель 1%-ного розчину фенолфталеїну, перемішують і титрують розчином гідроксиду натрію так само, як вище. Об'єм розчину лугу (V2), що пішов на титрування, записують.
Спочатку за наведеною нижче формулою розраховують обсяг лугу (X), який пішов на титрування всього розчину (молоко + вода + кислота):
Потім розраховують масову частку казеїну К ( в %) за формулою:
де Vк - об´єм розчину сірчаної кислоти, що було витрачено на осадження казеїну, мл; V1 - об'єм розчину гідроксиду натрію, що було витрачено на титрування 50 мл фільтрату, мл; 50 – вихідний об´єм розчину.
Потім розраховують масову долю казеїну К (у %) за формулою:
де V2 - об'єм розчину гідроксиду натрію, що було витрачено на титрування на другому етапі роботи, см3; X - розрахований об'єм розчину гідроксиду натрію, витрачений на титрування на першому етапі, см3; 0,1131 - маса казеїну, відповідна 1 мл розчину гідроксиду натрію з еквівалентною концентрацією 0,1 моль/дм3, г; m - об´єм молока, що було взято на дослідження, мл (20 мл).
6.3. Сичужне згортання молока
Отримання сичужного згустку є одним з найскладніших процесів в біотехнології сироваріння, в основі якого лежить ензиматичне перетворювання казеїну в параказеїн, з якого формується просторова структура згустку. Параказеїн утворюється внаслідок втрати казеїном колоїдної стійкості, викликаної гідролітичною дією реніну або інших молокозгортаючим ферментів.
Класичним молокозгортаючим препаратом є сичужний порошок, одержуваний зі слизової оболонки четвертого відділення шлунка (сичуга) підсисних телят і ягнят. Крім нього застосовують пепсини і ферментні
138
РОЗДІЛ 6. БІОТЕХНОЛОГІЧНІ ОСОБЛИВОСТІ ОТРИМАННЯ МОЛОЧНОКИСЛИХ ПРОДУКТІВ
препарати, що є сумішшю різних молокозгортаючих ферментів тваринного походження. Також використовують молокозгортаючі ферменти мікробного походження, але вони не є рівноцінною заміною сичужного порошку, оскільки відрізняються більшою протеолітичної активністю.
Сичужне (ензиматичне) згортання молока - перша стадія вироблення сичужних сирів, що складається з двох процесів:
•розщеплення 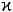 -казеїну на гідрофільний макропептід (МП) і гідрофобний пара-
-казеїну на гідрофільний макропептід (МП) і гідрофобний пара- 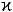 -казеїн, в результаті якого дезактивуються системи, що забезпечують стійкість міцели;
-казеїн, в результаті якого дезактивуються системи, що забезпечують стійкість міцели;
•флокуляції (агрегації) дестабілізованих параказеінових міцел, в результаті якої казеїн зі стану золю переходить в стан гелю і утворюється згусток.
Перший процес іде під дією ензимів і отримав назву первинної, або ензиматичної фази. Це реакція першого порядку, оскільки здатність до дифузії міцел казеїну занадто мала в порівнянні з рухливістю молекул молокозгортуючих ензимів. Автори гідролітичної теорії вважають, що під дією молокозгортуючого ферменту відбувається розрив пептидного
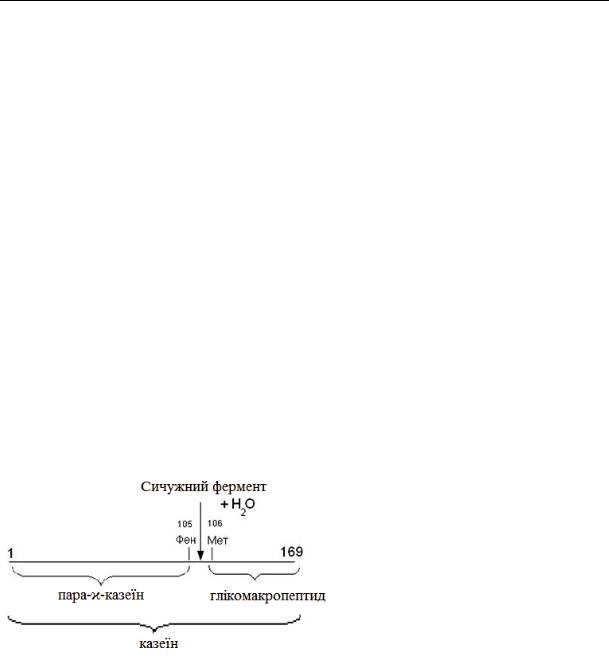
ланцюга 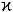 -казеїну між фенілаланіном і метіоніном (Phe105 – Met106) (рис.37). Від міцели
-казеїну між фенілаланіном і метіоніном (Phe105 – Met106) (рис.37). Від міцели 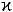 -казеїну відщеплюється глікомакропептид. Внаслідок цього
-казеїну відщеплюється глікомакропептид. Внаслідок цього 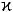 -казеїн перетворюється на пара-
-казеїн перетворюється на пара-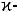 казеїн і втрачає свою
казеїн і втрачає свою
здатність забезпечити колоїдну стійкість казеїнових міцел.
Глікомакропептіди 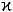 - казеїну мають високий негативний заряд і володіють сильними гідрофільними властивостями. При їх відщепленні від
- казеїну мають високий негативний заряд і володіють сильними гідрофільними властивостями. При їх відщепленні від 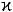 -казеїну знижується електричний заряд
-казеїну знижується електричний заряд
Рис. 37. Первинна, або ензиматична фаза
на поверхні казеїнових міцел (з поступовим наближенням до ізоелектричного стану), частково втрачається гідратна оболонка, в результаті чого знижується стійкість казеїнових міцел і вони коагулюють, настає друга стадія коагуляції.
Паралельно з біохімічним перетворенням казеїнового комплексу в результаті гідролітичної дії молокозгортуючих ферментів проходять фізико-хімічні зміни.
Закінчення цієї фази визначають по припиненню змін в молоці, що викликаються розщепленням 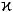 -казеїну хімозином, наприклад, з припинення збільшення вмісту небілкового азоту.
-казеїну хімозином, наприклад, з припинення збільшення вмісту небілкового азоту.
139
РОЗДІЛ 6. БІОТЕХНОЛОГІЧНІ ОСОБЛИВОСТІ ОТРИМАННЯ МОЛОЧНОКИСЛИХ ПРОДУКТІВ
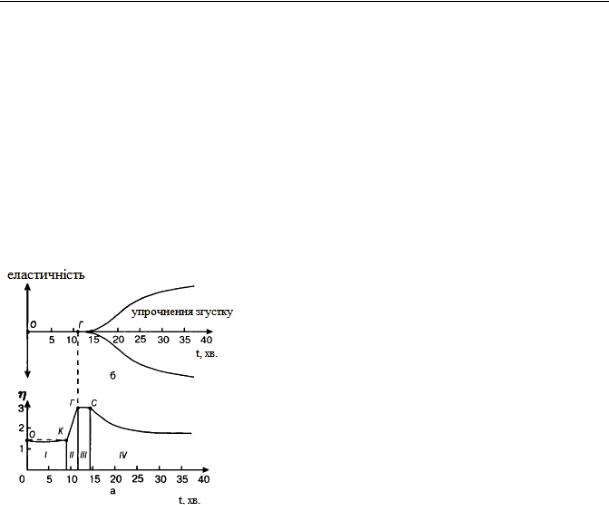
Другий процес йде без участі молокозгортаючих ензимів, в присутності іонів Ca, і називається вторинною (неензиматичною) фазою. На думку деяких вчених, процес сичужного згортання молока можна розділити на чотири стадії: індукційний період (лаг-фаза), який закінчується з початком утворення пластівців, візуально видимого; стадія флокуляції, що закінчується утворенням згустку; стадія метастабільної рівноваги, припиняється з початком синерезису, і синерезис (виділення рідкої фази з дисперсної структури (напр., гелю), що супроводжується зменшенням об'єму структури) (рис.38). Крива зміни в'язкості,
отримана ротаційним віскозиметром, має s-подібний вигляд. Вона показує, що після завершення індукційного періоду продовжується формування структури з наростаючою швидкістю. На початку відбувається агрегація окремих параказеїнових частинок, тобто так звана флокуляція - стадія II. Далі слідує стадія формування тривимірної просторової структури. Наприкінці згортання (точка Г) утворився згусток, що являє собою вищий рівень організації
структури.
Рис.38. Реограма (а) та еластограма (б) процесу сичужного згортання молока: (І – індукційний період, ІІ – стадія флокуляції, ІІІ – метастабільна рівновага, ІV – синеретична стадія; О – внесення сичужного ферменту, К – початок явної коагуляції, Г
– гель-точка, С – початок синерезиса
Модуль еластичності у нього менше модуля пружності. Тому сичужний згусток слід вважати еластичною системою. Протягом стадії III в'язкість залишається постійною, після чого починається руйнування структури з падінням в'язкості після крапки С (синерезис).
Друга і третя стадія поділяються так званою гель-точкою, положення якої визначається утворенням мінімальної кількості міжміцеллярних зв'язків, яке достатньо для утворення просторової структури - згустку. До гель-точки система зберігає властивості золю, після гель-точки утворюється гель - єдина просторова система, що володіє пружними властивостями. Ділянка реограми OK відповідає першій частині фази (до розщеплення 85% 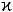 -казеїну); ділянка К-Г-С - друга фаза сичужного згортання молока. Ділянка Г-С характеризується зміцненням межміцеллярних зв'язків і посиленням пружних властивостей просторової системи. У точці С починається розшарування системи на тверду і рідку (сироватка) фази. Час досягнення гель-точки називають часом сичужного
-казеїну); ділянка К-Г-С - друга фаза сичужного згортання молока. Ділянка Г-С характеризується зміцненням межміцеллярних зв'язків і посиленням пружних властивостей просторової системи. У точці С починається розшарування системи на тверду і рідку (сироватка) фази. Час досягнення гель-точки називають часом сичужного
140