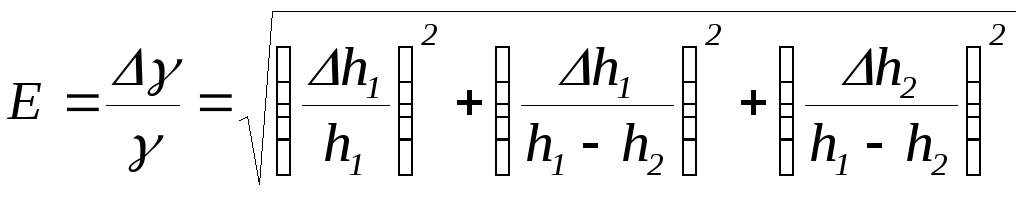Материал: Mekhanika_Ch2
18 Лабораторна робота № 7. Визначення величини співвідношення теплоємностей Cp/Cv для газів
МЕТА РОБОТИ
-
Провести спостереження за газовими процесами, що проходитимуть під час проведення дослідів.
-
Визначити величину показника адіабати для повітря.
-
Обчислити за даними роботи молярні та питомі теплоємності повітря.
ОБЛАДНАННЯ Лабораторна установка з водяним манометром.
18.1 Опис пристрою та методу вимірювання
Пристрій складається з скляного балону (1) об’ємом 12 л, гофрованої трубки (2), штока (3), рукоятки пружинного клапану (4), пружинного клапану (5), стопору (6), рукоятки штоку (7), водяного манометра (8) рис. 18.1.
Балон може сполучатись з атмосферою за допомогою пружинного клапану. Опускаючи чи піднімаючи рукоятку штока, можна збільшити або зменшити об’єм газу в балоні за рахунок розтягування або стискування гофрованої трубки. Стопор використовується для фіксування штока в верхньому положенні; водяним манометром вимірюється різниця тиску повітря в балоні та поза ним.
Під час виконання лабораторної роботи в балоні проходять чотири термодинамічних процеси. Розглянемо їх у тій послідовності, в якій вони проходять в лабораторній установці. Накачаємо в балон об'ємом V1 небагато повітря. Зазначимо, що це повітря не впливає на параметри того повітря, з яким в балоні здійснюються термодинамічні процеси; накачане повітря в термодинамічних рівняннях не бере участі. Це призведе до стиснення повітря балону до об'єму V2. На графіку (рис.18.2) це ділянка 1÷2. Цей перший процес проходить нерівномірно і неоднозначно. Тому графічно його показати неможливо і він зображений умовно штрих-пунктирною лінією.
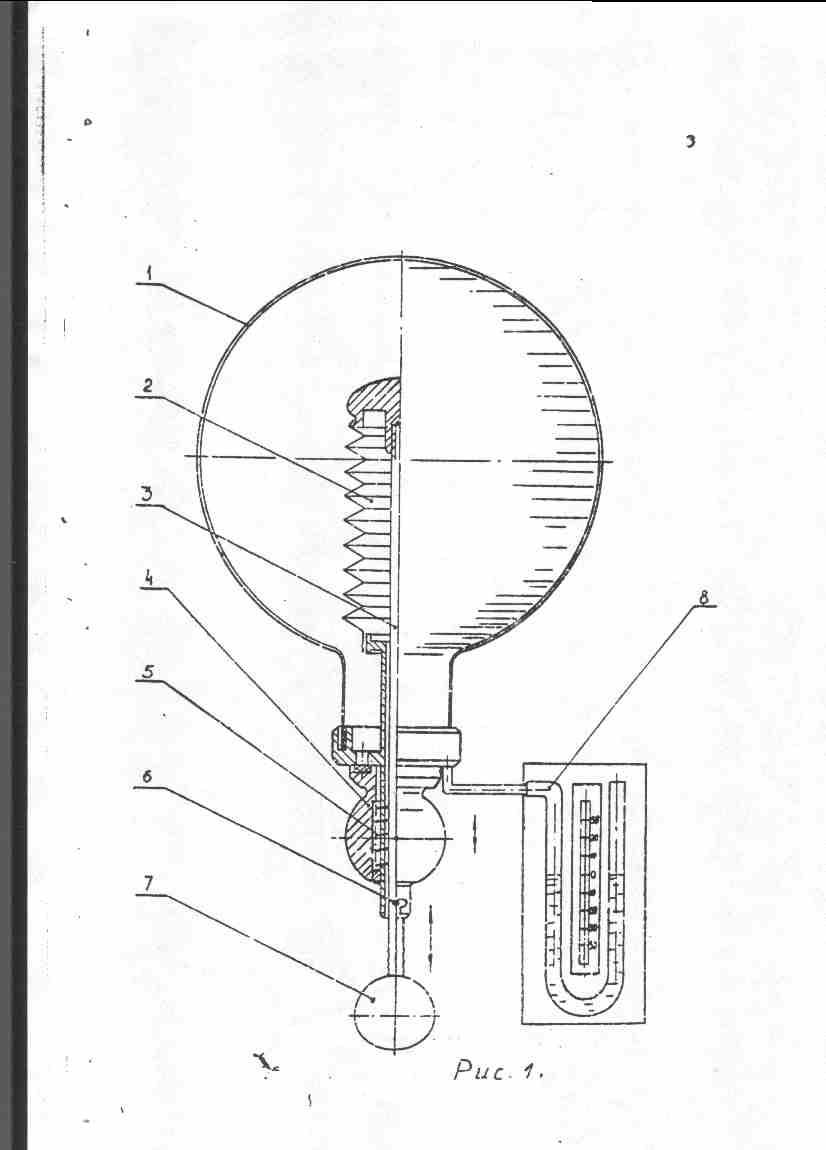
Рисунок 18.1
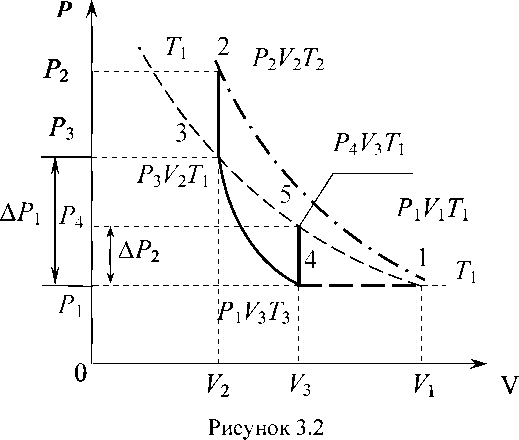
Рисунок 18.2
Відразу зазначимо, що реально в "чистому" вигляді провести жоден процес неможливо. Тому в подальшому визначати процеси ми будемо з деяким наближенням.
Оскільки при стисканні повітря зовнішніми силами виконувалася деяка робота, то повітря в балоні нагрілося і після припинення накачування воно почне охолоджуватися. Невеликими тепловими змінами об'єму скляного балона можна знехтувати і тоді другим процесом у балоні буде ізохорне охолодження газу (на графіку ділянка 2 ÷ 3). Як тільки температура повітря у балоні стане дорівнювати температурі навколишнього середовища (кімнатній), охолодження припиниться.
Тиск повітря в балоні можна виразити так:
![]() ,
(18.1)
,
(18.1)
де P1 - атмосферний тиск повітря, P1=gh1 - тиск, який показує рідинний манометр; h1 - різниця рівнів рідини в колінах манометра.
Третій процес, що виконується в роботі, є адіабатне розширення повітря до об'єму V3. Це основний процес в роботі, тому дуже важливо провести його правильно.
Адіабатний процес - це процес, що проходить без теплообміну з навколишнім середовищем. Він буде ідеальним, якщо стінки балона з газом будуть абсолютно нетеплопровідними. Якщо стінки пропускають тепло, то за час розширення відбудеться частковий теплообмін. Чим коротший проміжок часу розширення, тим меншим буде теплообмін. Очевидно, можна так швидко провести процес розширення, що теплообміном можна знехтувати і тоді цей процес можна вважати адіабатним. Звідси: якість проведення третього процесу залежить від швидкості - чим швидше він буде проведений, тим процес буде якіснішим, тобто більш наближеним до адіабатного.
Отже, швидко проведемо розширення повітря в балоні, максимально відтягнувши рукоятку пружинного клапану 4. Оптимальний час розширення 1÷2 секунди. Па графіку - це ділянка 3÷4. У кінці процесу тиск падає до атмосферного P1, об'єм стане дорівнювати V3, а температура T3 стане нижчою за кімнатну.
Рівняння адіабатного процесу , що відбувся у нашому випадку, може бути записаним у такому вигляді:
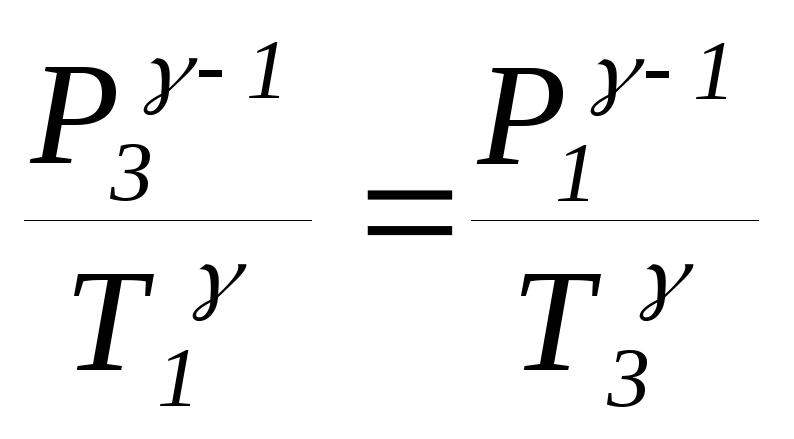 (18.2)
(18.2)
Після завершення третього процесу розпочнеться четвертий - ізохорне нагрівання повітря (ділянка 4÷5 на графіку). Закінчується він при досягненні повітрям температури T1. При цьому тиск повітря в балоні буде дорівнювати
![]() ,
(18.3)
,
(18.3)
де P2=gh2 - тиск, який показує манометр. Рівняння останнього ізохорного процесу має вигляд
![]() .
(18.4)
.
(18.4)
Об'єднаємо рівняння (18.2) й (18.4). виключивши з них температури Т1 і Т3
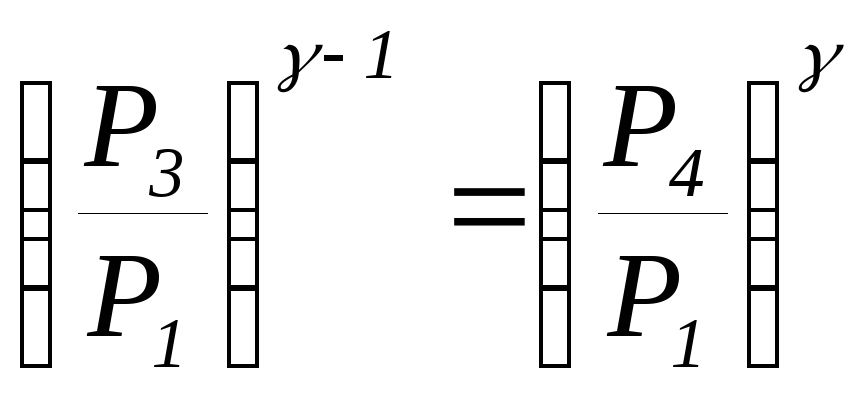 .
.
Підставивши сюди P3 і P4 з рівнянь (18.1) і (18.3), одержимо
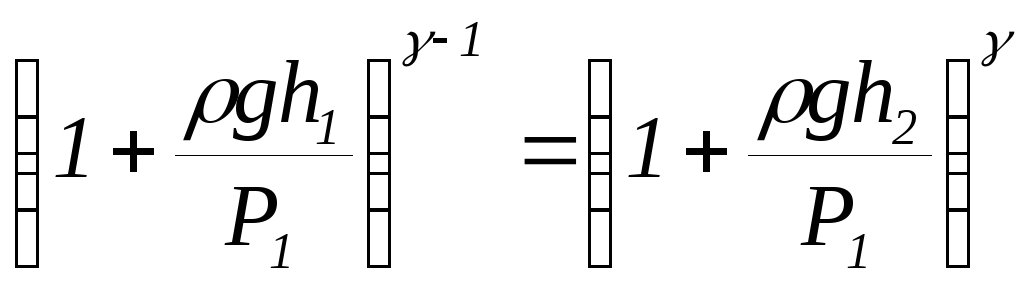 .
(18.5)
.
(18.5)
Застосувавши до виразу (18.5) формулу бінома Ньютона і враховуючи, що gh1<< P1 і gh2<< P2 одержимо
![]()
![]()
Звідки
![]() .
(18.6)
.
(18.6)
Формула (18.6) є розрахунковою.
18.3 Порядок виконання роботи
1. Опустите до упору рукоятку штока (7).
2. Відтягнути рукоятку пружинного клапану (4), коли рівні рідини в манометрі зрівняються, відпустити рукоятку.
3. Підняти рукоятку штока (7) і зафіксувати її стопором (6).
4. Через 2 хвилини записати значення різниці рівнів рідини в манометрі – h1.
5. Відтягнути на 0,5 с рукоятку пружинного клапану (4).
6. Через 2 хвилини записати значення рівнів рідини в манометрі – h2.
7. Повторити дослід по пунктам 1 ÷ 6 ще два рази, значення рівнів записати в таблицю 18.1.
8. Визначити для значень h1 та h2 за формулою (18.6).
Таблиця 18.1
|
№ |
h1 |
h2 |
|
|
|
1 |
|
|
|
|
|
2 |
|
|
|
|
|
3 |
|
|
|
-
Визначити відносну похибку за формулою:
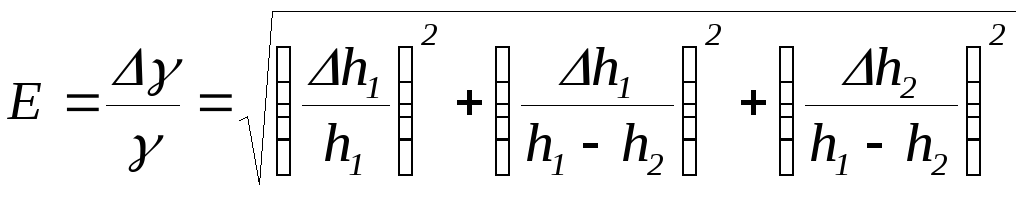
При цьому величину h1 та h2 взяти для будь-якого з дослідів, а півширину довірчого інтервалу h1 = h2 знайти за формулою для одноразового вимірювання. Для шкали манометра = 1 мм, = 0,5 мм.
10. Знайти півширину довірчого інтервалу за формулою
![]()
11.
Обчислити величину
для
повітря за формулою
![]() та порівняти її з одержаною в досліді
величиною
та порівняти її з одержаною в досліді
величиною
![]() .
i
для двохатомного газу = 5, для 3-х = 6.
.
i
для двохатомного газу = 5, для 3-х = 6.
12. Обчисліть молярні і питомі теплоємності повітря при сталому об'ємі і сталому тиску.
![]()
![]()
![]()
![]() ,
,
де
![]() – показник адіабати, значення якого
одержане в лабораторній роботі;
R=8,31
Дж/(моль-К); M=29
10-3
кг/моль.
– показник адіабати, значення якого
одержане в лабораторній роботі;
R=8,31
Дж/(моль-К); M=29
10-3
кг/моль.
Контрольні запитання
-
Назвіть ізопроцеси в ідеальних газах. Дайте пояснення, чим вони відрізняються?
-
Сформулюйте та запишіть перший закон термодинаміки.
-
Запишіть перший закон термодинаміки для кожного ізопроцесу.
-
Дати визначення числа ступенів свободи.
-
За якою формулою визначається середнє значення кінетичної енергії поступального руху молекули?
-
Яка середня енергія припадає на один ступінь свободи?
-
За якою формулою визначається внутрішня енергія ідеального газу?
-
Дайте визначення теплоємності, питомої та молярної теплоємності.
-
Чому теплоємність при сталому тиску більша теплоємності при сталому об’ємі?
-
Як пов’язані теплоємність при сталому тиску та теплоємність при сталому об’ємі з числом ступенів свободи?
-
Запишіть формулу для обчислення величин співвідношення Cp/Cv через число ступенів свободи.
Інструкція складена старшим викладачем кафедри
фізики Денисовой О.І.
Відредагував доцент кафедри фізики Золотаревський І. В.
Затверджена на засіданні кафедри фізики,
протокол № 3 від 01.12.2008 р.
19 LABORATORY WORK № 7. DETERMINATION OF THE RATIO OF THE SPECIFIC HEAT Cp/Cv FOR GASES
THE AIM: To determine a ratio of the specific heat at constant pressure to specific heat at constant volume
INSTRUMENTATION AND APPLIANCES: the device for a ratio of specific heat Cp/Cv determination, manometer.
19.1 The description of the device and method of measurements
The device consists of a glass sphere of 12 liters volume, goffered tube, rod, handle of the spring valve, stopper, handle of a rod, water manometer.
The sphere can incorporate to an atmosphere with the help of the spring valve. It is possible to increase or to reduce volume of gas in a sphere it is possible at the expense of a stretching or compression goffered tube at lowering or rise of the handle of a rod. The stopper is used for fixation of a rod in the top position. The difference between the pressure of air inside and outside of the sphere is measured by water manometer.
If to move a rod downwards up to the stop, and then quickly delay downwards spring valve, the pressure of air inside a sphere becomes equal to atmospheric pressure outside of a sphere. At movement of a rod upwards up to a stop there is action of force on air in a sphere. Thus the external force makes above air some certain work. As a result the internal energy of air in a sphere is increased, and its temperature becomes above room one.
The compression of air occurs as adiabatic process. During some time (approximately two minutes) occur reductions of temperature of air in a sphere up to a room temperature.
Thus the difference between levels of a liquid in manometer is decreased. It is possible to consider reduction of temperature of air in a sphere as the process at a constant volume.
If to pull down handle of the spring valve within 0,5 seconds, the part of air will exhaust for an atmosphere. Thus, air, which has remained in a sphere, does some work on expansion of gas.
Thus, the internal energy of air which has stayed in a sphere, decreases, and its temperature becomes lower than a room temperature, and its pressure will be equal to the atmospheric pressure. It is possible to consider expansion of air as adiabatic process. Temperature of air in a sphere will be raised up to a room temperature in two minutes. As a result, the pressure in a sphere will increase, and the difference of levels of a liquid in manometer will increase.
19.2 Experimental part
1. Pull down to stopper the handle of a rod.
2. Pull down to stopper the handle of the spring valve till the levels of a liquid in manometer become equal, and release the handle.
3. Lift the handle of a rod and fix by its stopper.
4. In two minutes you have to write down value of a difference of levels of a liquid in manometer in your experimental table - h1.
5. Pull down handle of the spring valve and keep it in this position within 0.5 seconds.
6. In two minutes you have to write down value of a difference of levels of a liquid in manometer into your experimental table - h2 .
7. Repeat researches on 1 ÷ 6 two times more.
8. Calculate the experimental value of ratio Cp/Cv by means of the formula
![]() .
.
|
№ |
h1, mm |
h2, mm |
|
|
|
1 |
|
|
|
|
|
2 |
|
|
|
|
|
3 |
|
|
|
|
9. Calculate a relative mistake by means of the formula: