Материал: 69.24
До умовно асептичних відносяться виробництва, у готовому продукті яких допускається деяка концентрація контамінантів:
· білково-вітамінні концентрати, кормові препарати амінокислот, вітамінів. До строго асептичних відносять виробництва, на всіх етапах яких повинна бути забезпечена найвищий ступінь захищеності від сторонньої мікрофлори й продуктів її життєдіяльності. Це виробництво антибіотиків, вакцин, кро-
возамінників і т.д.
Усередині груп виробництва можуть бути згруповані по виду використовуваних мікроорганізмів: аеробних або анаеробних; по виду процесу їхнього культивування - періодичний або безперервний.
Залежно від мети проведення мікробіологічні процеси можна розділити на наступні групи:
·культивування - цільовим продуктом є сама біомаса мікроорганізмів або її компоненти (виробництво кормових або її компонентів, вакцини й ін.)
·біосинтез позаклітинних продуктів метаболізму(виробництво спирту, оцтової й лимонної кислот, амінокислот, антибіотиків, экзоферментов і ін.);
·процеси, у яких мікроорганізми і їхні компоненти використовуються як біокаталізатори для здійснення тонких хімічних реакцій(виробництво 6- амінопеніцилланової кислоти, гормональних препаратів);
·виборча утилізація деяких компонентів із суміші (депарафінізація нафти, біологічне очищення стічних вод);
·мікробіологічне видобування коштовних елементів з руд (біометалургія).
Реалізація біотехнологічних виробництв проводиться на технологічних комплексів, які створюються, для виробництва певного продукту шляхом мікробіологічного синтезу, що носять назву – біотехнологічна система
(БТС).
·I ступінь - відповідає структурі біотехнологічного заводу, комбінату;
·II ступінь - технологічні ділянки, цехи, що включають декілька взаємоз- в'язаних технологічних процесів та апаратів - стадія підготовки поживного середовища, стадія ферментаціі;
·ІІI ступінь - апаратурна схема окремої технологічної стадії, ділянки.
·IV ступінь - це технологічні елементи БТС(апарати), де протікають типові технологічні процеси:
а) механічні - подріблення, різання та інші; б) гідродинамічні - перемішування,
змішування, розділення; в) теплові - нагрів та охолодження,
випаровування, сушіння; г) масообмінні - абсорбція, екстракція;
д) процеси хімічних та біохімічних перетворень; е) мікробіологічні - розмноження культур м/о.
·V ступінь (найнижчій) – це рівень біологічного агенту(мікроорганізмів) на якому протікають хімічні, біохімічні реакції за рахунок процесів фер-
31
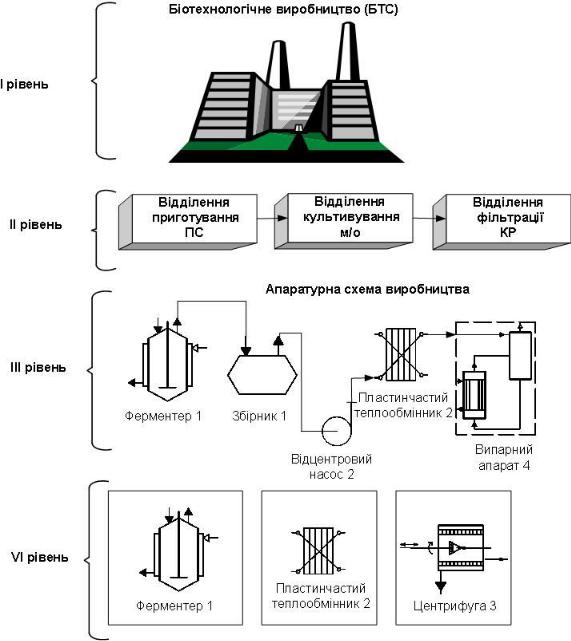
ментативного каталізу компонентів поживного середовища і перетворення їх в клітинах в біологічно активні речовини(БАР) – ферменти, амінокислоти, вітаміни, антибіотики.
Рис.2.1. Ієрархічна структура біотехнологічної системи
2.1.Узагальнена технологічна схема процесу мікробіологічного синтезу
Вихідним і основним елементом біотехнологічного процесу є продуцент. Потенційні можливості штаму-продуцента визначають економічні показ-
ники біотехнологічної схеми в цілому.
32
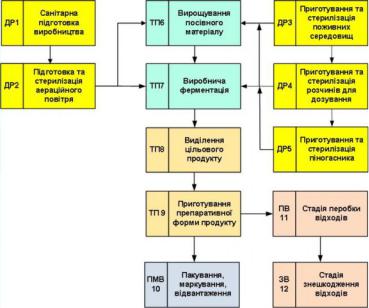
Основною стадією процесів мікробного синтезу є стадія культивування штаму-продуцента (ферментація), на якій відбувається біосинтез цільового продукту - біомаси або метаболітів.
Рис.2.1. Технологічна схема біотехнологічного виробництва (загальний вигляд)
Стадія культивування продуцента може бути охарактеризована якісно й кількісно. Кількісна характеристика — об'ємна продуктивність — виражається в грамах (кілограмах) цільового продукту на 1 м3 ферментаційного устаткування за 1 год і служить загальним критерієм ефективності процесу, що визначає собівартість цільового продукту, G, кг/(м3·год).
На наступних стадіях виробництва біопрепаратів не відбувається приріст цільового продукту, а проводиться його обробка. Мета цих стадій — одержан-
ня необхідної товарної форми препарату. На цих стадіях необхідно максима-
льно зберегти цільовий продукт.
Основне завдання вдосконалювання кінцевих стадій виробництва біопрепаратів — це скорочення втрат цільового продукту при виділенні з культуральної рідини.
Основна маса товарної продукції випускається промисловістю у двох формах :
·сухий продукт (порошок, гранули, дрібнодисперсні частки – вміст сухих речовин 90 -96 % );
·рідкий продукт (концентрат зі змістом сухої речовини до 50%).
[11]c. 498-517
Запитаня для самоперевірки
1.Як класифікуються мікробіологічні виробництва ?
2.Які основні стадії біотехнологічного процесу?
33
3. ТИПИ РЕГЛАМЕНТІВ ВИРОБНИЦТВА, ЇХ СКЛАД
Невід’ємною частиною технологічного розділу проекту виробництва є опис технології, представлення інформації про сировину та матеріали, креслення та інше. Основним документом технологічного розділу проектної розробки де представлена ця інформація є регламент виробництва. Регламенти виробництва є конфіденційним документом, який враховує специфічні особливості, як технології, так і специфіку підприємства.
З метою гармонізації вимог, що діють у Європейському співтоваристві для врахування принципів і правилGMP, вимог ВООЗ та вимог країн ЄС виникла необхідність у перегляді нормативно-технічної документації, що діє в Україні з метою її гармонізації з вимогами вищевказаних документів та Директив ЄС, які регламентують вимоги до реєстраційної документації на лікарські засоби. Результатом цієї роботи було створення галузевого нормативного документа (ГНД) “Продукція медичної та мікробіологічної промисловості. Зміст, порядок розробки, узгодження та затвердження”(ГСТУ 64 01-98)
В рамках діючих документів діють такі терміни та визначення.
Регламент - нормативний документ, що встановлює вимоги до технологічних процесів, технологічного обладнання і приміщень, пов’язаних з якісним виготовленням продукції при дотриманні умов охорони праці та нав-
колишнього середовища. |
|
|
|
|
|
|
|
|||
|
На початку ГНД дається визначення галузі використання нормативного |
|||||||||
документа у сукупності комплекту НТД. |
|
|
|
|
|
|||||
|
Вперше в Україні у обіг НТД включені два типи регламентів, так як ви- |
|||||||||
моги |
до |
технології |
виробництва |
включаються |
у |
два |
регламент- |
|||
технологічний, |
що |
стосується |
виробництва |
конкретного |
найменування |
|||||
продукції, та технічний, що містить вимоги до комплексу обладнання та його |
||||||||||
безпечної експлуатації на даній виробничій дільниці, |
у даному цеху. Введення |
|||||||||
у обіг двох типів регламентів значно спрощує роботу підприємств, які на ідентичному обладнанні випускають ряд однакових за формою але різних за
призначенням препаратів. |
|
|
|
Вимоги |
цього |
ГНД є |
обов’язковими для підприємств, установ і |
організацій, а |
також |
громадян- |
суб’єктів підприємницької діяльності, |
пов’язаних із виготовленням лікарських засобів(крім імунобіологічних та радіофармацевтичних), що здійснюють свою діяльність на території України незалежно від форми власності та підпорядкованості.
Цей нормативний документ може використовуватися підприємствами та громадянами України для підготовки регламентів на виробництво ветеринарних засобів, харчових домішок та іншої продукції.
Біотехнологічна продукція виготовляється за цим ГНД.
В цьому ГНД прийняті такі скорочення: ТТР - технологічний тимчасовий регламент; ТПР - технологічний промисловий регламент; ТхР – технічний регламент;
34
Загальні положення. Виготовлення продукції з метою реалізації чи проведення клінічних випробувань повинно здійснюватися тільки на основіза твердженого технологічного регламенту при наявності на виробництвіза твердженого технічного регламенту. Технологічний регламент обумовлює технологічні умови виробництва конкретного лікарського засобу за умови
наявності технічного регламенту. |
|
|
|
|
||
У |
ГНД |
визначені |
пріоритети |
дії |
технічного |
регламенту, і він |
поширюється на: підготовку виробничих (лабораторних, дослідно-промислових і промислових) приміщень і персоналу до роботи; створення необхідних санітарно-гігієнічних умов виробництва; виконання заходів, пов’язаних з охороною праці, технікою безпеки, пожежною безпекою, охороною навколишнього середовища; кваліфіковану ефективну експлуатацію обладнання, що
гарантує одержання лікарських засобів відповідно до вимог аналітичної нормативної документації. Технічний регламент розробляється для лабораторних, модельних і стендових установок, дослідних і дослідно-промислових дільниць, промислових установок, цехів, дільниць. Термін дії ТхР - сім років.
Технологічні регламенти поділяються на 2 категорії: технологічні тимчасові регламенти (ТТР), технологічні промислові регламенти (ТПР).
Згідно тимчасових технологічних регламентів(ТТР) виконуються лабораторні та дослідно-промислові роботи, виготовлення дослідних партій.
За тимчасовим технологічним регламентом (ТТР) дозволяється реєструвати і виготовляти разові та промислові серії для оптової реалізації у торгівельній мережі при невеликих обсягах виготовлення продукції, які встановлюються окремим рішенням Технологічної комісії Державної служби лікарських засобів і виробів медичного призначення(при наявності умов у виробника, що гарантують якість продукції та безпечність робіт по виготовленню).
Термін дії ТТР - до трьох років.
За технологічними промисловими регламентами (ТПР) дозволяється серійне виготовлення, вони є основним документом на реєстрацію препарату в Україні, для постановки продукції на виробництво.
Термін дії ТПР - п’ять років.
Вимоги до змісту регламентів. Та значна увага, що приділяється цьому розділу обумовлена тим, що деякі розділи регламенту є складовими, або ідентичні розділам кваліфікаційних робіт (курсових та дипломних проектів). У технологічному регламенті, і відповідно курсових та дипломних проектах, представлені такі розділи:
1.Характеристика готової продукції
2.Схеми виробництва та технологічний процес:
3.Схеми виробництва;
4.Характеристика сировини, матеріалів і напівфабрикатів;
5.Опис стадій технологічного процесу;
6. Матеріальний баланс
35