Материал: Задачи по биохимии
Андрогены(
тестостерон , дигидротестостерон) 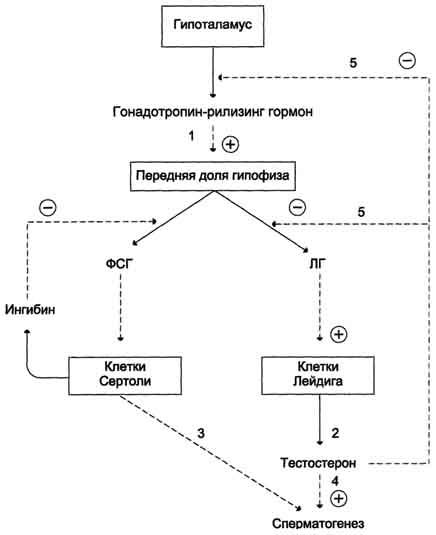
Синтезируются в семенниках, частично в яичках и надпочечниках. Стероидная природа, образуются из холестерола. Механизм действия: по внутриклеточно-ядерному Учавствуют в:
-
Половой дифференцировке и формировании вторичных половых признаков
-
Сперматогенезе
-
Характерном для мужчин поведении
-
Росте скелетно-мышечной системы
Индукции
синтеза ферментов тканевого дыхания и
липолиза
Гипофункция:
Евнухоидизм, ожирение, ложная гинекомастия,
крипторхизм (недоразвитие наружных
половых органов).
Эстрогены(эстрадиол,эстриол)
Прогестины( прогестерон)
синтезируются
в яичниках, желтом пятне, а также плаценте,
коре надпочечников и небольшое количество
в семенниках.
Стероидная
природа,
синтез заверш-ся ароматизацией 1 кольца
с помощью аромотазы.
Механизм
действия:
по внутриклеточно-ядерному
Регулируют: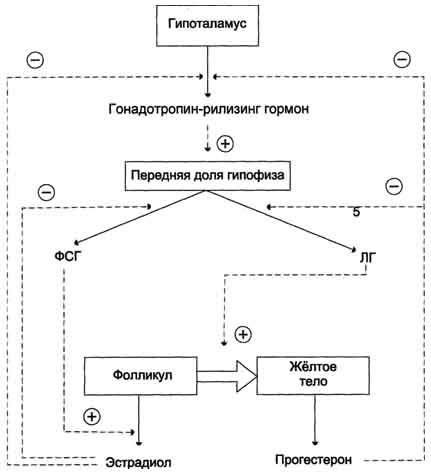
-
Половую дифференцировку
-
Формирование вторичных половых признаков
-
Овуляцию
-
Рост и развитие хрящей
-
Синтез белков и ферментов гликолиза, ПФП, липогенеза.
Гиперфункция прогестерона: Аменорея, увеличение молочных желез за счет из отечности, повышение либидо. Гипофункция прогестерона: Дисменорея, уменьшение массы молочных желез, бесплодие.
92. Белки крови: общая характеристика, роль, отдельные представители. Белки острой фазы воспаления. Парапротеины. Из 9-10% сухого остатка плазмы крови на долю белков приходится 6,5-8,5%. Белки плазмы крови: альбумин(40-50г/л), глобулины(20-30г/л), фибриноген(2-4г/л).Роль белков плазмы крови: поддержание онкотического давления(за счет альбуминов); поддержание вязкости крови; участие в сверывающей системе крови; поддержание рН крови; поддержание иммунитета; поддержание уровня катионов в крови; резерв аминокислот; транспортная функция-перенос питательных веществ, метаболитов, гормонов, лекарственных веществ. отдельные представители: глобулины, α2-макроглобулин, α1-антитрипсин, гаптоглобин, трансферрин, церулоплазмин, криоглобулин, С-реактивный белок, интерфероны. Белки острой фазы синтезируются в печени. Синтез белков острой фазы воспаления в печени стимулируют: 1). ИЛ-6, 2); ИЛ-1 и сходные с ним по действию (ИЛ-1 а, ИЛ-1Р, факторы некроза опухолей ФНО-ОС и ФНО-Р); 3). Глюкокортикоиды; 4). Факторы роста (инсулин, факторы роста гепатоцитов, фибробластов, тромбоцитов). Выделяют 5 групп белков острой фазы: 1. К «главным» белкам острой фазы у человека относят С-реактивный белок (СРВ) и амилоидный А белок сыворотки крови. Уровень этих белков возрастает при повреждении очень быстро (в первые 6-8 часов) и значительно (в 20-100 раз, в отдельных случаях - в 1000 раз). 2. Белки, концентрация которых при воспалении может увеличиваться в 2-5 раз в течение 24 часов. Это кислый α1-гликопротеид, α1-антитрипсин, фибриноген, гаптоглобин. 3. Белки, концентрация которых при воспалении или не изменяется или повышается незначительно (на 20-60% от исходного). Это церулоплазмин, С3-компонент комплемента. 4. Белки, участвующие в острой фазе воспаления, концентрация которых, как правило, остается в пределах нормы. Это α1-макроглобулин, гемопексин, амилоидный Р белок сыворотки крови, иммуноглобулины. 5. Белки, концентрация которых при воспалении может снижаться на 30-60%. Это альбумин, трансферрин, ЛПВП, преальбумин. Уменьшение концентрации отдельных белков в острой фазе воспаления может быть обусловлено снижением синтеза, увеличением потребления, либо изменением их распределения в организме.
парапротеины
общее название белков, образующихся в организме при некоторых патологических состояниях; обычно П. называют иммуноглобулины, продуцируемые патологическим клоном иммунокомпетентных клеток при миеломной болезни
93. Небелковыекомпоненты плазмы крови. Остаточный азот плазмы крови. Понятие азотемии и причины ее возникновения.
Органические небелковые соединения плазмы делятся на две группы.I группа - азотсодержащие небелковые компоненты. В состав небелкового азота крови входит азот промежуточных и конечных продуктов обмена простых и сложных белков. Раньше небелковый азот называли остаточный азот (остается после осаждения белков): 1) азот мочевины (50 %);2) азот аминокислот (25 %);3) низкомолекулярные пептиды;4) креатин;5) креатинин;6) билирубин;7) индикан;8) некоторые другие азотсодержащие вещества. При некоторых заболеваниях почек, а также при патологии, сопровождающейся массивным разрушением белков (например, тяжелые ожоги), может повышаться небелковый азот крови, т. е. наблюдается азотемия. Однако наиболее часто нарушается не общее содержание небелкового азота в крови, а соотношение между отдельными компонентами небелкового азота. Поэтому сейчас в плазме определяют азот отдельных компонентов. В понятие "остаточный азот" включают и низкомолекулярные пептиды. Среди низкомолекулярных пептидов есть много пептидов, обладающих высокой биологической активностью (например, гормоны пептидной природы). II группа - безазотистые органические вещества. К безазотистым (не содержат азот) органическим веществам плазмы крови относятся: 1) углеводы, липиды и продукты их метаболизма (глюкоза, ПВК, лактат, кетоновые тела, жирные кислоты, холестерин и его эфиры и др.); 2) минеральные вещества кров. Азотемия – это нахождение в крови повышенного содержания азотистых продуктов переработки белка, сигнализирующее о развитии почечной недостаточности.Азотемию по причинам возникновения выделяют: ренальную, постренальную и преренальную. Рассмотрим основные факторы появления различных ее видов: Ренальная – развивается при остром тубулярном некрозе, остром гломерулонефрите (поражении паренхимы почек), острой почечной недостаточности, вследствие интоксикации химическими средствами, токсинами, нефротоксическими ядами и т. д. При данном виде азотемии может наблюдаться возникновение уремии; Преренальная – возникает из-за уменьшения уровня циркулирующей крови (при обезвоживании, сильной кровопотере и т. д.), шока, развития сердечной недостаточности, кровоизлияния; Постренальная – причинами азотемии этого типа являются любые механические преграды, препятствующие оттоку мочи: камни в мочеточнике, опухоли сжимающие уретру, гиперплазия простаты, беременность (увеличенная матка оказывает давление на мочеточник).
94. Ферменты сыворотки крови: их происхождение и значение для диагностики заболеваний.
|
Название фермента |
Происхождение |
Повышение |
Понижение |
|
Аминотрансферазы (трансаминазы) Аланинаминотрансфераза (АлАТ) - фермент, который вырабатывается клетками печени и поступает в кровь, при их повреждении. Аспартатаминотрансфераза (AсАT) - попадает в кровь при повреждении клеток печени, мышц (в том числе сердечной мышцы) и головного мозга |
трансферазы |
- при инфаркте миокарда (особенно повышена концентрация ACT); - при остром вирусном гепатите (концентрация АЛТ выше, чем ACT); - при циррозе печени (концентрация ACT выше, чем АЛТ); - при опухолях печени; - при мышечной дистрофии и дерматомиозите (повышается содержание ACT).
|
- недостаточность витамина В6 (пиридоксина); - вследствие повторных процедур гемодиализа; - почечная недостаточность; - беременность |
|
Гамма-глутамилтранспептидаза (ГГТП) Фермент наиболее активен в печени, почках, поджелудочной железе.
|
пептидаза |
- при заболеваниях печени (особенно алкогольном гепатите); - при застойной сердечной недостаточности; - при панкреатитах и опухолях поджелудочной железы; - изредка — при инфаркте миокарда.
|
|
|
Амилаза Амилаза образуется в поджелудочной железе и слюнных железах.
|
гидролаза |
- острый панкреатит и хронический панкреатит; - киста поджелудочной железы; - закупорка протока поджелудочной железы, или его спазм; - эпидемический паротит; - иногда как следствие почечной недостаточности, прободений язвы желудка или двенадцатиперстной кишки и при диабетическом ацидозе.
|
-при гепатитах; -при недостаточности функции поджелудочной железы; -при токсикозе беременных |
|
Креатинфосфокиназа (КФК)
|
трансфераза |
-при различных повреждениях мышц (инфаркт миокарда, травмы); -при мышечной дистрофии; -при миозите и сильной мышечной нагрузке (бег); -при пониженной функции щитовидной железы; -при инсульте |
отмечается у людей, ведущих очень малоподвижный образ жизни, со сниженной мышечной массой, и большого клинического значения не имеет |
|
Лактатдегидрогеназа (ЛДГ)
|
оксидоредуктаза |
отмечается при любом повреждении тканей, содержащих АДГ в большом количестве (сердце, скелетные мышцы, печень, эритроциты)
|
|
|
Липаза — фермент, вырабатывающийся в поджелудочной железе и расщепляющий жиры.В норме содержание липазы в циркулирующей крови очень низкое.
|
эстераза |
острой панкреатит, обострение хронического панкреатита или при закупорке протока поджелудочной железы.
|
|
|
Щелочная фосфатаза
|
гидролаза |
- при закупорке желчных протоков или их воспалении и иногда при застойной (холестатической) форме гепатита; - при повреждении клеток печени вирусом гепатита, циррозе печени, раке печени, рахите, остеомаляции, опухолях костей, болезни Педжета, саркоидозе, повышенной функции паращитовидных желез. - при заживлении переломов костей, при заболеваниях кишечника, у беременных женщин и у детей при нормальном росте костей повышение щелочной фосфатазы незначительное.
|
при гипотиреозе и при замедленном росте у детей |
|
Кислая фосфатаза
|
гидролаза |
у мужчин с большой долей вероятности свидетельствует о раке простаты. Умеренное повышение активности кислой фосфатазы типично для простатитов, особенно после некоторых диагностических и лечебных манипуляций в области предстательной железы |
|
|
Билирубин
|
Продукт распада гемоглобина |
Непрямой билирубин. происходит при гемолитических анемиях или усиленном распаде эритроцитов по другой причине, а также при отсутствии или дефиците некоторых ферментов Прямой и общий. у здоровых людей, длительно соблюдающих низкокалорийную диету, или при голодании более 2 дней.
|
|
95. Буферные системы крови. Нарушения кислотно-щелочного равновесия крови.
Гидрокарбонатный буфер. В крови существует целый ряд буферных систем. Рассмотрим гидрокарбонатную систему. Она состоит из относительно слабой угольной кислоты, образующей при гидратации СО2 сопряженногооснования - гидрокарбоната СО2 +Н2О - Н2СО3 - Н+ + НСО3¯ Уравнение Гендерсона-Гассельбаха для этой реакции имеет вид : РН = рК' + lg При ионной силе плазмы рК' составляет 6,1. Казалось бы, при таком различии между рК ' и рН крови (7,4) емкость гидрокарбонатного буфера должна быть невелика. Однако, на самом деле, гидрокарбонатная система играет большую роль в создании общей буферной емкости крови, т.к. буферный эффект этой системы существенно увеличивается благодаря ее тесной связи с дыханием. Механизмы, направленные на поддержание напряжения СО2 в артериальной крови способствуют созданию высокой концентрации НСО3¯ в плазме. Поддерживая напряжение СО2 в крови, дыхательная система обеспечивает высокое содержание буферных соединений. Фосфатный буфер Фосфатная буферная система образована неорганическими фосфатами в крови. Состоит из слабой кислоты Н2РО4¯ сопряженного основания НРО2¯. В основе ее действия лежит КЩР : Н2РО4¯ - Н+ + НРО4¯ . Эта буферная система способна сопротивляться изменению рН в интервале 6,2- 8,2, т.е. обеспечивает значительную долю буферной емкости крови. рК' фосфатного буфера (6,8). сравнительно близка к рН крови, однако, емкость данного буфера невелика в связи с низким содержанием фосфата в крови. Белковый буфер Особенное значение гемоглобиновой буферной системы заключается в том, что кислотность гемоглобина зависит от степени его оксигенации. Эта зависимость отражена на рис.2 На этом рисунке приведены буферные кривые недиффундирующих буферных систем эритроцитов, красная кривая соответствует оксигенированному, а черная - дезоксигенированному состоянию гемоглобина. Видно, что при нормальных пределах рН оксигемоглобина является более сильной кислотой, чем дезоксигемоглобин. Такая разница обусловлена влиянием О2 , связанного с Fe, на сродство ближайших имидазольных групп гистидина к Н+. Благодаря этому гемоглобин, освобождаясь в тканях от О2 , приобретает большую способность к связыванию ионов Н+, а в венозной крови в результате выделения СО2 тканями происходит накопление в крови этих ионов. При поглощении О2 в легких происходят обратные процессы. Т.о. обмен О2 потенциирует буферный эффект гемоглобина Буферные основания Буферные свойства крови обусловлены анионами всех слабых кислот, важнейшими из них являются гидрокарбонаты и анионные группы белков. Все эти анионы, вместе взятые, называются буферными основаниями. На рис.3 приведены концентрации различных ионов в плазме, эритроцитах и цельной крови. Высота различных столбиков пропорциональна содержанию ионов. Из рисунка видно, что в плазме бо'льшая часть буферных оснований приходиться на долю ионов НСО3 ¯ , а в эритроцитах на долю анионных групп белков. Содержание ВВ ( буферных оснований ) в артериальной крови составляет примерно 48 ммоль/ л. Очень важно, что эта величина не изменяется при сдвигах напряжения СО2 . Так, если последнее возрастает, образуются эквивалентные количества Н+ и НСО3¯ . Ионы Н+ почти полностью связываются протеинатами, переходящими при этом в недиссоциированную форму. В результате содержание протеинатов снижается настолько, насколько увеличивается концентрация гидрокарбонатов. Поскольку общее количество буферных оснований крови не зависит от Р(СО2); по величине ВВ можно судить о сдвигах КЩР, связанных с увеличением или уменьшением содержания кислот в крови.
Ацидоз и алкалоз При ряде патологических состояний в крови накапливаются такие большие количества кислот или оснований, что описанные выше регуляторные системы (буферные системы крови, дыхательная и выделительная системы) уже не могут поддерживать рН на постоянном уровне. В зависимости от того, в какую сторону изменяется реакция крови, различают 2 типа нарушений КЩР. Понижение рН крови по сравнению с нормальным уровнем (рН ‹ 7,37) называется ацидозом, а повышение (рН › 7,43) - алкалозом. Каждый из этих двух типов подразделяется еще на несколько разновидностей в зависимости от причины сдвига рН. Такие сдвиги могут наступать при изменениях вентиляции легких (поражения легких могут сопровождаться увеличением напряжения СО2 в крови, и гипервентиляции приводят к снижению этого напряжения. Подобные состояния называют дыхательным (респираторным) ацидозом или алкалозом.