Материал: Задачи по биохимии
77. Медицинские показания и правило проведения теста «сахарной нагрузки» (теста толерантности к глюкозе).
Проба на толерантность к глюкозе (Глюкозо-толерантный тест, ГТТ) - метод диагностики сахарного диабета. Основные показания к применению: диагностика сахарного диабета, ранее обнаруженные небольшие (сомнительные) увеличения содержания глюкозы, наличие факторов риска развития диабета - ожирение, атеросклероз, сердечно-сосудистые заболевания, наличие диабета у родственников. Проба на толерантность к глюкозе проводится для выявления сахарного диабета и скрытых нарушений обмена углеводов. Принцип теста заключается в измерении содержания глюкозы 2 раза - до нагрузки и через 2 часа. Нагрузка с глюкозой: 75 грамм безводной глюкозы растворить в 250-300 мл. воды и выпить в течение 3-5 минут на голодный желудок. Для детей количество глюкозы составляет 1,75 г глюкозы на 1 кг массы тела. Тесту предшествует ночное голодание в течение 8 часов (не более 14 часов), воду пить можно. Последний прием пищи вечером должен содержать 30-50 г углеводов. Показанием для проведения теста являются сомнительные результаты измерения глюкозы, случайно выявленные гипергликемия или глюкозурия, а также клинические признаки сахарного диабета при нормальном содержании глюкозы. Следует учитывать, что в случае, если диагноз "сахарный диабет" не вызывает сомнений, применение теста может привести к развитию гликемического шока. В случае проведения перорального глюкозотолерантного теста отправными являются следующие показатели (в капиллярной и в венозной крови): Нормальная толерантность к глюкозе характеризуется уровнем гликемии через 2 ч после нагрузки глюкозой < 7,8 ммоль/л (<140 мг/дл).
Увеличение содержания: Толерантность. Снижение всасывания глюкозы из ЖКТ (плоская кривая): заболевания кишечника (напр., целиакия, спру), болезнь Уипла, надпочечниковая недостаточность (напр. болезнь Аддисона, гипопитуитаризм), гипотиреоз. Повышенная секреция инсулина (длительная гипогликемия): опухоль или гиперплазия островковых клеток поджелудочной железы. Уменьшение содержания: Толерантность. Повышенное всасывание глюкозы из ЖКТ: гипертиреоз, гастрэктомия, гастроэнтеростомия, ваготомия, избыточное потребление глюкозы. Снижение утилизации глюкозы тканями: сахарный диабет, поражение ЦНС, гиперлипидемия, гемохроматоз, синдром Кушинга. Пониженное образование гликогена (повышенный гликогенолиз и глюконеогенез): тяжелые заболевания печени, болезнь Гирке, гипертиреоз, стресс, инфекции, феохромоцитома, беременность.
78. Адреналин - гормон мозгового вещества надпочечников: схема синтеза и названия ферментов. Механизм действия адреналина и его влияние на обмен веществ.
Осуществляется
в клетках мозгового слоя надпочечников
(80% всего адреналина), синтез норадреналина
(80%) происходит также в нервных синапсах.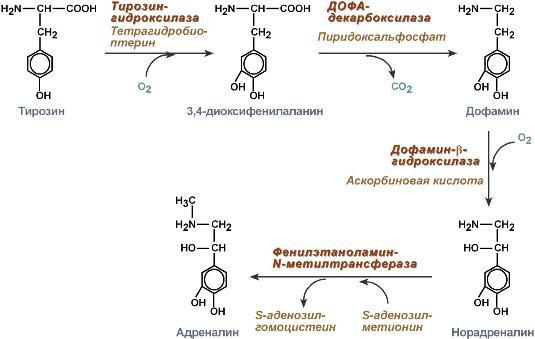
Активируют: стимуляция чревного нерва, стресс.
Уменьшают: гормоны щитовидной железы.
Механизм действия гормонов разный в зависимости от рецептора. Конечный эффект гормонов зависит от преобладания типа рецепторов на клетке и концентрации гормона в крови. Например, в жировой ткани при низких концентрациях адреналина более активны α2-адренорецепторы, при повышенных концентрациях (стресс) – стимулируются β1-, β2-, β3-адренорецепторы.
Аденилатциклазный механизм
-
при задействовании α2-адренорецепторов аденилатциклаза ингибируется,
-
при задействовании β1- и β2-адренорецепторов аденилатциклаза активируется.
Кальций-фосфолипидный механизм
-
при возбуждении α1-адренорецепторов.
Механизм действия и влияние на метаболизм
При возбуждении α1-адренорецепторов (печень, сердечно-сосудистая и мочеполовая системы): активация гликогенолиза, сокращение гладких мышц кровеносных сосудов и мочеполовой системы.
При возбуждении α2-адренорецепторов (жировая ткань, поджелудочная железа, почки): подавление липолиза (уменьшение стимуляции ТАГ-липазы), подавление секреции инсулина и секреции ренина.
При возбуждении β1-адренорецепторов (есть во всех тканях): активация липолиза, увеличение силы и частоты сокращений миокарда.
При возбуждении β2-адренорецепторов (есть во всех тканях): стимуляция гликогенолиза в печени и мышцах, и глюконеогенеза в печени, расслабление гладких мышц бронхов, кровеносных сосудов, мочеполовой системы и желудочно-кишечного тракта.
В целом катехоламины отвечают за биохимические реакции адаптации к острым стрессам, связанным с мышечной активностью – "борьба или бегство":
-
усиление липолиза и продукция жирных кислот в жировой ткани для мышечной активности,
-
гипергликемия за счет глюконеогенеза и гликогенолиза в печени для повышения устойчивости ЦНС,
-
стимуляция гликогенолиза в мышцах,
-
активация протеолиза в лимфоидной ткани для обеспечения глюконеогенеза субстратом (аминокислотами),
-
снижение анаболических процессов через уменьшение секреции инсулина.
Адаптация также прослеживается в физиологических реакциях:
-
мозг – усиление кровотока и стимуляция обмена глюкозы,
-
мышцы – усиление сократимости,
-
сердечно-сосудистая система – увеличение силы и частоты сокращений миокарда,
-
легкие – расширение бронхов, улучшение вентиляции и потребления кислорода,
-
кожа – снижение кровотока.
79. Гормоны коры надпочечников: классификация по химической структуре, схема основных этапов синтеза из холестерола, механизм действия.
В коре надпочечников образуются из холестерина стероидные гормоны: кортикостероиды (глюкокортикоиды и минералокортикоиды) и половые гомоны (женские и мужские).
Глюкокортикоиды: С21-стероиды, играют важную роль в адаптации к стрессу. Они оказывают разнообразные эффекты, но наиболее важный - стимуляция глюконеогенеза. Основной глюкокортикоид человека - кортизол. Осуществляется в сетчатой и пучковой зонах коры надпочечников. Активируют: АКТГ, обеспечивающий нарастание концентрации кортизола в утренние часы, к концу дня содержание кортизола снова снижается. Уменьшают: кортизол по механизму обратной отрицательной связи. Механизм действия – ЦИТОЗОЛЬНЫЙ. Гипофункция – болезнь Аддисона, гиперфункция – синдром Кушинга.
Минералокортикоиды: С21-стероиды, необходимы для поддержания уровня Na+ и К+. Самый активный гормон этого класса – альдостерон. Осуществляется в клубочковой зоне коры надпочечников. Образованный из холестерола прогестерон на пути к альдостерону подвергается последовательному окислению 11-гидроксилазой, 18-гидроксилазой и 21-гидроксилазой. Активируют: ангиотензин II, выделяемый при активации ренин-ангиотензиновой системы, повышение концентрации ионов калия в крови (связано с деполяризацией мембран, открытием кальциевых каналов и активацией аденилатциклазы). Механизм действия – ЦИТОЗОЛЬНЫЙ. Гипофункция не отмечена, гиперфункция – первичный альдостеронизм (синдром Конна) и вторичный альдостеронизм.
Андрогены - С19-стероиды. Эстрадиол — важнейший представитель эстрогенов. Подобно прогестерону он синтезируется в яичниках, а в период беременности также в плаценте. Эстрадиол регулирует менструальный цикл. Он стимулирует пролиферацию клеток слизистой матки, а также отвечает за развитие вторичных женских половых признаков (развитие молочных желез, характер жировых отложений и тому подобное). Тестостерон — наиболее важный представитель андрогенов (мужские половые гормоны). Он синтезируется клетками. Этот гормон отвечает также за развитие вторичных мужских половых признаков (развитие мускулатуры, волосяной покров и тому подобное).
Общим
предшественником кортикостероидов
служит холестерол. 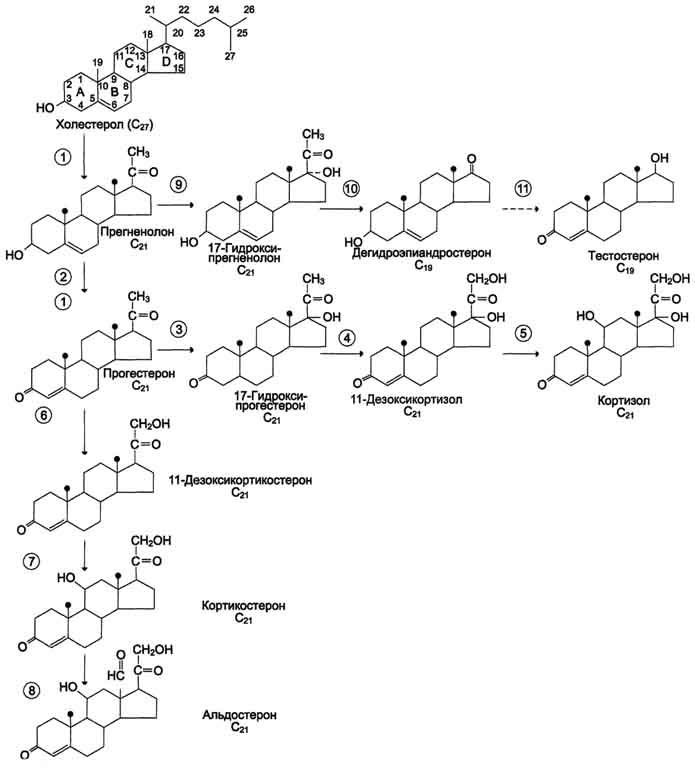
1 - превращение холестерола в прегненолон (гидроксилаза, отщепляющая боковую цепь);
2 - образование прогестерона (3-β-гидроксистероиддегидрогеназа);
3,4,5 - реакции синтеза кортизола (3-17-гидроксилаза, 4 – 21-гидроксилаза, 5 – 11-гидроксилаза);
6, 7, 8 - путь синтеза альдостерона (6 - 21-гидроксилаза, 7 - 11-гидроксилаза, 8 - 18-гидроксилаза, 18-гидроксидегидрогеназа);
9,10,11 - путь синтеза тестостерона (9 - 17-гидроксилаза, 10 - 17,20-лиаза, 11 - дегидрогеназа)
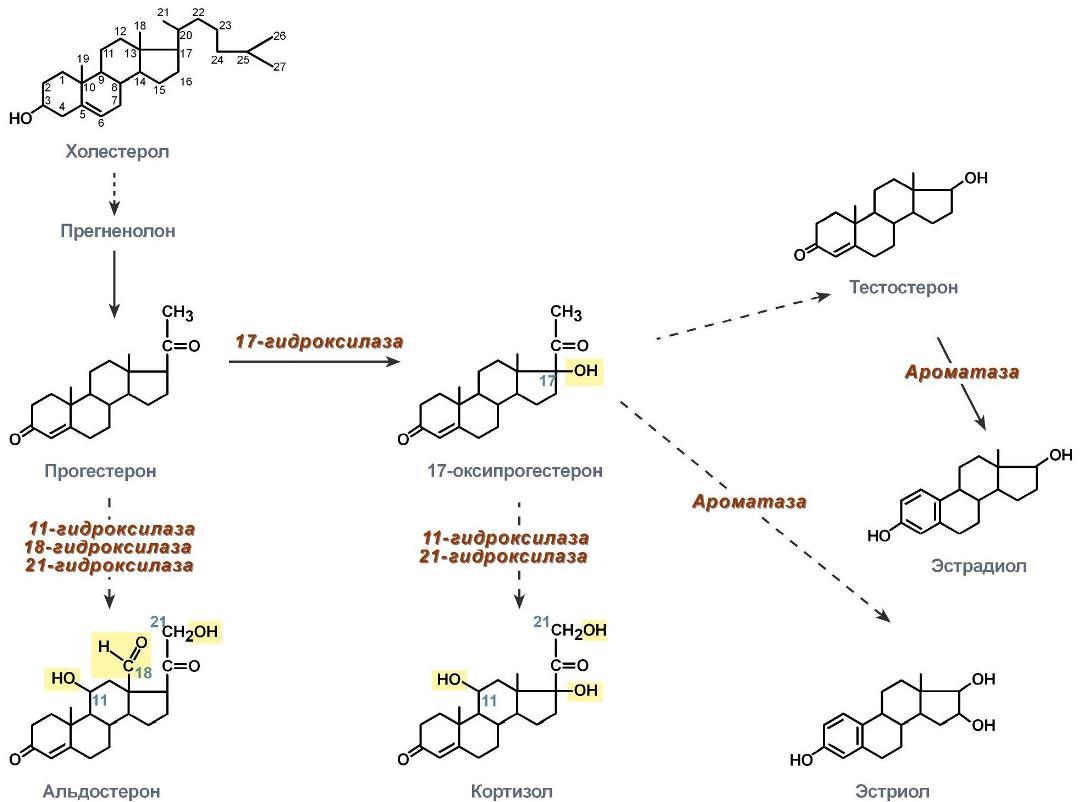
Ниже
схема синтеза отдельно стероидных
гормонов (картинка
большая, увеличить можно, кому не видно)
↓↓↓↓
80. Глюкокортикоиды: примеры гормонов, их роль в обмене веществ. Влияние глюкокортикоидов на мышечную и соединительную ткани. Биохимическое обоснование использования глюкокортикоидов, как иммунодепрессантов и противовоспалительных препаратов. (схемка синтеза в предыдущем вопросе)
Глюкокортикоиды
являются производными холестерола и
имеют стероидную природу. Основным
гормоном у человека является кортизол.
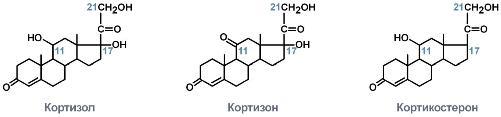
Синтез
осуществляется
в сетчатой и пучковой зонах коры
надпочечников. Образованный из холестерола
прогестерон подвергается
окислению 17-гидроксилазой по
17 атому углерода. После этого в действие
вступают еще два ключевых
фермента: 11-гидроксилаза и 21-гидроксилаза.
В конечном итоге образуется кортизол.
Активируют: АКТГ, обеспечивающий нарастание концентрации кортизола в утренние часы, к концу дня содержание кортизола снова снижается. Кроме этого, имеется нервная стимуляция секреции гормонов.
Уменьшают: кортизол по механизму обратной отрицательной связи.
Механизм действия – ЦИТОЗОЛЬНЫЙ.
Мишени и эффекты
Мишенью является мышечная, лимфоидная, эпителиальная (слизистые оболочки и кожа),жировая и костная ткани, печень.
Белковый обмен
-
значительное повышение катаболизма белков в мишеневых тканях. Однако в печени в целом стимулирует анаболизм белков.
-
стимуляция реакций трансаминирования через синтез аминотрансфераз, обеспечивающих удаление аминогрупп от аминокислот и получение углеродного скелета кетокислот,
Углеводный обмен
В целом вызывают повышение концентрации глюкозы крови:
-
усиление мощности глюконеогенеза из кетокислот за счет увеличения синтезафосфоенолпируват-карбоксикиназы,
-
увеличение синтеза гликогена в печени за счет активации фосфатаз и дефосфорилированиягликогенсинтазы.
-
снижение проницаемости мембран для глюкозы в инсулинзависимых тканях.
Липидный обмен
-
стимуляция липолиза в жировой ткани благодаря увеличению синтеза ТАГ-липазы, что усиливает эффект АКТГ, СТГ, глюкагона, катехоламинов, т.е. кортизол оказываетпермиссивное действие (англ. permission - позволение).
Водно-электролитный обмен
-
слабый минералокортикоидный эффект на канальцы почек вызывает реабсорбцию натрия и потерю калия,
-
потеря воды в результате подавления секреции вазопрессина и излишняя задержка натрия из-за увеличения активности ренин-ангиотензин-альдостероновой системы.
Противовоспалительное и иммунодепрессивное действие
-
увеличение перемещения лимфоцитов, моноцитов, эозинофилов и базофилов в лимфоидную ткань,
-
повышение уровня лейкоцитов в крови за счет их выброса из костного мозга и тканей,
-
подавление функций лейкоцитов и тканевых макрофагов через снижение синтезаэйкозаноидов посредством нарушения транскрипции ферментов фосфолипазы А2 ициклооксигеназы.
Другие эффекты
Повышает чувствительность бронхов и сосудов к катехоламинам, что обеспечивает нормальное функционирование сердечно-сосудистой и бронхолегочной систем.
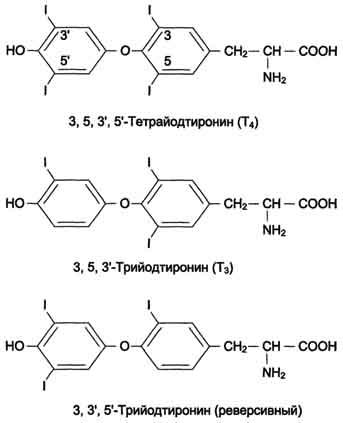
83,84. В щитовидной железе синтезируются гормоны - йодированные производные тирозина. Они объединены общим названием йодтиронины. К ним относят 3,5,3'-трийодтиронин (трийодтиронин, Т3) и 3,5,3',5'-тетрайодтиронин (Т4), или тироксин
Йодтиронины участвуют в регуляции многих процессов метаболизма, развития, клеточной дифференцировки, в регуляции экспрессии генов.
Заболевания, возникающие в результате нарушений синтеза, секреции и функций йодти-ронинов, - наиболее распространённые заболевания эндокринной системы.
1. Биосинтез йодтиронинов
Йодтиронины синтезируются в составе белка тиреоглобулина (Тг) (рис. 11-18) в фолликулах, которые представляют собой морфологическую и функциональную единицу щитовидной железы.
Тиреоглобулин - гликопротеин с молекулярной массой 660 кД, содержащий 115 остатков тирозина. 8-10% массы тиреоглобулина представлено углеводами. Содержание йодида в организме составляет 0,2-1%.
Тиреоглобулин синтезируется на рибосомах шероховатого ЭР в виде претиреоглобулина, затем переносится в цистерны ЭР, где происходит формирование вторичной и третичной структуры, включая процессы гликозилирования. Из цистерн ЭР Тиреоглобулин поступает в аппарат Гольджи, включается в состав секреторных гранул и секретируется во внеклеточный
коллоид, где происходит йодирование остатков тирозина и образование йодтиронинов.
Йодирование тиреоглобулина и образование йодтиронинов осуществляется в несколько этапов.
Транспорт йода в клетки щитовидной железы. Йод в виде органических и неорганических соединений поступает в ЖКТ с пищей и питьевой водой. Суточная потребность в йоде составляет 150-200 мкг. 25-30% этого количества йодидов захватывается щитовидной железой. Транспорт йодида в клетки щитовидной железы - энергозависимый процесс и происходит при участии специального транспортного белка против электрохимического градиента (соотношение концентраций I- в железе к концентрации I- в сыворотке крови в норме составляет 25:1). Работа этого йодид-переносящего белка сопряжена с Nа+,К+-АТФ-азой.
Окисление йода. Окисление I- в I+ происходит при участии гемсодержащей тиреоперокси-дазы и Н2О2 в качестве окислителя.
568
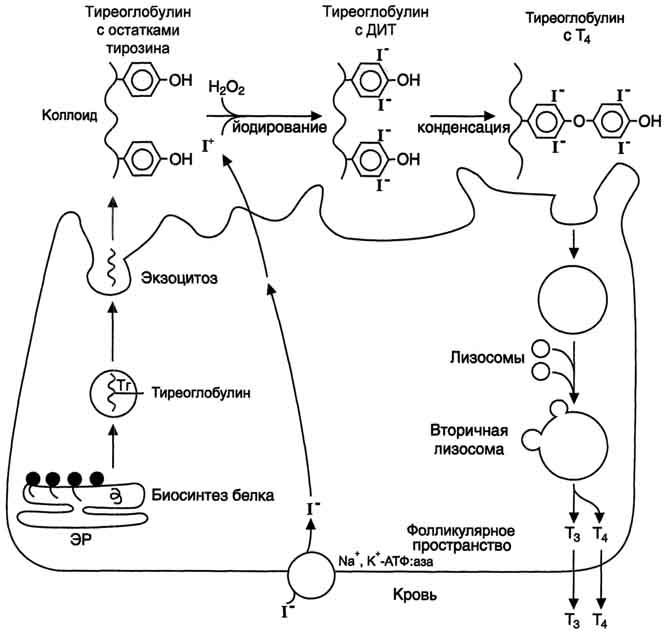 Схема
синтеза йодтиронинов.
Тиреоглобулин синтезируется на рибосомах,
далее поступает в аппарат Гольджи, а
затем во внеклеточный коллоид, где он
хранится и где происходит йодирование
остатков тирозина. Образование
йодтиронинов происходит в несколько
этапов: транспорт йода в клетки щитовидной
железы; окисление йода; йодирование
остатков тирозина; образование
йодтиронинов; транспорт йодтиронинов
в кровь. ЭР - эндоплазматический ретикулум;
ДИТ - дийодтиронин; Тг - Тиреоглобулин;
Т3
- трийодтиронин, Т4
- тироксин.
Схема
синтеза йодтиронинов.
Тиреоглобулин синтезируется на рибосомах,
далее поступает в аппарат Гольджи, а
затем во внеклеточный коллоид, где он
хранится и где происходит йодирование
остатков тирозина. Образование
йодтиронинов происходит в несколько
этапов: транспорт йода в клетки щитовидной
железы; окисление йода; йодирование
остатков тирозина; образование
йодтиронинов; транспорт йодтиронинов
в кровь. ЭР - эндоплазматический ретикулум;
ДИТ - дийодтиронин; Тг - Тиреоглобулин;
Т3
- трийодтиронин, Т4
- тироксин.
Йодирование тирозина. Окисленный йод взаимодействует с остатками тирозина в молекуле тиреоглобулина. Эта реакция также катализируется тиреопероксидазой.
Образование йодтиронинов.
Биосинтез тиреоидных гормонов состоит из следующих этапов
1) аккумуляция щитовидной железой йодидов крови (I-) с помощью "йодидный насоса" и их окисления йодидпероксидазою до молекулярного йода:
- 2е-
2 I-  I; 2
2) синтез специфического белка коллоида щитовидной железы тиреоглобулина и йодирования его тирозиновых остатков с образованием монойодтирозинив (МИТ) и
дийодтирозинив (ДИТ). Тиреогло- булин - гликопротеин с м.м. 660 кД, что олигомерные структуру (составляется из двух субъединиц); в со- ди белка - 115 остатков тирозина, 15-20% которых подлежат йодированию;
3) преобразования йодсодержащих тиро- Зилов остатков на йодованитиро- нины (в составе молекулы тиреогло- Булин);
4) секреция йодированного тирео- глобулина в полость фолликула, где этот высокомолекулярный предшественник тиреоидных гормонов сохраняется в составе коллоида;
5) поглощения (в условиях физиоло- гических потребностей и стимуляции тирео- Тропин) йодированного белка тирео- цитамы, включение его в фаголизо- сомы, расщепление молекулы йодо- ного тиреоглобулина (лизосо- минимальными тиреокатепсинамы) с образованием свободных молекул трех йодтиронины (Т3 ) и тетрайод- тиронины (Т4) и выход их из ба зальные мембраны клеток в кровь.