Материал: Задачи по биохимии
40. Понятие и разновидности азотистого баланса.
Азотистый баланс – соотношение между поступающим в организм и выводимым из организма азотом. Различают три вида азотистого баланса: азотистое равновесие, положительный азотистый баланс, отрицательный азотистый баланс
При положительном азотистом балансе поступление азота преобладает над его выделением. В физиологических условиях встречается истинный положительный азотистый баланс (беременность, лактация, детский возраст). Для детей в возрасте 1 года жизни он составляет +30%, в 4 года +25%, в подростковом возрасте +14%. При заболевании почек возможен ложный положительный азотистый баланс, при котором происходит задержка в организме конечных продуктов азотистого обмена.
При отрицательном азотистом балансе преобладает выделение азота над его поступлением. Это состояние возможно при таких заболеваниях как туберкулез, ревматизм, онкологические заболевания.
Азотистое равновесие характерно для здоровых взрослых людей, у которых поступление азота равно его выделению.
Азотистый обмен характеризуется коэффициентом изнашивания, под которым понимают то количество белка, которое теряется из организма в условиях полного белкового голодания. Для взрослого человека он составляет 53 мг N/ кг (или 24 г белка/сутки). У новорожденных коэффициент изнашивания выше и составляет 120 мг N на 1 кг массы тела. Азотистое равновесие обеспечивается белковым питанием.
Белковый рацион характеризуется опредёленными количественными и качественными критериями.
Количественные критерии белкового питания
Белковый минимум – то количество белка, которое обеспечивает азотистое равновесие при условии, что все энергетические затраты обеспечиваются углеводами и жирами. Он составляет 40-45 г/сутки. При длительном использовании белкового минимума страдают иммунные процессы, процессы кроветворения, репродуктивная система. Поэтому для взрослых людей необходим белковый оптимум - то количество белка, которое обеспечивает выполнение всех его функций без ущерба для здоровья. Он составляет 100 – 120 г/сутки.
Для детей норма потребления в настоящее время пересматривается в сторону её снижения. Для новорожденного потребность в белках составляет около 2 г/кг, к концу первого года снижается при естественном вскармливании до 1 г/кг, при искусственном вскармливании остаётся в пределах 1,5 – 2 г/кг
Качественные критерии белкового питания
Более ценные для организма белки должны отвечать следующим требованиям:
· содержать набор всех незаменимых аминокислот (валин, лейцин, изолейцин, треонин, метионин, лизин, аргинин, гистидин, триптофан, фенилаланин);
· соотношение между аминокислотами должно быть близким к соотношению их в тканевых белках;
· хорошо перевариваться в желудочно-кишечном тракте.
Этим требованиям в большей степени отвечают белки животного происхождения. Для новорожденных все белки должны быть полноценными (белки грудного молока). В возрасте 3-4 лет около 70-75% должно приходиться на полноценные белки. Для взрослых людей их доля должна составлять около 50%.
41. Особенности переваривания белков. Нормальные и патологические компоненты желудочного сока.
Пищеварения белков - это ферментативный гидролиз (протеолиз) пептидных связей в молекулах белков, в результате которого образуются свободные аминокислоты. Пищеварения белков происходит с помощью гидролаз, которые называются протеолитическими ферментами (протеазами или пептидазами). Они образуются в неактивной форме (проферменты или зимогена) и активируются путем частичного протеолиза, то есть путем гидролиза одного пептидной связи с последующимотщеплением ингибирующего N-концевого пептида. Активный фермент, образовавшийся в результате частичного протеолиза, может действовать на собственный профермент и переводить его в активное состояние, то есть осуществлять аутокатализ (сам себя активирует).
Место синтеза проферментов (слизистая оболочка желудка, поджелудочная железа) и место их активации (полость желудка, полость тонкой кишки пространственно отделены. Это необходимо для защиты секреторных клеток желудка и поджелудочной железы от аутопереваривания
Преждевременная активация проферментов в секреторных клетках происходит при язвенной болезни, остром панкреатите (активируются пепсин, трипсин,
соответственно). В норме в поджелудочной железе не происходит активация зимогенов благодаря наличию ингибитора трипсина, который образует с ферментом очень прочный комплекс. В желудке и кишечнике внутрених повехни покрыты муцинами - гликопротеинами слизи.
Муцины защищают эпителий желудочно-кишечного тракта от негативного воздействияпротеолитических ферментов.
Согласно местом действия на молекулы субстрата протеолитические ферменты распределяются на экзопептидаза и эндопептидазы.
Протеазы, или пептидазы, которые гидролизуют пептидную связь в конечной
аминокислоте, называются экзопептидаза.К ним относятся аминопептидазы, которая отщепляет последнюю аминокислоту с N-концабелковой молекулы, и карбоксипептидазы, которая гидролизует пептидную связь с С-конца молекулы белка, а также ди- и трипептидазы, расщепляющие дипептиды и трипептиды.
Пептидные связи, расположенные на расстоянии от концов молекулы белка, гидролизуют эндопептидазы: пепсин, трипсин, химотрипсин, эластаза.В зависимости от наличии в их активных центрах аминокислот серина, цистеина и других, различают сериновые протеазы, цистеиновые протеазы и другие.
Пептидазы характеризуются относительной специфичностью, то есть они расщепляют все
белки, но каждый из этих ферментов преимущественно гидролизует пептидные связи только между
определенными аминокислотами:
пепсин гидролизует пептидные связи, образованные карбосильнимы группами ароматических
аминокислот (фенилаланина и тирозина),а также лейцина и глутамата;
трипсин розщепляюе связи, образованные карбоксильными группами аргинина и лизина;
химотрипсин - фенилаланина, тирозина и триптофана;
эластаза - глицина, аланина, серина, пролина
Протеолитические ферменты используются как лекарственные средства (ацидинпепсин,фестал, панкреатин) при нарушении секреции желудочного сока, при воспалении поджелудочной железы. Кроме того, протеазы используются для обработки гнойных ран (Расщепляют белки, содержащиеся в гнойной жидкости). У шлунку діє фермент пепсин, котрий синтезується у основних клітиних слизової оболонки шлунку у вигляді неактивного проферменту пепсиногену. Цей зимоген активується шляхом часткового протеолізу за допомогою соляної кислоти (повільно), а далі – за механізмом аутокаталіза (швидко). Пепсин – це фермент з відносною специфічністю. Він гідролізує пептидні зв’язки, утворені карбоксильними групами ароматичних амінокислот (фенілаланіну, тирозину).
Нарушение переваривания белков в желудке:
Гиперхлоргидрия -повышенная продукция НСl.
Гипохлоргидрия - уменьшенная продукция НСl.
Ахиллия - отсутствие в желудочном соке НСl и пепсина.
(Полная ахилия или тотальная резекция желудка может вызвать злокачественную пернициозной
анемию, так как отсутствует внутренний фактор Касла - гастромукопротеин, необходимдля всасывания витамина В12).
Компоненты желудочного сока в норме и при патологических состояниях
|
Состояние |
рН |
Кислотность (ТЕ) |
Пепсин |
Фактор Касла |
Молочная кислота |
Кровь |
||||||
|
общая |
связанная НСl |
свободная НСl |
||||||||||
|
Норма |
1,5-2,0 |
40-60 |
20-30 |
20-40 |
+ |
+ |
- |
- |
||||
|
Гиперацидный гастрит |
1,0 |
80 |
|
40 |
+ |
± |
- |
- |
||||
|
Гипоацидный гастрит |
2,5 |
40 |
|
20 |
± |
± |
± |
- |
||||
|
Ахилия |
7,0 |
20 |
|
- |
- |
- |
+ |
- |
||||
|
Язва желудка |
1,5 |
60 |
|
40 |
+ |
+ |
- |
+ |
||||
|
Рак желудка |
6,0 и> |
40-60 |
|
20 |
+ |
+ |
+ |
+ |
||||
42. Гниение белков в толстом кишечнике.
Всасывание аминокислот представляет собой активный Na-зависимый процесс, требующий затрат энергии АТФ. Перенос отдельных аминокислот осуществляется специальными переносчиками с участием трипептида глютатиона.
У детей могут всасываться не только аминокислоты, но также пептиды и низкомолекулярные белки. Это, с одной стороны, обеспечивает поступление в организм ребёнка иммуноглобулинов, антител грудного молока. С другой стороны, может вызывать аллергические реакции.
Процессу гниения в толстом кишечнике под действием ферментов гнилостной микрофлоры подвергаются не полностью расщепившиеся белки и отдельные не всосавшиеся аминокислоты. При гниении белков образуется большое количество газообразных и негазообразных веществ. К продуктам гниения белков относятся CO2, CH4, NH3, H2S, меркаптаны, альдегиды, кетоны, карбоновые кислоты, диамины, вещества циклической структуры.
Диамины образуются при декарбоксилировании диаминокислот лизина и орнитина
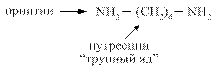
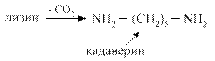
Диамины могут выводиться из кишечника или обезвреживаться в печени
При гниении белков могут образовываться токсичные циклические продукты. Гниение тирозина ведёт к появлению крезола и фенола, гниение триптофана сопровождается образованием скатола и индола.
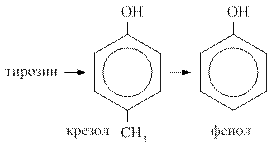
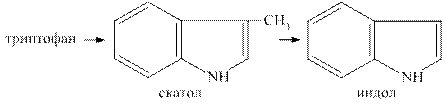
Продукты гниения белков чрезвычайно токсичны, по системе vena porta, они поступают в печень, где подвергаются процессам обезвреживания.
43. Реакции дезаминирования аминокислот и их биологическая роль.
Дезаминирование - это процесс отщепление α-аминогруппы от аминокислоты в виде аммиака.
Дезаминирования подлежат все аминокислоты, кроме лизина. Существует несколько видов дезаминирования:
прямое окислительное – для глутаминовой кислоты,
прямое неокислительное:
гидролитическое - для цистеина,
внутримолекулярная перестройка - для гистидина,
восстановительное - для серина и
треонина,
непрямое - для большинства аминокислот.
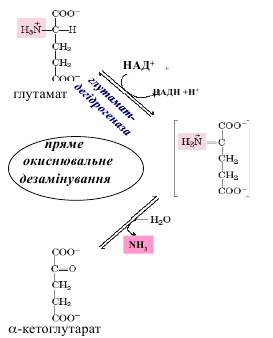
Основным видом прямого дезаминирования является окислительное дезаминирование,
которому подлежит только глутаминовая кислота.Прямое окислительное дезаминирование глутаминовой кислоты осуществляется
помощью фермента глутаматдегидрогеназы (кофермент НАД + или НАДФ +),
локализованного в митохондриях многих органов (максимально в печени) и с высокой
скоростью преобразующего глутамат в α-кетоглутарат. При прямом дезаминированииобразуется свободный аммиак (токсичное вещество), который далее обезвреживается. Большинство
аминокислот участвует в косвенном дезаминировании, первым этапом которого является трансаминирование
44. Трансаминирование аминокислот: биологическая роль реакций, использование в диагностике.Глюкозо-аланиновый цикл.
Трансаминирование - это перенос аминогруппы от аминокислоты (донора) на α-
кетокислоту (акцептор) с последующим образованием новой α-кетокислоты и новой
аминокислоты без промежуточного выделения аммиака.
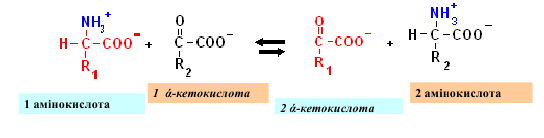
Эту реакцию катализируют аминотрансферазы (трансаминазы). Коферментом
аминотрансфераз является пиридоксальфосфат (Палфи) - активная форма витамина В6, который в качестве посредника принимает аминогруппу от аминокислоты и превращается в пиридоксаминфосфат (Памфа). Аминотрансферазы органоспецифические: аланин-Аминотрансфераза (АЛТ) локализован преимущественно в пеичнци, аспартатаминотрансфераза (АСТ) - в сердце. При повреждении этих органов ферменты
попадают в кровь. Определение их активности в сыворотке крови является очень важным
методом для выявления и контроля за ходом острого гепатита (АлАт) иинфаркта миокарда (АсАт). Активность этих индикаторных ферментов повышается при
данных заболеваниях в 20-30 раз.
Значение реакций трансаминирования:
коллекторная функция - сбор аминогрупп от различных
аминокислот в виде глутаминовой кислоты;
синтез заменимых аминокислот;
перераспределение аминного азота в тканях; начальный этап катаболизма аминокислот, первая
стадия косвенного дезаминирования;
благодаря реакциям трансаминирования углеродный
скелет аминокислот может включаться в другие виды обмена
веществ
Глюкозо-аланиновый
цикл функционирует
в мышцах при голодании. При дефиците
глюкозы, АТФ синтезируется за счет
распад белков и катаболизма аминокислот
в аэробных условиях, при этом
глюкозо-аланиновый цикл обеспечивает:
1) удаление азота из мышц в нетоксичной
форме; 2) синтез глюкозы (печень).