Материал: выделение_макрофагов
http://imuno.net/208.php
Культивирование макрофагов и моноцитов. Методики.
Брюшинные макрофаги. Материалы и оборудование
а) Для получения перитонеальных клеток необходимы инбредные мыши различных штаммов в возрасте 3—4 мес, изотонический фосфатный буфер (например, Институт иммунных препаратов и питательных сред, Берлин), после получения сухого препарата его растворяют в тридистиллированной воде и проводят стерилизацию фильтрованием при 4°С 4—6 нед. Нужно иметь также раствор гепарина без консервантов (5000 МЕ/мл), сыворотку эмбрионов коров, инактнвированную нагреванием в течение 30 мин при 56 °С, 70% этанол, вату, кубики льда, анатомические пинцеты, ножницы, стеклянные шприцы на 10 и 20 мл, стальные иглы № 16 и 18, стакан на 400 мл, силиконизированные стеклянные центрифужные пробирки на 25 мл, настольную центрифугу,
б) Для подсчета и дифференциального определения макрофагов и моноцитов используют смесь цитрат/NаСl (8 объемов 1М NaCl+ 2 объема 1М лимонной кислоты; подводят рН 20% NaOH до 3,0—3,5 при 4°С после добавления небольшого количества тимола), 0,1% раствор кристаллического фиолетового в 1М лимонной кислоте, 0,1% раствор нейтрального красного в дистиллированной воде (краситель хранят при комнатной температуре несколько месяцев), раствор туши (коммерческую черную тушь разводят в соотношении 1 : 20 0,15 М NaCl, автоклавируют), мерные пипеткидля лейкоцитов и эритроцитов, камеру Biirker, обогреваемый столик, световой микроскоп,
в) Для получения культур макрофагов и моноцитов нужно иметь раствор Хенкса (например, Институт иммунных препаратов и питательных сред, Берлин), концентрат растворяют в тридистиллированной воде, стерилизуют фильтрацией, хранят при 4°С в течение 4—6 нед; среду Игла-МЕМ (тот же поставщик) и PPMI 1640; к средам добавляют по 2 г гидрокарбоната натрия и по 290 мг глутамина, растворяют в 1 л тридистиллированной воды, стерилизуют фильтрацией, хранят 4—6 нед при 4°С. Также необходимы растворы антибиотиков: 1 000 000 ЕД пенициллина +1 г стрептомицина растворяют в 100 мл тридистиллированной воды, стерилизуют фильтрацией, делят на небольшие порции и сохраняют при —20°С, инактивированная сыворотка эмбрионов коров, нормальная лошадиная сыворотка (инактивированная), человеческая сыворотка (инактивированная), газовая смесь: 92,5 частей воздуха и 7,5 частей СОг, стеклянные чашки Петри диаметром 5 см, пипетки на 1, 5 и 10 мл, мерные цилиндры на 50 и 100 мл, эрленмейеровские колбы на 50 и 100 мл, эксикатор, термостат, качалка.
Для силиконирования стеклянной посуды ее скачивают раствором силикона (Serva, ФРГ) и высушивают 1 ч при 100 °С. Способы очистки посуды см. раздел "Образование антител культурами клеток". Посуду упаковывают в алюминиевую фольгу и стерилизуют 2 ч при 180 °С. Так же стерилизуют ножницы и пинцеты. Растворы и среды стерилизуют пропусканием через антибактериальный фильтр G5.
Получение макрофагов из моноцитсодержащих суспензий клеток
а) Получение перитонеальных клеток: мышей забивают цервикальной дислокацией. Шкуру животного смачивают 70% этанолом. Захватывают пинцетом шкуру на животе и делают надрез ножницами с таким расчетом, чтобы разрез раздвигался в краниально-каудальном направлении. В брюшную полость вводят 3—4 мл жидкости (изотонический буфер с добавлением 5000 ЕД гепарина и 20 мл сыворотки эмбрионов коров из расчета на 1л). Жидкость вводят осторожно, стараясь не повредить кишечник, слегка приподнимая брюшную стенку пинцетом. После инъекции живот массируют большим и указательным пальцами 20—30 сек. Перитонеальную жидкость медленно отсасывают шприцем. Для этого иглу вводят в латеральную часть живота параллельно брюшной стенке. Рекомендуется отсасывать перитонеальную жидкость с обеих сторон живота, тогда из 4 мл введенной жидкости получают 3,5 мл перитонеальной жидкости, которую собирают в охлажденные до 0°С силиконнзированные центрифужные пробирки. Перитонеальную жидкость, загрязненную кровью, не используют. Клетки осаждают центрифугированием в течение 10 мин при 150 g, ресус-пендируют осадок в растворе Хенкса. До засева культуры клетки сохраняют на льду. Ниже приводится состав клеток перитонеальной жидкости у различных штаммов мышей.
Состав клеток перитонеальной жидкости у различных штаммов мышей
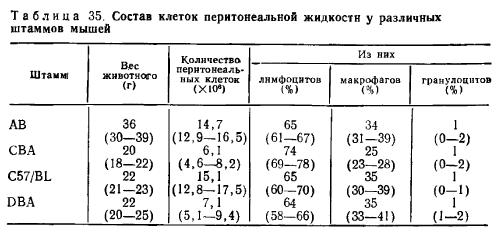
Примечание. Представлены данные от 5 животных 3-месячного возраста, в скобках — размах вариации.
Внутрибрюшинное введение различных раздражающих средств за 3—4 дня до получения перитонеальной жидкости существенно увеличивает число клеток и содержание в них макрофагов.
Влияние различных раздражающих веществ на число и состав клеток перитонеального экссудата (данные получены на мышах СБА)
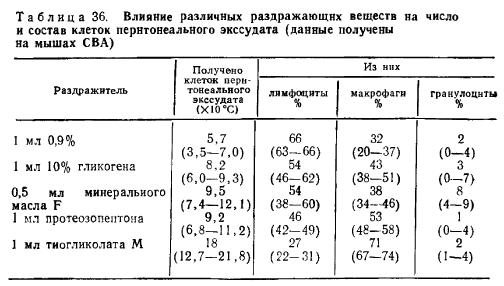
Следует указать, что индуцированные перитонеальные макрофаги отличаются по целому ряду свойств от неиндуцированных. К числу таких свойств относятся усиление пиноцитоза и фагоцитоза, а также усиление секреции биологически активных веществ in vitro.
Разделение клеток крови в градиенте плотности Получение мононуклеаров из крови: мононуклеары получают из гепаринизированной крови (10 me гепарина/мл),
Между величиной и плотностью клеток существует тесная взаимосвязь. Обычно меньшие по размеру клетки обладают относительно меньшим объемом цитоплазмы по сравнению с ядром и, следовательно, большей плотностью. Разумеется, из этого правила есть исключения. Клетки, различающиеся по .величине и плотности, могут быть разделены методом изопикнического пли изокинетического центрифугирования, а также осаждением в градиенте плотности. При изопикническом центрифугировании клетки располагаются в слоях градиента с соответствующей плотностью. В случае изокинетического центрифугирования в менее плотном градиенте клетки с большим диаметром седиментируют быстрее. Тот же принцип лежит в основе осаждения клеток в градиенте плотности.
Материалы и оборудование. Для работы необходимы: центрифуга с охлаждением, бакет-ротор, градиентный смеситель, вещества для формирования градиента, такие, как альбумин, сыворотка эмбрионов коров, фиколл, лимфопреп, перколл (Pharmacia, Швеция), визотраст или другие рентгеноконтрастные вещества.
Центрифугирование в градиенте плотности
Ввиду разнообразия применяемых методов фракционирования клеток в градиенте плотности невозможно в рамках настоящей главы дать их детальный разбор. В зависимости от биологического вида, органного происхождения, стадии жизненного цикла и активации плотность лимфоцитов, макрофагов, гранулоцитов варьирует в пределах 1,04—1,12 г/мл. Обычно разброс величин плотности составляет около половины этого интервала. Условия центрифугирования подбираются индивидуально в зависимости от характера эксперимента, основные варианты представлены в таблице:
И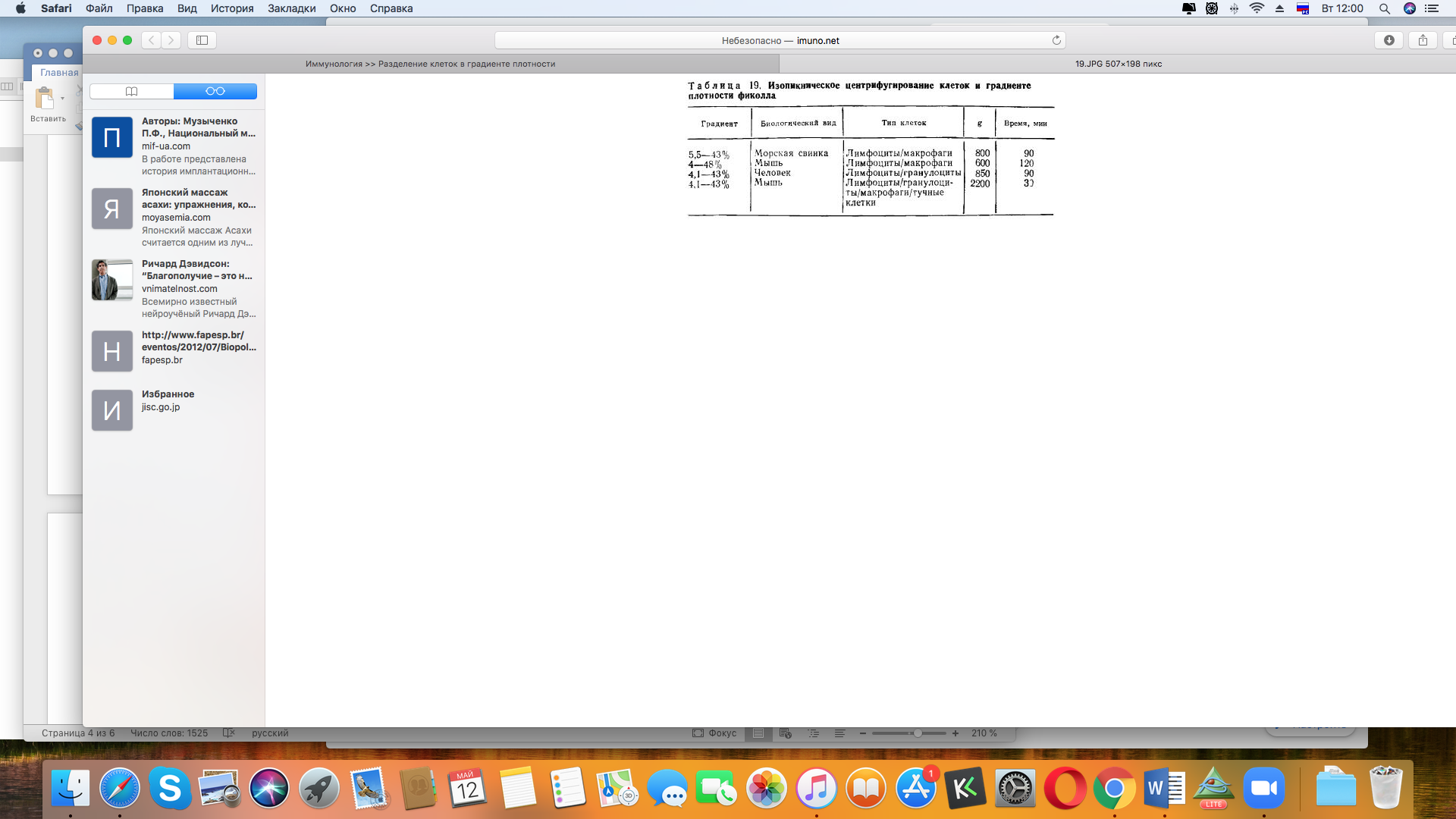 зопикническое
центрифугирование клеток и градиенте
плотности фиколла
зопикническое
центрифугирование клеток и градиенте
плотности фиколла
Если требуется разделить клетки в соответствии с их плотностью, но нет никаких предварительных указаний на то, как это сделать, можно попытаться разделить клетки в линейном градиенте, исследовать, в какой области градиента преобладает определенный тип клеток, а затем провести разделение в прерывистом градиенте.
Изопикническое разделение. В качестве одного из вариантов градиентного центрифугирования, помимо перечисленных в таблице, можно использовать следующий.
Градиентбычьий сывороточный альбумин15—28%; 3800 g в течение 45 минут или 4000 g в течение 30 минут. Разделению подвергаются лимфоциты мыши и крысы. При приготовлении градиента надо выбирать инертные, которые не диссоциируют на ионы и образуют водные растворы с низкой вязкостью.
Растворы таких веществ должны обладать незначительным осмотическим давлением во избежание повреждения разделяемых клеток. Лучше всего этим требованиям отвечают фиколл, перколл и альбумин. Альбумин предварительно должен быть отдпализирован, деионизирован, его рН должен быть доведен до 5,1. Это значение рН хорошо переносится клетками и препятствует образованию агрегатов. Диализ необходим для удаления солей, которые могут присутствовать в альбумине и повышать осмотическое давление. Добавлением гомологичной нормальной сыворотки разницу в осмотическом давлении можно еще уменьшить. На дно центрифужных пробирок часто наслаивают так называемую «подушку», т. е. небольшое количество раствора высокой плотности (45% фиколл или 40% альбумин). Затем вносят суспензию клеток в растворе фиколла или альбумина низкой плотности и подслаивают собственно градиент. Можно также примешивать клетки непосредственно к линейному градиенту, но при этом следует избегать образования агрегатов. После центрифугирования клетки отсасывают при помощи перистальтического насоса, собирают фракции, содержащие клетки. Жидкость из пробирки можно отсасывать сверху или снизу, через прокол в стенке пробирки.
Значительно чаще, чем непрерывный, используют ступенчатый градиент плотности. По своему составу градиенты могут значительно варьировать. Мы ограничимся только двумя примерами.
*Одновременное разделение эозинофилов, нейтрофилов и моноцитов человека в градиенте фиколл/гипак:
(A) 15,0 мл 9% фиколла + 10,0 мл 50% гипака; плотность 1,14 г/мл.
(Б) 17,5 мл 9% фиколла + 10,0 мл 50 гипака; плотность 1,13 г/мл.
(B) 20,0 мл 9% фиколла+10,0 мл 50% гипака; плотность 1,12 г/мл.
(Г) 24,0 мл 9% фиколла + 10,0 мл 50% гипака; плотность 1,06 г/мл.
Составляют градиент осторожно, наслаивая друг на друга по 2,0 мл растворов уменьшающейся плотности. Сверху наслаивают 2,0 мл гепаринизированной крови, разведенной в соотношения 1:2 0,15 М NaCl. Центрифугируют 40 минут при 1000 g и 22°С. Клетки распределяются тогда между различными слоями следующим образом: между плазмой и слоем Г — моноциты и лимфоциты с 97—100% чистотой, между Г и В — нейтрофилы с 94—99% чистотой, между В и Б — непрофилы (50—98%) и эозинофилы (2—50%), между Б и А —эозинофилы с 80—99% чистотой.
**Разделение гранулоцитов и фракции лимфоциты/моноциты человека в градиенте фиколл/триомбраст:
(А) 10 объемов 34% триомбраста плотность 1,075 г/мл при 22°С
24 объема 9% фиколла (Б) 10 объемов 34% триомбраста плотность 1,097 г/мл при 22°С 24 объема 14,6% фиколла
На градиент, составленный из 5 мл фракции А и 5 мл фракции Б, наслаивают 10 мл разведенной в соотношении 1:2 гепаринизированной крови. Центрифугируют 40 минут при 400 g и 22°С. Легкая фракция содержит лимфоциты (свыше 60%), моноциты (свыше 35%) и гранулоциты (около 1%).
Плотная фракция содержит 98% гранулоцитов, их выход составляет 60%.
***Изокинетическое разделение.
Изокинетическое разделение используют при необходимости разделять клетки одинаковой плотности, но различной величины. Если используется градиент фиколла 2,6—5,5%, то центрифугирование проводят при 18,7 и 97 g в течение 30—14 мин. Результаты можно существенно улучшить, дополнив изокинетическое центрифугирование изо-пикническим. Все многообразие методов разделения клеток можно видеть на примере разделения моноцитов и лимфоцитов человека в градиенте перколла. Раствор перколла (30 мл) с плотностью 1,060 г/мл в среде, не содержащей Са2+ и Mg2+, центрифугируют в течение 1 ч при 26 000 g для формирования градиента плотности. На этот градиент наслаивают 3,0 мл суспензии моноциты/лимфоциты (15х106/мл). Разделение моноцитов и лимфоцитов происходит в ходе изокинетического центрифугирования в течение 5 минут при 400 g. Выход высокогомогенной фракции моноцитов составляет около 50% от их содержания в крови.
Седиментация в градиенте плотности
Фракционирование клеток различной величины чаще всего проводят в седиментационной камере по принципу Miller и Phillips. Диаметр таких камер обычно варьирует от 11 до 21 см, но известны и камеры меньшего размера. Для стабилизации разделяющей жидкости и предотвращения конвенции градиент формируют из сыворотки эмбрионов коров. Готовят суспензию клеток (107/мл) в 3% сыворотке эмбрионов коров. В камере диаметром 11 см седиментируют 20 мл, диаметром 21 см—100 мл суспензии клеток. Градиент формируется в процессе центрифугирования, которое происходит при 4°С н длится 3,5—4,5 ч. Клетки сорбируют фракциями по 12—15 мл.
Оценка метода
Если величина и плотность клеток коррелируют между собой, центрифугирование в градиенте плотности и седиментация в градиенте дают одинаковые результаты. Однако если клетки при одинаковой величине обладают различной плотностью или при одинаковой плотности различной величиной, то один из двух методов разделения может оказаться более эффективным. Воспроизводимость методов, основанных на центрифугировании, очень высока. Например, при разделении клеток одинакового происхождения в линейном градиенте альбумина (15— 30 фракций) положение пика отклоняется в среднем на 0,0003 г/мл, т. е. приблизительно на четверть величины средней фракции. Также отмечаются заметные вариации профиля разделения клеток у различных индивидов. Выход составляет 89±9°/о, погибшие клетки образуют осадок.
Еще одной проблемой центрифугирования в градиенте плотности является необходимость создания по всему градиенту условий, одинаково хорошо переносимых всеми клетками. В противном случае возможна утеря клетками биологической активности. Для разделения Т- и В-лимфоцитов градиентные методы не подходят. В нестимулированном состоянии оба типа клеток различаются весьма незначительно по плотности и величине. Поскольку эти последние свойства сильно варьируют в зависимости от степени дифференцировки и активации клеток, получение профилей их распределения по плотности в величине представляет собой картину, отражающую внутриклеточные процессы в Т- и В-субпопуляциях. После стимуляции антигенами или митогенами как В-, так и Т-лимфоциты дают очень большой разброс по плотности и величине в начале иммунного ответа. На поздних этапах популяция становится гомогенной. Помимо лимфобластов, разделить можно и такие субпопуляции, как Т-хелперы и Т-супрессоры. Степень чистоты макрофагов достигает 98%, гранулоцитов — свыше 90%.
Из перитонеальной жидкости эозинофилы выделяются с чистотой 88%, тучные клетки — с чистотой 95%. При помощи четырехступенчатого градиента за один этап работы удается получить из крови одновременно эозинофилы (чистота 80—99%), нейтрофилы (чистота 94—99%), моноциты (чистота 97—100%). Из опухолей, содержащих приблизительно 2% лимфоцитов, получали фракции, содержащие 15% В- и 43% Т-лимфоцитов. Из костного мозга, хотя и с ограничениями, удается выделять стволовые клетки и лимфоциты.