Материал: Вплив антропогенного навантаження на функціонування глутатіонової системи у насінні представників роду Acer L
Клен гостролистий, або клен платановидний (Acer platanoides L.),- дерево висотою до 25-30 метрів з розлогою густою кроною. Стрижневий корінь відносно невеликий, але бічні корені поширюються досить далеко. Потужний стовбур покритий сіро-бурою корою. Листя клена розташовані на тонких черешках, мають добре прокреслені жилки і, як правило, 5 лопастей, які закінчуються загостреними частками. Зеленувато-жовті квітки, зібрані в щитковидні суцвіття на кінцях гілок, можуть бути як роздільностатевими, так і обох статей, причому на одному і тому ж дереві.
Нектарники в квітках рясно випромінюють солодку рідину. Цвіте
клен до розпускання листя або під час нього. Плід - подвійна крилатка, яка
ділиться на два односемянних плодики з великими крилами. У вересні крилатка
розпадається і плодики розносяться вітром. У дикій природі клен гостролистий
розмножується насіннєвим шляхом, але, незважаючи на те, що насіння проростає
навесні, більша частина сходів гине. У перші роки життя клен гостролистий росте
досить швидко, максимальної своєї висоти досягає до 50-60 років. Плодоносить
він з 17 років, а середня тривалість життя дерева становить 150-200 років.


Рис. 2.1.2. Acer platanoides L.
Клен гостролистий поширений в основному в Євразії. На півночі ареал його поширення обмежений скандинавськими країнами, на півдні - північною межею Ірану, на сході - Уральським хребтом. На Україні і в Росії він росте лише в широколистяних або змішаних лісах, а також у лісостеповій зоні. Клен частіше росте по сусідству з дубом і ясеном, часто його висаджують у міських парках і скверах, в полезахисних лісових смугах. Дерево не боїться затінення і холодів, але відчутно до стану грунту і воліє вологі і родючі землі.
Клен гостролистий у стародавніх вважався добрим деревом, з ним пов'язано безліч прикмет - його висаджували на щастя чи для залучення любові. Перші згадки про застосування клена як лікарської рослини датуються 16-17 століттям. Для лікування використовували не тільки кору, листя, плоди і квітки клена, але і кленовий сік, який мав славу смачного і корисного напою. Також кленовим соком змащували рани і виразки. Віник з клена вважався одним з атрибутів знахарських лазень.
Деревина клена дуже міцна, в той же час вона добре піддається обробці і легко полірується. З неї виготовляють спортивний інвентар, меблі, господарське начиння, струнні музичні інструменти, фанеру. Кленові дрова НЕ коптять і дають багато тепла. З листя отримують чорний і жовтий фарбники для вовни. Медоносні властивості цієї рослини вище всяких похвал - з солодкого кленового нектару бджоли роблять високоякісний світлий мед, причому з одного дерева здорова бджолина сім'я може заготовити до 10 кг меду. З кленового соку готують сироп. Гілки і листя клена із задоволенням поїдає худоба.
Згідно з проведеними нещодавно дослідженнями, клен здатний затримувати в повітрі суспензії важких металів і пари бензолу[28]. Тому ця рослину доцільно висаджувати в міських умовах, з метою поліпшення екологічної ситуації.
У кленовому соку міститься цукор і каучук. У листі клена виявлені вуглеводи, каротиноїди, альдегіди, фенолкарбонові і органічні кислоти, вітаміни С і Е, дубильні речовини, ліпіди і ненасичені жирні кислоти.
Насіння клена знаходиться у глибокому ендогенному спокої, викликаномунаявністю в насінні інгібіторів росту, тому перед весняним посівом насіння стратифікуютьза температури 0-3°С протягом 2-3 місяців. За 5-7 °С тривалість холодової стратифікації зростає [47]. Тому для швидкого подолання дії інгібіторів, стимулювання проростання насіння і наступного росту сіянців використовують фізіологічно активні речовини - стимулятори росту.
2.2 Методи досліджень
Збирання насіння проводили у вересні 2014 р. на чотирьох пробних ділянках із модельних дерев віком 20-30 років з гілок п’ятого порядку галуження нижньої та середньої частин крони на північній стороні.
Методика визначення активності глутатіон-S-трансферази
Активність глутатіон-S-трансферази (GSТ) [EC 2.5.18] визначали за [81].
Субстратом служив 2,4-динітрохлорбензол (ДНХБ).
Рослинний матеріал (0,2 г сирої ваги) розтирали у фарфоровій ступці з 1 мл натрій-фосфатного буферу (рН 8,0), центрифугували протягом 20 хв при 16000 об/хв., у супернатанті визначали активність GSТ.
Реакційну суміш, яка містить 1 мл фосфатного буфера (рН 8,0), 0,1 мл розчину відновленого глутатіона й 0,2 мл зразка, витримували в ультратермостаті 10 хвилин при 30˚ С.
Ферментативну реакцію ініціювали додаванням 0,1 мл 0,02 М розчину ДНХБ і на КФК-2МП реєстрували зміни оптичної густини розчину при довжині хвилі 340 нм протягом 4 хв.
Каталітичну активність ферменту виражали в мкмоль ДНХБ, перетвореного за 1 секунду (мккатал).
Розрахунок каталітичної активності проводили за формулою:
A=![]() ,
,
де ΔЕ - зміна оптичної густини реакційної суміші за час вимірювання; заг. - загальний об’єм реакційної суміші, мл; проби - об’єм супернатанту, взятого для аналізу, мл; - товщина кювети, 0,3 см; - час вимірювання, 240 сек; - коефіцієнт молярної екстинкції ДНХБ, 9,6 мкмоль-1∙∙см-1.
Методика визначення активності глутатіон-редуктази (GR)
Визначення активності глутатіон-редуктази (GR, EC 1.6.4.2) проводили за методом [78].
Рослинний матеріал (0,1 г сирої ваги) розтирали у фарфоровій ступці з 1 мл натрій-фосфатного буферу (рН 8,0), центрифугували протягом 20 хв при 16000 об/хв., у супернатанті визначали активність GR.
Реакційну суміш, яка містила 1 мл 0,1 М фосфатного буферу (рН 8,0), 0,1 мл 1 мМ розчину ЕДТА, 0,3 мл розчину окисленого глутатіону (GSSG) та 0,2 мл розчину NADPH, витримували у термостаті протягом 10 хвилин при 37˚ С. Реакцію починали додаванням 0,2 мл проби і реєстрували зменшення концентрації NADPH у кюветі спектрофотометра при довжині хвилі 340 нм. Каталітичну активність ферменту виражали у наномоль NADPH, переробленого за 1 сек (нанокатал).
Розрахунок каталітичної активності проводили за формулою:
A=![]() ,
,
де ΔЕ - зміна оптичної густини реакційної суміші за час вимірювання; заг. - загальний об’єм реакційної суміші, мл; проби - об’єм супернатанту, взятого для аналізу, мл; - товщина кювети, 0,3 см; - час вимірювання, 240 сек; - коефіцієнт молярної екстинкції NADPH, 6,22 мкмоль-1∙∙см-1.
Методика визначення активності глутатіон-пероксидази (GPX)
Визначення активності глутатіон-пероксидази (GPX, EC 1.11.1.9) проводили за методом [85].
Рослинний матеріал (0,2 г сирої маси) розтирали у фарфоровій ступці з 1 мл натрій-фосфатного буферу (рН 7,4), центрифугували протягом 20 хв. при 16000 об/хв., у супернатанті визначали активність GPX.
Реакційну суміш, яка містила 1,2 мл 0,1 М фосфатного буферу (рН 7,4), 0,2 мл 1 мМ розчину ЕДТА, та 0,1 мл 4 мМ розчину NADPH, 2 мл 10 мМGSH, 0,2 мл зразка витримували у термостаті протягом 10 хвилин при 30˚ С. Реакцію починали додаванням 0,2 мл 2,5 мМ розчину перекису водню і реєстрували зменшення концентрації NADPH у кюветі спектрофотометра при довжині хвилі 340 нм. Каталітичну активність ферменту виражали у наномоль NADPH, переробленого за 1 сек (нанокатал).
Розрахунок каталітичної активності проводили за формулою:
A=![]() ,
,
де ΔЕ - зміна оптичної густини реакційної суміші за час вимірювання; заг. - загальний об’єм реакційної суміші, мл; проби - об’єм супернатанту, взятого для аналізу, мл; - товщина кювети, 0,3 см; - час вимірювання, 240 сек; - коефіцієнт молярної екстинкції NADPH, 6,22 мкмоль-1∙∙см-1.
Методика визначення відновленого глутатіону
Вміст відновленого глутатіону (GSH) визначали згідно з [45] за реакцією SH-групи глутатіону з 5,5-дитіо-біс(2-нітробензойною) кислотою (реактив Елмана). У результаті реакції утворюється 5-дитіо-2-нітробензойний аніон, який має інтенсивний жовтий колір, на чому й засновано кількісне вимірювання SH-груп у клітинних екстрактах.
Вміст SH-груп вимірювали за калібрувальним графіком (рис. 2.2.1), побудованим з розчинами відновленого глутатіону у таких концентраціях: 10, 25, 50, 75 та 100 нМ/мл.
Рослинний матеріал (0,5 г сирої ваги) розтирали у середовищі виділення (0,1 М трис-HCl буфер, рН 7,8, з додаванням 1 мМ хлориду магнію та 0,3 мМ Трилону Б), центрифугували протягом 20 хв. при 15000 g, надосадову рідину брали для подальшої обробки.
Небілкову розчинну фракцію отримували шляхом осадження розчинних білків із надосадової рідини за допомогою 50% трихлороцтової кислоти (ТХУ): до 3 мл зразка додавали 2,4 мл дистильованої води та 0,6 мл ТХУ, перемішували, витримували 15 хв. та центрифугували протягом 20 хв. при 15000 g, супернатант брали для визначення небілкових толових сполук.
Реакційна суміш для визначення містила 2 мл 0,1 М трис-HCl
буфер, рН 7,8, та 1 мл супернатанту (контрольна проба містила 3 мл вказаного
буферу). Вимірювали оптичну густину (А0) на фотоелектроколориметрі
КФК-2МП при довжині хвилі 400 нм у кюветах товщиною 0,5 см проти контролю. До
проб додавали 0,05 мл реактиву Елмана, проби інкубували протягом 1 години при
37˚ С, після чого знов вимірювали оптичну густину (А1). Для
розрахунків використовували різницю (А1 -А0=А) та дані
калібрувального графіку, вміст SH-груп виражали в нмоль GSH/г наважки.
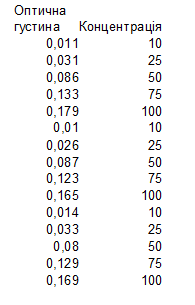
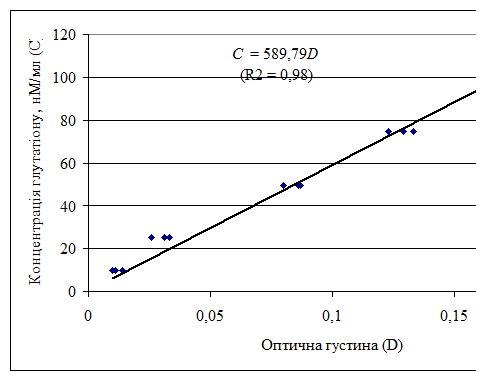
Рис. 2.2.1. Калібрувальний графік для визначення вмісту
відновленого глутатіону
. Стандартне відхилення обчислювали за формулами:
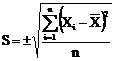 ;
;
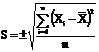 ;
;
- стандартне відхилення;
![]() -
-
![]() - відхилення варіації від середнього арифметичного.
- відхилення варіації від середнього арифметичного.
. Статистичну помилку розраховували за формулами:
![]() ,
для n<30;
,
для n<30;
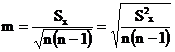 ,
для n>30,
,
для n>30,
де m - помилка вибіркового середнього.
. Коефіцієнт Ст’юдента обчислювали за формулою:
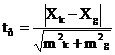 .
.
. Достовірність результатів визначали за таблицею Ст’юдента - якщо
![]() ,
то дані достовірні[15; 57; 59].
,
то дані достовірні[15; 57; 59].
3. Фізико-географічна характеристика району досліджень
Дослідження впливу техногенного забруднення на стан глутатіонової системи у деревних рослин A. platanoidesта A. pseudoplatanus проводили на чотирьох пробних ділянках -контрольній та трьох дослідних, розміщених на урбатехногенних територіях м. Дніпропетровськ:
№1 -умовно чиста зона - Ботанічний сад Дніпропетровського національного університету імені Олеся Гончара, де, за даними міської санепідемстанції, концентрації забруднювачів не перевищують ГДК;
№2 -зелена зона, розташована на території, прилеглій до пр. Кірова з інтенсивним автомобільним рухом, який є джерелом важких металів.
№3 -штучний фітоценоз, прилеглий до вул. Героїв Сталінграду з інтенсивним автомобільним рухом і забруднений важкими металами.
№4 -зелена зона ВАТ «Інтерпайп Нижньодніпровський трубопрокатний завод» і ВАТ «Дніпрометиз», яка прилягає допр. Правди з інтенсивним автомобільним рухом. Основні забруднювачі - токсичні гази та важкі метали. Лісорослинні умови, характеристики деревостану, структура і склад насаджень в дослідній і контрольній зонах були подібними.
Необхідно підкреслити, що в умовах степової зони лісова рослинність зустрічається дуже рідко внаслідок географічної невідповідності лісів умовам існування. Природні ліси у степу приурочені, головним чином, до балок і долин річок, де краща зволоженість ґрунтів та менша їх мінералізованість. Штучні ж ліси знаходяться не лише в умовах географічної, але часто й екологічної невідповідності біогеоценозів, що створюються, умовам їх існування [90].
Не зважаючи на це, створення лісів у межах степової зони України можливе за правильного підбору лісоутворювальних порід, які б підходили до конкретних умов середовища існування, в результаті чого покращуються рослинні умови на користь лісу і тоді він перебуває в умовах своєї екологічної відповідності. Географічна ж невідповідність спостерігається лише в надто посушливі роки, коли кількість опадів різко зменшується, а рівень ґрунтових вод знижується [91].
Більша частина лісів Дніпропетровської області має штучне походження і виконує санітарно-гігієнічні, захисні, водо- й ґрунтово-охоронні та інші функції. Штучних лісонасаджень в області понад 125 тис. га, з них понад 50 тис. га належать до санітарно-гігієнічних і оздоровчих: це міські ліси, зелені зони навколо населених пунктів, джерел водопостачання, лікувальних закладів, промислових підприємств у межах санітарно-захисних зон [40].
Кліматичні умови фізико-географічного району недостатньо сприятливі для вирощування багатьох деревно-чагарникових і трав'янистих рослин з інших флористичних областей. Клімат району характеризується як помірно континентальний, посушливий. Середня температура найбільш холодного місяця (січня) становить -5,7 °С. Середній річний температурний мінімум, що визначає стан зимівлі багатьох теплолюбних рослин, становить -23...-25 °С, а абсолютний мінімум досягає -38 °С. Зима малосніжна, періоди морозів чергуються із тривалими відлигами, які можуть спричинити несвоєчасне пробудження ростової активності, розпускання листових і квіткових бруньок рослин-інтродуцентів і ушкодження їх морозами. Відзначаються осінні й весняні заморозки, які згубно впливають на деякі рослини, особливо молоді [92]. Літо: спекотне, часті суховії. Середня температура найтеплішого місяця (липня) становить +22 °С, максимальна досягає +37...+40 °С. За рік у середньому випадає 410-490 мм опадів, при цьому на теплий період року припадає до 65% загальної кількості опадів (300-350 мм), найчастіше у вигляді короткочасних злив. В окремі роки тривалий бездощовий період супроводжується повітряною посухою, що нерідко призводить до ґрунтової посухи [93].
За даними клімадіаграм, наведених на рис.3.1, в період проведення
дослідження спостерігалося істотне підвищення температури атмосферного повітря
навесні і на початку літа та суттєве зниження температури у вересні - жовтні
порівняно зі спостереженнями клімату в період з 1991 по 2014 рр., а саме -
відхилення від норм в межах від -5,4°С до + 3,0°С (залежно від місяця), що
значно вплинуло на стан глутатіонової системив насінні деревних рослин як у
контрольній зоні, так і на дослідних ділянках. Кількість опадів у червні -
липні та у вересні - жовтні різко зменшилась - на 28% порівняно з минулими
роками.
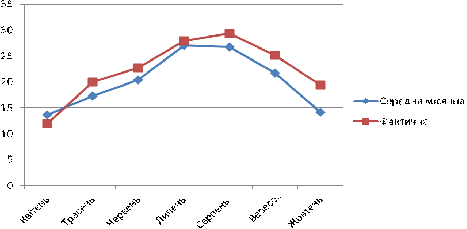
А - температурна крива
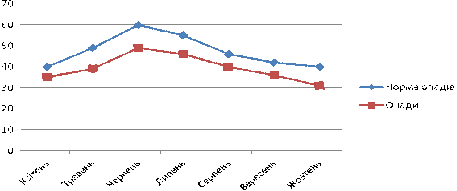
Б - крива змін кількості опадів
Рис. 3.1. Клімадіаграми за даними метеоцентру м. Дніпропетровськ (2014
р.)
Таким чином, під час польового дослідження для існування рослин склалося
екстремальне сполучення погодних умов - високих температур і значної посухи
[93]. Оскільки таке поєднання абіотичних факторів середовища спостерігалося і в
районах пр. Кірова, вул. Героїв Сталінграду, пр. Правди м. Дніпропетровськ, а
такожу районі Ботанічного саду ДНУ, всі відмінності в значеннях біохімічних
показників між контрольними та дослідними рослинами зумовлені лише дією
антропогенного навантаження.