Материал: В-Л-Быков-Цитогогия_и_общая_гистология
нием клеток. В нем располагается сосудистая сеть, питающая хрящ, а также камбиальные элементы - прехондробласты, которые морфологически имеют признаки покоящихся малодифференцированных клеток, способных активироваться, пролиферировать и дифференцироваться в хондробласты при соответствующей стимуляции. Образование хондробластов в этом слое обеспечивает аппозиционный рост хряща в эмбриональном периоде и в детском возрасте. У взрослого по завершении роста хряща сигналом к активации камбиальных элементов обычно служит повреждение надхрящницы.
Зональность строения хряща
Вхряще (как органе) выявляются два нерезко разграниченные слоя (зоны),
впределах каждого из которых хрящевая ткань характеризуется рядом морфологических, биохимических и функциональных особенностей (см. рис.
12-5):
(1)зона молодого хряща располагается в виде сравнительно тонкого слоя непосредственно под надхрящницей. Она состоит из уплощенных молодых хондроцитов, лежащих поодиночке параллельно поверхности хряща, которые окружены гомогенным оксифильным матриксом.
(2)зона зрелого хряща образует его основную массу и располагается глубже предыдущей. В области плавного перехода из зоны молодого хряща хондроциты в ней становятся более округлыми, еще глубже они располагаются
ввиде изогенных групп, а матрикс приобретает базофилию и разделяется на территориальный и интертерриториальный (см. выше).
Регрессивные изменения хряща
Регрессивные изменения хряща в наибольшей степени затрагивают гиалиновый хрящ, тогда как эластический и волокнистый хрящи сравнительно устойчивы к повреждениям и мало меняются при старении. Проявлением регрессивных изменений хряща служит его обызвествление (кальцинация, или минерализация), которое отмечается в ходе развития костей (когда дегенеративно измененная хрящевая ткань замещается костной), а также при старении.
Механизмы обызвествление хряща. В отличие от прежних представлений, рассматривающих минерализацию хряща как вторичное,
- 356 -
сугубо пассивное явление, в настоящее время получены свидетельства об активной роли самих хондроцитов в этом процессе. Минерализации предшествуют характерные изменения матрикса и клеток хряща. Матрикс утрачивает базофилию, клетки набухают и увеличиваются в размерах (повидимому, вследствие изменения осмотического равновесия), получая название гипертрофированных, или пузырчатых хондроцитов.
Гипертрофированные (пузырчатые) хондроциты характеризуются сначала набухшими, в дальнейшем пикнотизирующимися ядрами, вакуолизированной цитоплазмой с большими скоплениями гликогена и резко расширенными цистернами грЭПС. содержащими синтезированные продукты. Эти клетки обеспечивают последующую минерализацию хряща благодаря тому, что они: (1) продуцируют ряд веществ (крупные агрегаты протеогликанов и С- пропептид коллагена II типа), которые, накапливаясь локально в больших концентрациях, способствуют связыванию кальция и росту кристаллов гидроксиапатита; (2) секретируют матричные пузырьки.
Матричные пузырьки - мелкие (около 100-200 нм) округлые мембранные образования, которые отделяются от поверхности гипертрофированных хондроцитов и обнаруживаются в межклеточном веществе и участках минерализации хряща. Они участвуют в процессе обызвествления межклеточного вещества хрящевой ткани, подобно тому, как матричные пузырьки, продуцируемые остеобластами, обеспечивают обызвествление межклеточного вещества костной ткани (см. ниже). Матричные пузырьки благодаря ассоциированным с мембраной ферментам и липидам обладают способностью связывать и накапливать кальций, поэтому они содержат высокие концентрации минеральных соединений и являются участками отложения первых кристаллов солей кальция в межклеточном веществе хряща (в виде гидроксиапатитов).
Изменения хряща при обызвествлении. По мере роста кристалов и слияния обызвествленных участков матрикса хрящ утрачивает прозрачность и становится твердым и хрупким. Базофилия матрикса начала теряется, а с обызвествлением усиливается. Хондроциты постепенно гибнут и исчезают вследствие нарушения диффузии питательных веществ через минерализующийся матрикс. Обызвествленный хрящ обычно разрушается хондрокластами - многоядерными клетками типа остеокластов.
Репаративная регенерация хряща
Регенерация хряща при его повреждении может осуществляться благодаря наличию камбиальных элементов в надхрящнице. Содержа-
- 357 -
щиеся в надхрящнице прехондробласты активируются, пролиферируют и дифференцируются в хондробласты, которые вырабатывают межклеточное вещество хряща, постепенно заполняющее образовавшийся дефект. Однако практически полноценная регенерация наблюдается лишь при небольших повреждениях хряща в детском возрасте. У взрослого регенерацию хрящевой ткани опережает развитие волокнистой соединительной ткани, происходящей из надхрящницы, которая быстро заполняет дефект хрящевой ткани, со временем превращаясь из рыхлой волокнистой ткани в плотную (рубец). Иногда в этом участке соединительной ткани развивается костная ткань. Такое заживление, хотя и обеспечивает связывание неповрежденных участков хряща, неполноценно и при нагрузках может привести к повторному разрыву хряща по линии рубца.
Хрящ как объект трансплантации и тканевой инженерии
В связи с низкой проницаемостью матрикса хряща для макромолекул и отсутствием сосудов он относительно инертен иммунологически и благодаря этому считается удачным объектом для трансплантации. Разработка методов трансплантации хряща ориентирована, в первую очередь, на возможность замены поврежденного суставного хряща (см. ниже), поскольку поражения суставов относятся к одним из наиболее распространенных заболеваний человека. При операциях трансплантации суставного хряща используют приемы как аутопластики (пересадки собственного хряща после его удаления из другого места и придания ему необходимой формы), так и аллопластики (использования донорской, в частности, трупной ткани). В последние годы с целью получения необходимого материала для хрящевых имплантатов широкое применение нашли методы тканевой инженерии: разработаны приемы выращивания хрящевых фрагментов нужных размеров с необходимыми механическими свойствами в искусственных строго контролируемых условиях.
КОСТНЫЕ ТКАНИ
Костные ткани образуют скелет, защищающий внутренние органы от повреждений, входящий в локомоторный аппарат и являющийся важнейшим депо минеральных веществ в организме (содержат около 1200 г Са - 99% его запасов в организме - и 530 г Р).
- 358 -
Общие принципы структурно-функциональной организации костных тканей
Костная ткань образована клетками и обызвествленным межклеточным веществом (матриксом). Примерно 67% ее массы приходится на минеральные компоненты (придающие ей высокую прочность), 33% - на органические (обеспечивающие необходимый уровень пластичности).
Клетки костной ткани включают остеобласты, остеоциты и остеокласты (рис. 12-6). Остеокласты происходят из стволовой клетки крови; остальные клетки развиваются в последовательности:
остеогенные клетки-предшественники -> остеобласты -> остеоциты
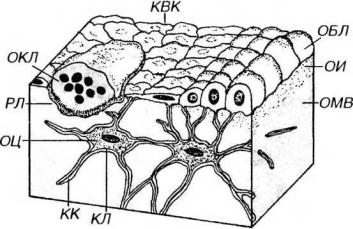
Рис. 12-6. Клетки костной ткани. ОБЛ - остеобласты (активные), КВК - клетки, выстилающие кость (неактивные остеобласты), КЛ - костные лакуны с телами остеоцитов (ОЦ), КК - костные канальцы, содержащие отростки ОЦ, ОКЛ - остеокласт резорбционной лакуне (РЛ), ОИ - остеоид, ОМВ - обызвествленное межклеточное вещество.
Остеогенные клетки-предшественники - малодифференцированные клетки мезенхимного происхождения, которые способны дифференцироваться в остеобласты. Они очень многочисленны в ходе развития костей у плода и имеют вид отростчатых клеток с крупным светлым ядром. Эти клетки встречаются и в соединительных тканях взрослого организма, где они имеют мелкие размеры, веретеновидную форму и слабо развитые органеллы; они могут находиться также в пе-
- 359 -
риферической крови. Их превращение в остеобласты происходит под индуцирующим воздействием ряда факторов, из которых наиболее изучена группа костных морфогенетических белков (КМБ).
Остеобласты - метки, образующие костную ткань. Они синтезируют и секретируют неминерализованное межклеточное вещество (матрикс) кости (остеоид), участвуют в его обызвествлении, регулируют поток кальция и фосфора в костную ткань и из нее. Различают активную и неактивную формы остеобластов.
Активные остеобласты - кубические или призматические клетки, связанные тонкими отростками с другими клеточными элементами - клеткамипредшественниками, соседними остеобластами и остеоцитами (см. рис. 12-6). Округлое ядро с крупным ядрышком удалено от полюса, контактирующего с поверхностью костного матрикса. Цитоплазма характеризуется выраженной базофилией; на ультраструктурном уровне ей свойственна отчетливая полярность. Она содержит мощно развитый синтетический аппарат (включающий множественные цистерны грЭПС, часто растянутые, крупный комплекс Гольджи), большое число митохондрий, пузырьков (рис. 12-7). На ее поверхности находятся многочисленные микроворсинки. Эти клетки покрывают в норме 2-8% поверхности кости.
Продукты, синтезируемые и секретируемые остеобластами в составе органического матрикса костной ткани (остеоида): коллаген I типа (90% всех образуемых ими белков), в небольшом количестве коллагены других типов - III, IV, V, XI, XIII - (5% белков), ряд неколлагеновых белков - гликопротеины матрикса (остеонектин, костный сиалопротеин, остеопонтин, остеокальцин), протеогликаны (бигликан, декорин, гиалуроновая кислота). Остеобласты продуцируют также цитокины, различные факторы роста, костные морфогенетические белки, ферменты (щелочную фосфатазу, коллагеназу), фосфопротеины (фосфорины).
Нарушение синтеза остеоида остеобластами наблюдается при ряде заболеваний. Так, выработка химически измененного коллагена остеоида (вследствие мутаций кодирующих его генов), вызывающая нарушение нормального процесса формирования костной ткани, обнаруживается при ряде врожденных заболеваний, проявляющихся ломкостью костей, например, различных формах несовершенного остеогенеза (osteogenesis imperfecta). Дефицит витамина С (цинга) у детей характеризуется нарушением формирования и роста костей вследствие дефекта синтеза коллагена н гликозаминогликанов. По этой же причине при цинге затрудняется заживление переломов костей.
- 360 -