Материал: Соединения свинца (II) в системе почва-растения
В почве подавляющая часть свинца находится в виде твёрдых соединений. Рекомендуемые в литературе методики, позволяют выделить лишь некоторые условные фракции свинца, которые нельзя отнести к каким-то определенным химическим соединениям.
В целом, они дают всё же основание полагать, что в кислых почвах существует часть свинца, вплоть до 70%, способная действительно обмениваться на другие ионы; в нейтральных почвах преобладают фракции, связанные с оксидами железа, марганца и органическим веществом, а в слабощелочных и щелочных условиях свинец распределён между «карбонатной», «органической» и «остаточной» фракциями. Тем не менее, химический состав и свойства соединений, присутствие которых обусловливает наличие элемента в этих «фракциях», остаются неясным [5].
Само по себе «фракционирование» сравнительно
малоинформативно. Твёрдые соединения свинца в почвах находятся во
взаимодействии с почвенным раствором, через который происходит как поступление
элемента в растения, так и внутрипочвенная миграция, и трансформация его
соединений. Характер связывания свинца в твёрдых составляющих, очевидно, и
определяет его концентрацию в растворе, которая должна, таким образом, отражать
свойства соединений, в которых находится свинец. Чтобы понять причины появления
свинца в почвенном растворе, необходимо проанализировать свойства соединений
этого элемента, которые могли бы присутствовать в почвах, и возможные механизмы
его связывания[3].
.4 Почва как полифункциональный сорбент
Почва - это полифункциональный сорбент, гетерогенная четырехфазная система (жидкая, твердая, газообразная фазы и живые организмы). С увеличением почвенной кислотности способность почв адсорбировать тяжелые металлы снижается. Влияние кислотности на величину адсорбции обусловлено несколькими процессами, протекание которых зависит от реакции среды: гидролизом тяжелых металлов, специфической адсорбцией тяжелых металлов на илистых частицах.
На адсорбцию сильно влияет органическое вещество
почвы. Так адсорбции тяжелых металлов гумусом происходит с участием
карбоксильных и фенольных групп, путем замещение водорода на ионы металла. При
этом образуются хелаты, в которых металл входит в анионную часть молекул
органического вещества. В этом случае металл соединен координационными
(гомеополярными) связями и не проявляет себя как катион. Комплекс также может
металл в обмен на катион водорода во вне функциональных группах. Следовательно,
металлы могут входить как в катионную, так и в анионную части молекул гумусовых
кислот. Использование логарифмической формулы Фрейндлиха для описания процессов
адсорбции тяжелых металлов почвами также позволяет обнаружить на изотермах
наличие двух и более контрастно адсорбции.
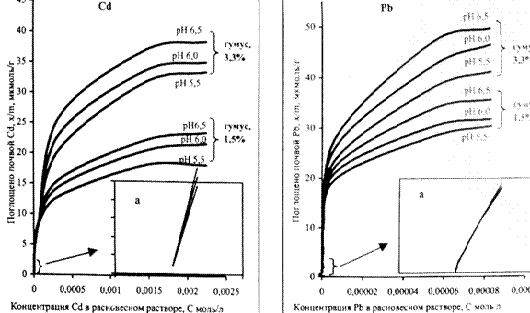
Рисунок 2 - Изотермы адсорбции свинца
дерново-подзолистой почв
Разделение изотерм адсорбции на два участка с энергетической гетерогенностью адсорбционных мест и указывает на наличие в почве двух и более групп обменных центров. Наличие нескольких групп обменных центров, обладающих не одинаковым сродством к тяжелым металлам, свидетельствует о, что часть катионов адсорбируется почвой специфически, а часть неспецефически. На эти процессы влияет кислотность почвы. При низких концентрациях заполняются места с более высокой энергией связи, т. е имеет место специфическая адсорбция. С увеличением концентрации тяжелых металлов происходит неспецифическая адсорбция, заполняются места с более низкой энергией связи.
Содержание гумуса в большей степени влияет на специфическую адсорбцию, чем кислотность. Так с увеличением содержания в почве гумуса с 1.5 - 3.3% наблюдается увеличение специфической адсорбции кадмия и цинка на 7 - 9%,а свинца на 12%. При этом доля максимального количества специфически поглощенных тяжелых металлов от ЕКО снижается. Установлено, что специфическая адсорбция металлов в большей степени зависит от генетических особенностей почвы (гранулометрического и минерального состава, содержания полуторных гидроксидов железа, алюминия и марганца, чем от их агрохимических свойств. Было доказано, что максимальное количество элементов, адсорбируемых специфически, изменяется в ряду Pb2+, Zn2+, Cd2+ [3].
Свинец по сравнению с другими металлами в больших количествах поглощается и удерживается почвой. Отношение максимальной сорбции свинца к ЕКО находится в пределах 31 - 58%,в то время как для цинка и кадмия такой показатель равен 25 - 46 и 17 - 32% соответственно. Этим и объясняется малая подвижность в почве свинца. При этом с уменьшением кислотности и увеличением содержании гумуса максимальное количество поглощенных металлов, отнесенное к общему количеству ионов в ППК, способных к обмену, снижается, что может быть связано с возрастанием конкуренции за адсорбционные места в ППК.
Показано что поглощение свинца черноземом,
серой-лесной и дерново-подзолистой почвой при рН 4.5 и 6 сопровождается
вытеснением в раствор не только иона кальция, но и иона водорода, и
представляет собой не бинарный, а трехкатионный ионный обмен. Этот обмен
является обратимым процессом. При рН 6 и выше вступает в действие и начинает
превалировать другой механизм поглощения Pb2+ осаждение карбоната свинца.
Поведение Pb2+ в почвах и его доступность растениям зависит от того, насколько
прочно он связан и насколько легко может быть высвобожден в раствор под
влиянием тех или иных воздействий [5].
.5 Влияние соединений свинца на организм
человека
Свинец - это тяжелый металл, токсичен, токсичная доза 1-3 г,
смертельная доза для человека 10 г, является канцерогеном. Попадает в
организм через пищевод, дыхательные пути, кожу, накапливается в организме и трудно оттуда выводится, при постоянной работе с ним будут появляться различные заболевания, связанные с токсичностью свинца.
Во всем мире вредное воздействие свинца на здоровье человека в результате свинцового загрязнения окружающей среды, повышенных концентраций свинца на рабочем месте и в быту обходится человечеству невероятно дорого, вызывая распространение свинцовой интоксикации среди взрослых и детей, впоследствии долгие годы страдающих от тяжелых хронических заболеваний. Только в тех странах, где в силу специфических обстоятельств или действующего законодательства применение свинецсодержащих материалов было ограничено или находилось под контролем, проблема свинцового отравления может рассматриваться как имеющая второстепенное значение [7].
Из-за широкого распространения свинцового загрязнения практически все население подвергается риску его воздействия независимо от социально-экономического статуса, расовой и этнической принадлежности или места проживания (сельская местность, город или пригород). Однако большинство случаев свинцового отравления остаются нераспознанными, поскольку при низких дозах интоксикации явные симптомы проявляются только у небольшого процента пострадавших. За исключением высоких доз свинцовое отравление очень трудно или невозможно диагностировать без данных анализов крови. Дети дошкольного возраста наиболее восприимчивы к вредному воздействию свинца, поскольку их нервная система находится в стадии формирования [8].
Согласно современным медицинским представлениям, в организме ребенка вполне допустимо содержание свинца до 10 микрограммов на каждый децилитр крови. Даже при низких дозах свинцовое отравление вызывает снижение интеллектуального развития, внимания и умения сосредоточиться, отставание в чтении, ведет к развитию агрессивности, гиперактивности и другим проблемам в поведении ребенка. Эти отклонения в развитии могут носить длительный характер и быть необратимыми. Низкий вес при рождении, отставание в росте и потеря слуха также являются результатом свинцового отравления. Высокие дозы интоксикации ведут к умственной отсталости, вызывают кому, конвульсии и смерть. Вредное воздействие свинца на здоровье взрослых проявляется в повышении кровяного давления, нарушении деятельности нервной системы, печени, почек, снижении репродуктивной функции. Большая часть свинца поступает в организм человека с продуктами питания, а также с водой и пылевыми аэрозолями.
Наиболее опасным является попадание свинца с пылевыми аэрозолями от загрязненных почв. Свинец, попадая в организм, через несколько минут проникает в клетки крови и быстро связывается с эритроцитами, в которых содержание свинца в 16 раз выше, чем в плазме крови. Депонируется в костной системе, включая зубы. Свинец является конкурентным биометаллом по отношению к Ca и может его вытеснить из избирательных мест связывания с фосфатными, карбоксильными и сульфатными лигандами в тканях и на клеточных мембранах, реализуя его повреждающее действие через нарушение пассивного транспорта кальция [6].
Поражает все внутренние органы, в том числе почки. На фоне длительного контакта со свинцом развиваются нарушения функционального состояния почек, заканчивающиеся необратимой хронической нефропатией. Повышенные уровни свинца в крови представляют особую опасность для беременных женщин, поскольку свинец свободно проникает через плаценту, оказывая отравляющее действие на плод. Свинец, накопленный в костных тканях еще в детском возрасте, выделяется обратно в кровь во время беременности, угрожая здоровью матери и ребенка.
В медицине известно, что свинец негативно влияет на нервную систему человека и, в частности, на поведение, однако вред, нанесенный этим металлом, легко может быть исправлен. В кровь свинец попадает через дыхательные пути или же через слизистую оболочку рта.
Несмотря на то, что применение медикаментозного метода лечения (так называемой хелатотерапии) способствует выведению свинца из организма, такие препараты дороги, имеют побочные эффекты, а само лечение - болезненно.
Кроме того, они применимы только к пациентам с
высокими дозами интоксикакации и не вылечивают неврологические заболевания,
развившиеся в результате предшествующего отравления свинцом. Единственно
надежным лекарством против свинцовой интоксикации является её предотвращение -
контроль источников свинцового загрязнения до того, как они произвели свое
разрушительное действие на здоровье человека [8].
.6 Методы обнаружения и количественного
определения соединений свинца в природных объектах
Для нахождения соединений тяжелых металлов, в частности соединений свинца, используют следующие методы определения: физико-химические методы (масс-спектрометрия, фотометрия, атомно-адсорбционный метод и др.), электро-химические методы (кулонометрия, потенциометрия, вольтамперометрия и др.).
Масс-спектрометрия. Масс-спектрометрия (масс-спектроскопия, масс-спектрография, масс-спектральный анализ, масс-спектрометрический анализ) метод исследования вещества путём определения отношения массы к заряду (качества) и количества заряженных частиц, образующихся при том или ином процессе воздействия на вещество [11].
Атомно-абсорбционный метод. Атомно-абсорбционный спектральный метод анализа среди новейших физико-химических методов исследования нужно назвать атомно-абсорбционный анализ. Этим методом можно производить количественное определение большей части элементов периодической системы в различных объектах внешней среды, не прибегая при анализе микро- и макроэлементов к предварительному разделению определяемых элементов или к отделению мешающих примесей, что влечет за собой увеличение погрешности определения и увеличение его трудоемкости. Атомно-абсорбционный спектральный анализ характеризуется высокой избирательностью. Он отличается от длительного и кропотливого химического метода быстротой определения, более простым приготовлением образцов, точностью и чувствительностью. Принцип атомно-абсорбционного спектрального анализа основан на способности атомов металлов поглощать свет характеристических длин волн. Характеристические длины волн составляют линейчатый эмиссионный спектр, определенный для каждого элемента. Свет от источника резонансного излучения поглощается свободными атомами, проходя через атомный пар, образованный путем испарения и диссоциации соединения определяемых элементов, вводимых в пламя в виде аэрозоля.
Наибольшее распространение получил пламенный способ испарения и атомизации соединений определяемых элементов, хотя в принципе, с успехом могут быть использованы и другие способы. Например: испарение пробы из графитовой кюветы, нагретой до высокой температуры, испарение и создание свободных атомов при помощи квантового или плазменного генератора, а также распыление и атомизация исследуемой пробы в полом катоде. Все способы получения поглощающих слоев можно отнести к двум группам: равновесным и импульсным. По чувствительности импульсные методы (графитовая кювета, импульсная лампа, лазерный луч) должны превосходить равновесные (пламя, разряд в полом катоде, печь Кинга), т.к. для достижения и поддержания равновесной концентрации элемента в поглощающей ячейке требуется значительно большее количество вещества по сравнению с тем, которое сосредоточено в поглощающей ячейке в каждый момент. При импульсном испарении пробы для создания концентрации паров в ячейке, равной равновесной, потребовалось бы в 3·104 раза меньшее количество веществ, чем в пламени. Но техника регистрации спектров поглощения при импульсном испарении сложнее, чем для равновесных методов, так как в первом случае необходимо регистрировать быстро изменяющийся сигнал, а во втором - постоянный. Поглощение света атомным паром подчиняется закону Бугера-Ламберта-Бера.
Ввиду того, что атомное поглощение соответствует переходам атомов из более низких в более высокие энергетические состояния, величина поглощения зависит от заселенности нижнего уровня, соответствующего наблюдаемой линии. Заселенность возбужденных уровней незначительна по сравнению с заселенностью нижнего уровня, поэтому наибольшее поглощение наблюдается для линий, соответствующих поглощательным переходам с нижнего невозбужденного уровня. Эти линии в атомно-абсорбционном анализе называют резонансными.
Для многих элементов силы осцилляторов спектральных линий измерены, поэтому выбор наиболее чувствительных линий не представляет труда. Когда величины сил осцилляторов в спектре элемента неизвестны, можно экспериментально выбрать наиболее чувствительные линии. В результате экспериментальных исследований установлено, что наиболее чувствительные в поглощении линии часто не совпадают с наиболее интенсивными атомными линиями элементов в эмиссионном спектральном анализе, в том числе и в пламенной фотометрии. Объясняется это тем, что интенсивность излучения резонансных линий зависит от участка спектра. Изменение интенсивности при температурах пламени или дугового разряда практически обусловлено экспоненциальным множителем, определяющим участок спектра, поэтому интенсивность излучения быстро падает в короткую область спектра.
Таким образом, эмиссионный спектр имеет иное распределение резонансных линий по интенсивности, чем спектр поглощения. Более интенсивными в испускании являются резонансные линии с большей длинной волны; более чувствительные в поглощении линии лежат в коротковолновой стороне от наиболее интенсивной в испускании резонансной линии (или совпадают с ней). Для большинства элементов, кроме газов, галогенов и некоторых неметаллов, наиболее интенсивные резонансные линии расположены в видимой и ультрафиолетовой областях спектра, легко доступных для измерении [13].
Фотометрический метод. Общие положения. Метод анализа, основанный на сравнении качественного и количественного изменения световых потоков при их прохождении через исследуемый и стандартный растворы, называется фотометрическим. Обычно в ходе анализа измеряют ослабление светового потока, которое происходит вследствие избирательного поглощения света определяемым веществом. В зависимости от используемой аппаратуры в
фотометрическом анализе различают:
спектрофотометрический метод - анализ по поглощению монохроматического света (все волны имеют одинаковую длину волны);
фотоколориметрический метод - анализ по поглощению полихроматического света.
Сущность метода. Определяемый компонент при помощи химической реакции переводят в окрашенное соединение, после чего каким-либо инструментальным или визуальным способом измеряют интенсивность окраски полученного раствора. Таким образом, в колориметрии играют существенную роль, во-первых, правильно выбранные условия протекания химической реакции по переводу определяемого компонента в окрашенный раствор и, во-вторых, знание оптических свойств окрашенных растворов, что позволяет правильно выбрать способ измерения интенсивности окраски [11].