Материал: Соединения свинца (II) в системе почва-растения
Соединения свинца (II) в системе почва-растения
Министерство образования Республики Беларусь
Учреждение образования
«Гомельский государственный университет имени Франциска Скорины»
Биологический факультет
Кафедра
химии
Курсовая работа
Соединения
свинца (II) в системе почва - растения
Исполнитель: студент группы Б-34
Р.Л. Дегтярёв
Научный руководитель: к.х.н., доцент
А.В.
Хаданович
Гомель
2013
Введение
В последние десятилетия в связи с быстрым развитием промышленности во всем мире усиливается загрязнение окружающей среды тяжелыми металлами в масштабах, которые не свойственны природе. В силу этого возрастание их содержания в окружающей среде становится серьезной экологической проблемой современности [1].
Тяжелые металлы - химические вещества, с металлическими свойствами, имеющие относительно большую плотность при малой концентрации, обладающие аккумулятивной способностью.
Загрязнение окружающей среды, в особенности тяжелыми металлами - один из наиболее сильных факторов разрушения компонентов биосферы. Потребление энергии и минеральных ресурсов человеком - главная причина загрязнения биосферы тяжёлыми металлами. Следовательно, исследования в этой области являются важной актуальной задачей [3].
Значительное увеличение содержания тяжелых металлов в окружающей среде сопровождается их накоплением в растениях, что оказывает негативное влияние на рост, развитие и продуктивность. В связи с этим изучение реакции растений на действие тяжелых металлов вызывает не только большой научный, но и практический интерес [4].
Потребление энергии и минеральных ресурсов
человеком - главная причина загрязнения биосферы тяжёлыми металлами. Тяжёлые
металлы, выделяющиеся из антропогенных источников, поступают в окружающую среду
и вовлекаются в нормальные биогеохимические циклы. Исследование переноса,
времени пребывания и судьбы загрязнений в каждой экосистеме представляет собой
специальную задачу охраны окружающей среды. Поведение тяжёлых металлов в любой
экосистеме очень сложно, и поэтому обычно оно изучается раздельно в воздухе,
воде, почве и живых организмах.
1. Пути поступления тяжелых металлов в почву
В последние десятилетия человек стал причиной быстрой деградации почв, хотя потери почв имели место на протяжении всей человеческой истории. Насчитывают не менее 6 типов антропогенно-технических воздействий, которые могут вызвать разного уровня ухудшение почв. В их числе:
) водная и ветровая эрозия.
) засоление, подщелачивание, подкисление.
) заболачивание.
) физическая деградация, включая уплотнение и коркообразование.
) разрушение и отчуждение почвы при строительстве, добыче полезных ископаемых.
) химическое загрязнение почв.
Одним из типов антропогенно-технических воздействий является загрязнения почвы тяжелыми металлами. Этот вид загрязняющих веществ начали изучать одним из первых. К тяжелым металлам обычно относят элементы, которые имеют атомную массу более 50. Из атмосферы в почву тяжелые металлы попадают чаще всего в форме оксидов, где постепенно растворяются, переходя в гидрооксиды, карбонаты или в форму обменных катионов. Если почва прочно связывает тяжелые металлы (обычно в богатых гумусом тяжелосуглинистых и глинистых почвах), это предохраняет от загрязнения грунтовые и питьевые воды, растительную продукцию. Но тогда сама почва постепенно становится все более загрязненной и в какой-то момент может произойти разрушение органического вещества почвы с выбросом тяжелых металлов в почвенный раствор. В итоге такая почва окажется непригодной для сельскохозяйственного использования. Общее количество свинца, которое может задержать метровый слой почвы на одном гектаре, достигает 500 - 600 т; такого количества свинца даже при очень сильном загрязнении в обычной обстановке не бывает. Почвы песчаные, малогумусные, устойчивы против загрязнения; это значит, что они слабо связывают тяжелые металлы, легко отдают их растениям или пропускают их через себя с фильтрующимися водами. На таких почвах возрастает опасность загрязнения растений и подземных вод. В этом заключается одно из трудноразрешимых противоречий: легко загрязняющиеся почвы предохраняют окружающую среду, но почвы, устойчивые к загрязнению, не обладают защитными свойствами в отношении живых организмов и природных вод.
Источники эмиссии тяжелых металлов и пути их проникновения в окружающую среду весьма разнообразны, они могут носить как природный, так и антропогенный характер. Большинство тяжелых металлов поступает в окружающую среду в результате деятельности человека. Источником природной эмиссии тяжелых металлов в окружающую среду является извержение вулканов, лесные пожары, морская вода и др. Главные антропогенные источники поступления тяжелых металлов в биосферу - топливные электростанции, предприятия по добычи и переработке цветных металлов, транспорт, машино-строительство, химическая промышленность, сельскохозяйственное производство. При этом общая масса металлов, поступающих от природных источников значительно ниже, чем от антропогенных: свинца в 17,2 раза, кадмия - 8,8, цинка - 7,2. Техногенное поступление тяжелых металлов в окружающую среду происходит в виде пыли газов и аэрозолей (возгонка металлов промышленных предприятий и автотранспорта), в составе сточных вод бытовых отходов.
свинец почва сорбент природный
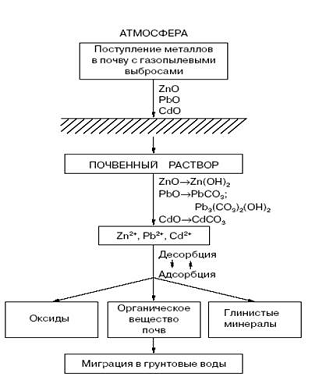
Рисунок 1 - Трансформация и миграция тяжелых
металлов в почве [5]
Загрязнение тяжелыми металлами может происходить и за счет сельского хозяйства, основными источниками которого является: использование в качестве удобрений сточных вод и их осадков, примеси тяжелых металлов в удобрениях (например, кадмий и уран в фосфорных удобрениях), использование пестицидов, отходы интенсивного птицеводства и животноводства. Так из всех используемых в сельском хозяйстве удобрений самыми загрязненными являются фосфорные. Основным загрязнителем в них является кадмий. Исследования показали, что тяжелые металлы в удобрениях находятся в виде примесей, максимальное их количество находится в фосфорных удобрениях и доломитовой муке.
Таким образом, уровни содержания тяжелых металлов в почвах агроэкосистем формируется под воздействием антропогенных и природных факторов. Тяжелые металлы, прежде всего, накапливаются в почвенном покрове, где они распределяются между твердой и жидкой фазой почвы. В одной и тоже почве металлы могут находиться в разной по растворимости и подвижности формах. От того, как сильно тяжелые металлы поглощаются и удерживаются почвой и в, какой форме находятся, зависит их фототаксичность и аккумуляция в растениях.
Если основной формой загрязнителя в почве является малоподвижная или неподвижная (в поглощенном состоянии, в виде нерастворимых или труднорастворимых соединений), угроза проявления токсических свойств металлов будет минимальна и наоборот. В свою очередь, свойства почвы определяют прочность фиксации соединений элементов и ее буферную способность по отношению к тяжелым металлам, влияют на токсичность для растений. Чем больше и прочнее почва удерживает тяжелые металлы, тем активнее они удаляются из почвенного раствора в состав соединений твердой фазы. Поэтому изучение закономерностей поведения тяжелых металлов в почве и выявление факторов, влияющих на эти процессы, имеет важное агроэкологическое значение [10].
Поэтому в изучении путей поступления тяжелых металлов в почву имеет важное научно-практическое значение. Если почвы загрязнены тяжелыми металлами и радионуклидами, то очистить их практически невозможно. Пока известен единственный путь: засеять такие почвы быстрорастущими культурами, дающими большую зеленую массу; такие культуры извлекают из почвы токсичные элементы, а затем собранный урожай подлежит уничтожению. Но это довольно длительная и дорогостоящая процедура. Можно снизить подвижность токсичных соединений и поступление их в растения, если повысить рН почв известкованием или добавлять большие дозы органических веществ, например торфа. Неплохой эффект может дать глубокая вспашка, когда верхний загрязненный слой почвы при вспашке опускают на глубину 50 - 70 см, а глубокие слои почвы поднимают на поверхность. Для этого можно воспользоваться специальными многоярусными плугами, но при этом глубокие слои все равно остаются загрязненными.
Наконец, на загрязненных тяжелыми металлами (но
не радионуклидами) почвах можно выращивать культуры, не используемые в качестве
продовольствия или кормов, например цветы [3].
.1 Физико-химические оценки механизмов
поглощения свинца (II)
В качестве механизмов связывания свинца называют осаждение его малорастворимых солей и обменное или необменное поглощение гидроксидами металлов, силикатами и органическим веществом почв. К малорастворимым соединениям свинца относят природные минералы, основными из которых является галенит (PbS), встречающийся во многих районах земного шара, а так же рудные минералы англезит (PbSO4), церуссит (PbCO3), пироморфит (PbCl2*3Pb3(PO4)2) и милитезит (PbCl2*3Pb3(AsJ4)3). Эти соединения, очевидно, и попадают в почвы вблизи разработок рудных месторождений. Металлический свинец сравнительно устойчив к воздействию природных факторов, поскольку под влиянием воздуха и паров воды на его поверхности образуется плёнка оксикарбоната, защищающая металл от дальнейшего окисления. Воздействие воды, содержащей растворённый кислород, приводит к образованию гидроксидов свинца, растворение которых и делает воду токсичной.
Оксид свинца (II) образуется при нагревании металла на воздухе. Другими оксидами являются Pb6O2 и Pb3O4. Первый из них входит в состав пластин свинцовых аккумуляторов, второй используют в качестве пигмента красок. В щелочных растворах образуются гидроксокомплексы [Pb4(OH)4]4+, [Pb2(OH)]3+, [Pb3(OH)4]2+, [Pb(OH)]+, [Pb6(OH)8]4+, [Pb(OH)2]0.
Нитрат свинца хорошо растворим в воде, но при его диссоциации в воде образуется стабильный комплекс. Оксигалиды свинца Pb2OCl2, Pb3O2CI2, Pb3OCl4 известны как минералы.
Гидрофосфат (PbHPO4) образует малорастворимый в воде минерал монетит. Соединения с общей формулой [3 Pb3(PO4)2 * PbX2], где X - Сl, Br или OH называют апатитами свинца. Хлорапатит свинца встречается в природе в виде минерала хлоропироморфита (Pb5(PO4)3Сl). Карбонат PbCO3 является одним из наименее растворимых соединений свинца. В природе он встречается в виде минерала церуссита. Растворимость его заметно возрастает в присутствии растворимого в воде углекислого газа. Ещё менее растворим сульфид свинца - галенит. На воздухе он постепенно окисляется, в результате чего при нахождении сульфидной руды на воздухе галенит постепенно покрывается сначала коркой англезита PbSO4, который затем с поверхности переходит в церуссит. Растворимость некоторых соединений свинца и их произведения растворимости.
Исходя из этих данных можно сделать вывод о том,
что в жидкой фазе почв концентрацию элемента могли бы контролировать только
карбонат, сульфид и пироморфит свинца. Наличие в почвах кальцита, концентрация
которого существенно выше, чем у церуссита, приводит к появлению в почвенном
растворе ионов карбонатов и гидрокарбанатов в концентрациях, достаточных для
осаждения ионов свинца из раствора. Таким образом, в карбонатных почвах
связывание ионов свинца происходит за счёт осаждения церуссита.
Таблица 1 - Растворимость некоторых соединений свинца (II) в воде
|
соединение |
Растворимость, мг/л |
-lg, моль/л |
ПР |
t,С |
|
Pb(OH)2 |
11,4 |
5,5*10 |
15 |
18 |
|
PbCO3 |
0,037 |
6,2*10 |
13,48 |
25 |
|
PbS |
6*10 |
2,8*10 |
27,1 |
25 |
|
PbHPO4 |
2,3 |
1,8*10 |
9,92 |
25 |
|
PbSO4 |
37 |
7,8 |
25 |
|
|
Pb5(PO4)3Cl |
1*10 |
5*10 |
83,7 |
25 |
Альтернативным механизмом поглощения свинца является обменное или необменное поглощение свинца (II) оксидами - гидроксидами Fe и Mn, глинистыми минералами и органическим веществом почв. В условиях лабораторного эксперимента исследователи установили, что оксидами - гидроксидами железа в интервале рН от 3,5 до 5,5 практически полностью поглощают ионы свинца из раствора.
Оксиды Mn так же связывают растворённый свинец, рН влияет на этот процесс в существенно меньшей степени. Практически не оказывает на него влияния и изменения поверхности твёрдой фазы. От 20 до 93% свинца, поглощённого свежеосаждёнными оксидами марганца, не удавалось экстрагировать 25% уксусной кислотой, а после «состаривания» в течение 28 недель для доля этой неэкстрагируемой фракции возросла до 37 - 100% поглощения свинца (II). Для свежеосаждённого и «состаренного» гетита доля экстрагируемого такой кислотой свинца составляла, соответственно, 10 - 44 и 19 - 62%. Можно сделать вывод о том, что при взаимодействии свинца даже с простыми сорбентами часть его оказывается более прочно связанной, а часть менее, то есть, проявляется неоднородность «сорбционных центров».
Чтобы заряд поверхности частиц оставался
неизменным, поглощение свинца почвами и их составляющими должно сопровождаться
вытеснением в раствор каких то других ионов. Связывание 1 моль свинца (II)
гидроксидами Mn при рН 4, по данным, приводит к вытеснению H+ в количестве 1
моль для бирнессита и 1,3 моль для криптомелона. Для гидроксидов железа
(гематита и петита) это отношение составило соответственно 1,3 и 2 моль.
Авторами работы, выдвинуто предположение о том, что поглощение свинца из кислых
растворов происходит в соответствии с уравнением:
SOH0 + Pb2+ = [SO - Pb2+] + H+ (1)
где SOH0 - незаряженный участок поверхности, а формула в квадратных скобках отражает поглощенную форму катиона свинца.
С ростом рН можно ожидать поглощение моногидроксокомплекса:
+ Pb2+ + Н2О = [SO- - Pb(OH)2] + 2Н+ (2)
С дальнейшим поверхностно - индуцированным межфазным осаждением гидроксида металла в соответствии с выражением:
+ Pb2+ + 2 Н2О = [S - Pb(OH)2] + 2Н+ (3)
Для оксидов железа резкое увеличение поглощения в узком диапазоне рН автор приписывает достижению уровня рН, при котором становится возможным поглощение PbOH+. Соединения в составе которых есть свинец на поверхности оксидов, гидроксидов, относят к поверхностным внутрисферным комплексам. Почвы с большим содержанием гумуса не проявляли большей селективности по отношению к Pb2+. Наиболее селективными сорбентами оказались оксиды железа.
«Сверх - эквивалентное» поглощение обнаружено, согласно при связывании почвами других катионов, например катионов меди. В соответствии с данными исследований, поглощение катионов почвами принято подразделять на «неспецифическое» и «специфическое». Под «неспецифическим» обычно понимают связывание катионов за счёт действия электростатических сил в двойном электрическом слое, а «специфическое» относят за счёт формирования координационных связей с поверхностью через атомы кислорода или группы - ОН. «Сверх - эквивалентное» поглощение происходит именно за счёт механизма, неселективного поглощения по отношению к ионам Pb2+.
Об особенностях механизма связывания свинца почвами, подтверждающих гипотезу, можно судить по тому, что его величина не пропорциональна ёмкости катионного обмена [3].
Предложены и другие гипотезы механизма поглощения свинца в почвах. В частности, другим типом взаимодействия может быть образование комплексов свинца с органическим веществом, сорбированными на поверхности глинистых частиц. Высказывается мнение о том, что роль глинистой фракции в поглощении свинца незначительна по сравнению с ролью органического вещества.
Роль органического вещества неоднозначна и с другой точки зрения: выделенные из почв гуминовые кислоты прочно связывали часть свинца, но 65% удержанного ими свинца оказывались в обменной фракции. Выделяемая 1н. HNO3 фракция свинца, по мнению авторов, входит в состав комплексных соединений с гуминовыми кислотами. Катионы Pb2+ могут быть связаны с гуминовыми кислотами либо через карбоксильные, либо через гидроксильные группы. Недиссоциированные слабокислые ОН- группы сахаров и фенолов также, возможно, участвуют в образовании таких комплексов.
Итак, на основе приведённых данных подтверждённые и гипотетические механизмы поглощения свинца можно представить в виде схемы, показанной в таблице 2.
Таким образом, на современном этапе исследования
механизмов поглощения металла можно утверждать, что, во-первых, существуют
некоторые условные фракции свинца в почвах, которые нельзя отнести к тем или
иным химическим соединениям. Во-вторых, в зависимости от свойств почв металл
можно сделать практически полностью недоступным для растений и иммобильным.