Материал: Шандра О.А. Нормальна фізіологія. Вибрані лекції _ навч. посіб. _ О.А. Шандра, Н.В. Общіна _ О._ОГМУ, 2005. - 322 с
ках особливими білками, які здатні утворювати з гормонами специфічні комплекси, що трансформують гормональний сигнал у гормональну дію. Такі біоспецифічні білки називаються клітинними рецепторами відповідних гормонів, або гормональними дискримінаторами.
До головних властивостей рецепторних молекул, які відрізняють їх від багатьох неспецифічних гормонозв’язуючих білків, належить висока вибіркова спорідненість до даної групи гормонів (лігандна стереоспецифічність); обмежена ємність до гормонів, що зв’язуються; особливості тканинної локалізації.
Висока спорідненість рецептора до гормону, що зв’язується, виявляється у спроможності реагувати на зовсім малу кількість гормону. Висока вибірковість лігандної спорідненості білків-рецепторів, стереоспецифічність зв’язуючих місць полягає в тому, що рецепторні білки здатні переважно зв’язувати певну групу природних і синтетичних гормонів, а також антигормонів.
Обмежена зв’язуюча ємність — наступна важлива риса характеристики рецепторів. Вона зумовлена низькою концентрацією зв’язуючих місць і, отже, їх легконасиченістю відповідною групою гормонів.
Специфічність локалізації рецепторів у тканинах визначається концентрацією рецепторних білків, що зумовлює чутливість тканин до гормону.
Рецептори визначають не тільки дискримінований прийом гормонального сигналу, але й ініціацію специфічних гормональних ефектів.
Вважається, що це відбувається двома способами відповідно до двох механізмів впливу гомонів на клітини-мішені.
Мембрана клітини-мішені
Цитоплазма клітини-мішені
Р
Г
Г |
АЦ |
цАМФ |
Неактивна |
Вплив на |
|
мембрану |
|
||||
протеїнкіназа |
|
||||
|
|
|
|
||
|
|
|
(транспорт) |
|
|
|
|
|
|
|
|
|
|
|
Активна |
Синтез білка |
Кінцевий |
|
|
|
біоефект |
||
|
|
|
протеїнкіназа |
||
|
|
|
|
||
|
|
|
Активація |
|
|
|
|
|
|
|
|
|
|
|
|
ферментів |
|
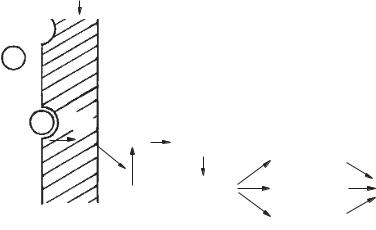
Рис. 19. Схема взаємодії гормону з рецептором клітини-мішені: P — рецептор; Г — гормон; АЦ — аденілатциклаза
84
Р
F
Г
Са2+
|
Мембрана клітини-мішені |
|
|
|||
|
|
|
||||
|
|
|
|
Цитоплазма клітини-мішені |
|
|
|
||||||
|
Са+ білок |
|
|
|
||
|
|
|
Кальмодулін |
Кальмодулін |
·Са2+ |
|
|
|
|
|
|||
|
Са2+ |
|||||
|
|
|
|
неактивний |
активний |
|
Активація Кіназа фосфорилази Фосфорилаза Біологічний ефект
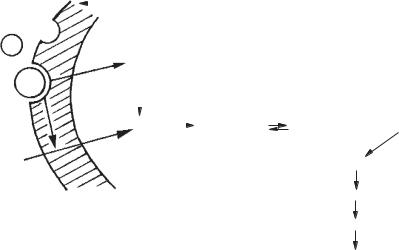
Рис. 20. Схема взаємодії гормону з рецептором клітинимішені, вторинний месенджер — іони Са, активний кальмодулін активує ферменти, що відбивається на фізіологічному ефекті: Р — рецептор; Г — гормон; Са + білок — внутрішньоклітинний кальцій, що пов’язаний з білками форми
Перший спосіб — рецепція стероїдних гормонів — складається з таких етапів:
1)стероїд, що не зв’язаний транспортними білками крові, здатний відносно легко проникати всередину клітини-мішені та швидко зв’язуватися в її цитоплазмі специфічними білками-рецепторами;
2)комплекс, що утворився, набуває властивостей, відсутніх у білкарецептора і в гормоні. Поява цих властивостей (наприклад, високої валентності) дозволяє комплексу входити в клітинне ядро і моделювати процеси транскрипції ДНК та РНК;
3)цикл рецепції завершується після зруйнування комплексу або використання його в процесі синтезу білка;
4)посередники (вторинні месенджери).
Другий спосіб — рецепція пептидних гормонів і катехоламінів з поверхні клітини завдяки утворенню внутрішньоклітинних посередників. Одним із головних і добре вивчених посередників є мембранний фермент
— гормонозалежна аденілатциклаза. Цей фермент сприяє утворенню з АТФ найважливішого посередника реалізації гормональних ефектів цик- лічно-3,5-аденозинмонофосфату (цАМФ). Утворений цАМФ активізує цАМФ-залежні протеїнкінази, що являють собою ферменти, які здійснюють фосфорилування відповідних білків. Останні забезпечують біологіч-
85
ний ефект гормону. Встановлено, що гормонозалежна аденілатциклаза
— це спільний фермент, на який поширюється дія різних гормонів. До цієї групи належать АКТГ, ТТГ, ФСГ, ЛГ, МСГ, АДГ, глюкагон та інші гормони. Відповідь на дію цих гормонів спостерігається вже через короткий проміжок часу в прямо пропорційній кількості цАМФ. Опосередкувати включення і виключення клітинних процесів можуть також іони кальцію (див. рис. 20). До цієї групи гормонів належать окситоцин, гастрин, холецистокінін, які діють через α-аденорецептори.
Біологічна дія Са2+ забезпечується трьома основними механізмами:
—зниженням проникності клітинної мембрани для іонів;
—зниженням активності ферментів;
—взаємодією з внутрішньоклітинною мікротубулярною ворсинчастою системою, що втягнута в секреторні процеси клітини.
Внутрішньоклітинний вільний кальцій впливає на відповідні кінази фосфорилаз у тому випадку, якщо він зв’язаний з внутрішньоклітинним білком кальмодуліном. Кальмодулін — рецепторний білок з високою афінністю до кальцію, складається з 148 амінокислотних залишків
іприсутній у всіх клітинах, що мають ядро. Його молекулярна маса
17 000.
Утворення комплексу гормону з рецептором приводить до підвищення внутрішньоклітинного рівня вільного Са2+, що перетворює його на активну форму і впливає на кальційчутливі білки, або ферменти, які відповідають за певний біологічний ефект гормону. Механізм дії цієї групи подано на рис. 10. Для цих гормонів: СТГ, пролактину, соматостатину, інсуліну — «вторинний месенджер» досі ще невідомий. Гормони цієї групи чинять як ранній, так і пізній вплив на клітини-мішені. Швидкий вплив, який виявляється через кілька хвилин або секунд, головним чином, спрямований на забезпечення транспорту різних речовин через мембрану клітини. Пізня дія гормону полягає у посиленні синтезу білка, активації ферментів і виявляється лише через кілька хвилин або навіть годин.
Таким чином, специфічна дія гормону виявляється тільки після утворення комплексу з відповідним рецептором. Рецептор розпізнавання та зв’язування гормону генерує хімічні чи фізичні сигнали, які викликають низку пострецепторних взаємодій, що завершуються специфічним і фізіологічним проявом ефекту гормону.
Отже, біологічна дія гормону залежить не тільки від наявності його в крові, але й від кількості та функціонального стану рецепторів, а також від рівня функціонування пострецепторного механізму.
Кількість рецепторів, як і інших компонентів клітини, постійно змінюється, відбиваючи процеси синтезу та руйнування. Основна роль у регуляції синтезу кількості рецепторів належить гормонам. Є зворотні взаємовідношення між рівнем гормонів у міжклітинній рідині та кількістю рецепторів. Наприклад, при гіперінсулінемії та ожирінні
86
кількість інсулінових рецепторів, локалізованих на гепатоцитах, адиноцитах, тимоцитах, моноцитах, зменшується на 50–60 %, і навпаки, інсулінодефіцитні стани супроводжуються збільшенням кількості рецепторів до інсуліну. Таким чином, зміна чутливості органів і тканин до гормонів змінюється завдяки механізмам зворотного зв’язку.
Зниження чутливості до гормону може бути зумовлене такими механізмами:
—зменшенням афінності рецептора внаслідок впливу інших гормонів і гормонорецепторних комплексів;
—зниженням кількості функціонуючих рецепторів внаслідок вивільнення їх із мембрани у позаклітинний простір;
—інактивацією рецептора внаслідок конформаційних змін;
—руйнуванням рецепторів шляхом підвищення активності протеаз або деградацією гормонорецепторного комплексу під впливом ферментів лізом;
—пригніченням синтезу нових рецепторів.
Для кожного виду гормонів є агоністи й антагоністи. Останні являють собою речовини, які здатні конкретно зв’язувати рецептор з гормоном, знижуючи його біологічний ефект. Агоністи, навпаки, утворюючи комплекс із відповідним рецептором, посилюють дію гормону. Наприклад, для кортизолу прогестерон є антагоністом, кортикостерон — агоністом, а альдостерон — слабким агоністом.
Регуляція секреції гормонів
Гормональна регуляція тканин і клітин є важливим компонентом ефекторної регуляції функцій організму. Гормони регулюють ріст, розвиток і диференціювання тканини й органів, а також адаптацію до зміни умов життєдіяльності: рівня фізичної активності, характеру харчування, інтенсивності нервово-психічної діяльності, вагітності, вигодовування тощо.
Гормони як важливий спосіб взаємодії органів і тканин, стабілізації та забезпечення їх узгоджених дій посідають підпорядковане, порівняно з нервовою регуляцією, положення.
Принцип нервізму — пануючої ролі нервової системи, особливо її найвищих відділів, — є досить універсальним. Гуморальна регуляція підпорядковується нервовим впливам. Особливістю гуморального компонента адаптації, аж до стресової реакції, є несвідоме її включення (В. М. Дільман).
Життєдіяльність організму супроводжується перебудовою активності ЗВС під впливом ЦНС — прямо й опосередковано, а також екстрагіпофізарно. Перший шлях припускає вплив ЦНС на гіпоталамус — найвищий вегетативний центр регуляції внутрішнього середовища організму. Нейрони гіпоталамуса мають виражену секреторну здатність
87
у досягненні інтегративно-провідникової функції. Крім типових нейромедіаторів, нейрони гіпоталамуса виділяють особливі речовини поліпептидної природи. Кожна з них стимулює секрецію певного гормону передньої частки гіпофіза. Ці речовини названі рилізинг-факторами, або ліберинами. Описані тиреоліберин, меланоліберин, кортиколіберин, гонадоліберин, соматоліберин. Для деяких гормонів (пролактин, соматотропін, меланотропін) виділені такі гальмуючі, або інгібуючі, фактори, які названо статинами. Під впливом ліберинів і статинів відбувається синтез і секреція тропних гормонів гіпофіза, які в свою чергу визначають рівень секреції гормонів ЗВС. Гормони вибірково впливають на чутливі до них клітини (клітини-мішені) та змінюють клітинні процеси, а отже, і гомеостаз організму. Однак у природних умовах відокремити регулюючий вплив від саморегулюючого важко, тому виділення фазності реакцій на той чи інший вплив також умовне.
Наприклад, В. М. Дільман вважає, що при крововтраті, болю, голодуванні та інших фізіологічних і патологічних станах розвивається двофазна адаптація. Перша фаза переважно нервова, реалізується через зміну активності вегетативної нервової системи, мозкового шару надниркових залоз, адреналіну тощо. Внаслідок цього розвивається стан готовності до боротьби — перерозподіляється кровотік, посилюється діяльність серця, розігріваються м’язи, а також її енергетичне забезпечення: викид з жирових депо ліпідів, а з печінки — глюкози у кров.
Друга фаза, переважно гормональна, — виділення жиромобілізуючих гормонів гіпофіза (кортикотропін, СТГ, ліпопротеїнів і пролактину), а також кортизолу з надниркових залоз, за рахунок чого відбувається більш ощадливий (раціональний) розподіл енергетичних запасів. Кортизон у комбінації із СТГ пригнічує споживання глюкози скелетними м’язами, залишаючи її для нервових клітин. Оскільки запаси глікогену дуже обмежені, під впливом кортизолу починається розщеплення білка та утворення з нього глюкози. Головним джерелом білка є лімфоцити з лімфовузлів, вилочкової залози та кісткового мозку. Як наслідок використання білка відзначається «пригнічення» непотрібних на цей момент функцій — імунітету, сексуальності, апетиту тощо.
Таким чином, цей шлях припускає, з одного боку, посилення активності по ланцюжку: ЦНС — гіпоталамус — гіпофізотропні гормони (залежно від ЗВС), а з іншого — еферентні впливи медіаторів вегетативних нервових закінчень на інші ЗВС (підшлункову, медулярну речовину надниркових залоз, залоз кишечнику та ін.). Так розвивається граничний стан між нормою і синдромом психоемоційного напруження (Л. Є. Панін, В. П. Соколов, 1981), якийсупроводжується появоютривожності та зниженням емоційної стабільності, переважанням тонусу симпатичної нервової системи над парасимпатичною і підвищенням активності гіпоталамо-гіпофізарно-наднирковозалозного ланцюжка та сим-
88