Материал: Розрахунок ректифікаційної колони періодичної дії для розділення суміші бензол–толуол
![]()
![]()
Виконання цієї умови означає, що помилки в розрахунках не допущені.
Середні концентрації рідини та пару в мольних частках
Оскільки колони періодичної
дії працюють як колони для зміщення парів, то вони складаються з однієї
частини.
![]()
![]()
Густина пари
![]()
![]()
де Мср - середня мольна маса пари, кт/кмоль; Т0= 273, 15 - абсолютний нуль, К; Тср=Т0+tcр - середня температура пари. К;
тут tcр - середня температура пари у колоні, визначена у залежності від Уср (див. рис.2), К;
Ро - атмосферний тиск, Па;
р - тиск у колоні, Па.
Густина
рідини
![]()
![]() - середня
концентрація рідини; У вольних частках;
- середня
концентрація рідини; У вольних частках;
![]() та
та ![]() - густина
низькокиплячого та висококиплячого компонентів при tср.
- густина
низькокиплячого та висококиплячого компонентів при tср.
Кількість
пари, що підіймається по колоні
![]()
де Mp. = Mнк Хр + Мвк(1 - Xр.) - мольна маса дистиляту, кг/кмоль;
Кількість рідини, що стікає по колоні;
![]()
де Mср(р) = Mнк Хср + Мвк(1
- Xср) - середня
мольна маса стікаючої по колоні рідини, кг/кмоль.
2.2
Тепловий розрахунок установки
Тепловий розрахунок складається з метою визначення необхідної кількості теплоти в кубі - кип'ятильнику, витрат теплоти, яка передається охолоджуючий воді в дефлегматорі та у водяних холодильниках дистиляту і кубового залишку, а також для визначення витрати гріючого пару в кубі та води у згаданих апаратах.
Тепловий баланс колони
Схема теплових потоків, на
якій кип'ятильник розглядається як складова частина
колони
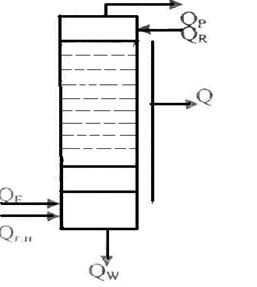
QГ.П + QF
+ QR = QP
+ QW + QF
+ QПОТ,
де QГ.П - кількість тепла, яке надходить з гріючою парою, що витрачається на випаровування рідини, Вт;
QF - тепло, яке надходить з вихідною сумішшю, Вт;
QR - тепло, яке надходить з флегмою, Вт;
QP - тепло яке виходить з пароподібним дистилятом, Вт;
QW - тепло, яке виходить з кубовим залишком, Вт;
QПОТ - втрати тепла в навколишнє середовище, Вт.
Витрата теплоти,
охолоджуючій воді, що віддається, в дефлегматорі-конденсаторі, знаходимо по
рівнянню:
![]()
тут
![]()
де rа і rб - питомі теплоти конденсації бензолу і толуолу при температурі 820 С..
Витрата теплоти, одержуваної в
кубі-випарнику від гріючої пари, знаходимо по рівнянню:
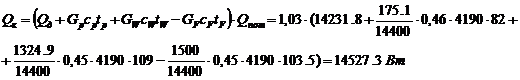
тут питомі теплоємності узяті відповідно при tp = 820 С tw= 109 0 С і tf = 103,50 С , температура кипіння початкової суміші tf = 103,5 0 С визначена по рис. № 2.
Витрата теплоти в
паровому підігрівачі початкової суміші:
![]()
сF = (0,45.0,43 + 0,55.0,42) 4190 Дж/(кг.К) узята при середній температурі (92,5 + 18)/2 ≈ 55 0 С.
Витрата теплоти, охолоджуючій воді у
водяному холодильнику, що віддається, дистиляті:
![]()
тут питома теплоємність дистиляту Сp = 0,43*4190 Дж/(кг.До) узята при середній температурі (82 + 25) /2 = 54 0 С.
Витрата теплоти, охолоджуючій воді,
що віддається, у водяному холодильнику кубового залишку:
![]()
де питома теплоємність кубового залишку Cw = 0,424*4190 Дж/(кгK) узята при середній температурі (109 + 25) /2 = 67 0 С.
Витрата гріючої пари:
у кубі-випарнику
![]()
де ![]() - питома
теплота конденсації гріючої пари; Всього: 0,007 кг/с = 100,8 кг/опер.
- питома
теплота конденсації гріючої пари; Всього: 0,007 кг/с = 100,8 кг/опер.
Витрата охолоджуючої води:
а) у дефлегматорі
![]()
б) у водяному холодильнику
дистиляту
![]()
в) у водяному холодильнику
кубового залишку
![]()
Всього: 0,00017+0,000015+0,00016=0,000345м3/с або 4,97 м3/опер;
Визначення швидкості пари і діаметру колони:
Рівняння робочoї
лінії:
![]()
![]()
Середні концентрації рідини:
![]()
Середні концентрації пари знаходимо
по рівняннях робітників лінії
![]()
Середні температури пари визначаємо по діаграмі t-x,y (рис.2)
- при ![]()
Середні молярні маси і густина пари:
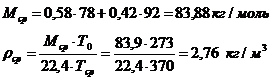
Густина рідких бензолу і толуолу близька. Температура у верху колони при Xp = 0,991 дорівнює 820 С, а в кубі-випарнику при Xw=0,006 вона дорівнює 109 . (рис.2).
Густина рідкого бензолу при t=820 С ρб = 813 кг/м3, а рідкого толуолу при t=1090 С ρт = 783 кг/м3.
Приймаємо середню густину рідини в
колоні:
![]()
Швидкість пари в колоні
(С=0,032)
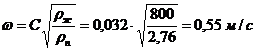
(95+8Об'ємна витрата проходячої
через колону пари при середній температурі в колоні tср= 970
С
![]()
або 0,13 м3/с
де Мр - молярна маса дистиляту, рівна
Мр = 0,991 . 78 + 0,009 . 92 = 78,12 кг/міль
Діаметр колони:
![]()
По каталогу довіднику
«Колонні апарати» беремо D=600 мм, тоді швидкість пари в колоні буде:
![]()
2.3 Гідравлічний розрахунок тарілок
ректифікаційний установка періодичний тиск
Приймаємо наступні розміри ситчатої тарілки: діаметр отвір d0 = 4 мм, висота силової перегородки hв = 40 мм. Вільний перетин тарілки (сумарна площа отворів) 8% від загальної площі тарілки. Площа, займана двома сегментними переливними стаканами, складає 20% від загальної площі тарілки.
Розрахуємо гідравлічний опір тарілки
у верхній і нижній частині колони по рівнянню:
Δ
p
= Δ
pсух+
Δ
pσ+
Δ
pпж
Гідравлічний опір сухої тарілки:
![]()
Де ξ=1,82- коефіцієнт опору незрошуваних ситчатих тарілок з вільним перетином 7- 10%; ω0= 0,6/0,08= 7,5 м/с - швидкість пари в отворах тарілки.
Опір, обумовлений силами
поверхневого натягy:
![]()
де ![]() -
поверхневий натяг рідини при середній температурі у колоні 970 С (у
бензолу і толуолу практично однакове поверхневий натяг); d0 = 0,004м - діаметр
отворів тарілки. Опір парорідинного шару на тарілці:
-
поверхневий натяг рідини при середній температурі у колоні 970 С (у
бензолу і толуолу практично однакове поверхневий натяг); d0 = 0,004м - діаметр
отворів тарілки. Опір парорідинного шару на тарілці:
![]()
Висота парорідинного шару
hпж=
hп+Δh
Величину ∆h - висоту шару над
зливною перегородкою розраховуємо по формулі:
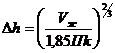
де Vж - об'ємна витрата рідини, м3/с; П - периметр зливної перегородки, м; k = ρпж/ρж - відношення густини парорідинного шару (піни) до густини рідини, приймаємо приблизно рівним 0,5.
Об'ємна витрата рідини у колоні:
![]()
де Мср = 0,7*78 + 0,3*92 = 82,2 - середня молярна маса рідини, кг/кмоль. Периметр зливної перегородки П знаходимо, вирішуючи систему рівнянь:
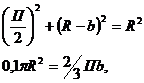
де R = 0,3 м - радіус
тарілки, ![]() - наближене
значення площі сегменту.
- наближене
значення площі сегменту.
Рішення дає: П = 1,24 м; b = 0,25 м. Знаходимо ∆h:
Висота парорідинного шару на тарілці:
hпж=
hп+Δh=0,04
+ 0,0052 = 0,0452 м
Опір парорідинного шару:
![]()
загальний гідравлічний опір тарілки колоні:
Δ
p
= Δ
pсух+
Δ
pσ+
Δ
pпж
= 141,3 + 26,2 + 230,5 = 398 Па
Перевіримо чи виконується при
відстані між тарілками h
= 0,3 м умова необхідна для нормальної роботі тарілок:
![]()
![]()
Отже, вищезгадана умова дотримується
Перевіримо рівномірність
роботи тарілок - розрахуємо мінімальну швидкість пари в отворах ωо.мин,
достатньо для того, щоб ситчата тарілка працювала всіма отворами:
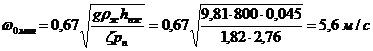
Розрахована швидкість ωо.мин, = 5,6 м/с; отже, тарілки працюватимуть всіма отворами.. Визначення числа тарілок і висоти колони.
а.) Наносимо на діаграму у - х
робочі лінії (рис. 5) і знаходимо число ступенів зміни концентрації
nт.
У колоні nт
-11, ступенів.
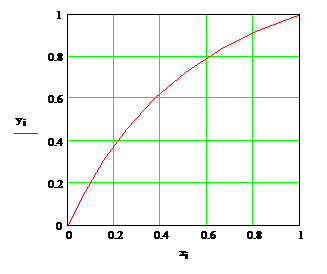
Рис. 5 - Визначення числа
ступенів зміни концентрації
Число тарілок розраховуємо по рівнянню:
п = пт / η
для визначення середнього к. п. д. тарілок η знаходимо коефіцієнт відносної летючості компонентів, що розділяються α = Ра / Рб і динамічний коефіцієнт в'язкості початкової суміші μ при середній температурі в колоні, рівній 97 0 С.
При цій температурі тиск насиченої пари бензолу Рб = 1239 мм рт. ст., толуолу Рт = 509 мм рт. ст. (табл. 1), α = 1239/509 = 2,43.
Динамічний коефіцієнт в'язкості
бензолу при 97 0 С рівний 0,29 сП, толуолу 0,29 сП. Приймаємо динамічний
коефіцієнт в'язкості початкової суміші μ
= 0,29 сП = 0,29.10-3 Па.с.Тоді по графіку (рис.
6) знаходимо . η
= 0,4 Довжина шляху рідини на тарілці
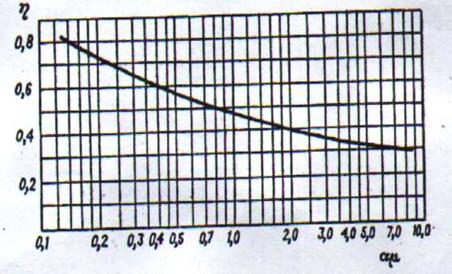
Рис. 6 - Діаграма для наближеного визначення середнього до. п. д. тарілок
l
= D
- 2b
= 0,6 - 2.0,24 = 0,12 м
По графіку (рис. 7) знаходимо значення поправки на довжину шляху ∆ = 0,1 середній к. п. д. тарілок по рівнянню:
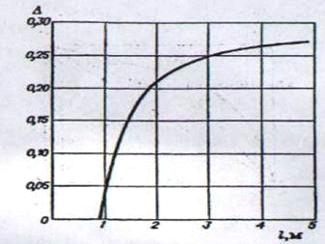
Рис. 7 - Залежність поправки ∆ від довжини шляху рідини на тарілці l
ηl
= η (1
+ Δ)
= 0,4 (1 + 0,1) = 0,47
Для порівняння розрахуємо середній
к. п. д. тарілки η0
по критерійній формулі, одержаній шляхом статистичної обробки численних опитних
даних для колпачкових і ситчатих тарілок:
![]()
У цій формулі безрозмірні
комплекси:
![]()
![]()
де ω - швидкість пари в колоні, м/с; Sсв - відносна площа вільного перетину тарілки; hп - висота зливної перегородки, м; ρп и ρж - густина пари і рідини, кг/м3; Dж - коефіцієнт дифузії легколетучего компоненту в початковій суміші, визначуваний по формулі, м2/с; σ - поверхневий натяг рідини живлення, Н/м.
Физико-хімічні константи
віднесені до середньої температури в колоні. Заздалегідь розрахуємо коефіцієнт
дифузії
Dж :
![]()
У нашому випадку: β = 3; μж = 0,29 сП = 0,29.10-3 Па.с; М = МF = 83,9 кг/кмоль; υ = 14,8.3 + 3,7.6 -15 = 96; Т = 97 + 273 = 370 К.
Коефіцієнт дифузії:
![]()
Безрозмірні комплекси:
![]()
![]()
Середній к. п. д. тарілки:
![]()
що близьке до знайденого значення ηl.
Число тарілок:
п = пт / ηl
= 11/0,47
= 23
Загальне число тарілок nт = 23, із запасом п = 25.
Висота тарільчатої частини колони:
Нт = (п - 1) h
= (25 - 1) 0,3 = 7,2
м.
Загальний гідравлічний опір тарілок:
Δр
= Δр п =
398*23=9154 Па ≈ 0,09 кгс/см2.
ВИСНОВОК
Загальна кількість
енергетичних витрат при виконанні процесу ректифікації на колоні періодичної
дії з ситчатимі тарілками для розділення при атмосферному тиску 1500 кг/опер
рідкої суміші речовин бензолу і толуолу, що містить 12 мас. % бензолу і 88 мас.
% толуолу, необхідний зміст бензолу в дистиляті 99 мас. %, необхідний зміст
толуолу в кубовому залишку 0,5 мас. % (початкова суміш перед подачею в колону
підігрівається до температури кипіння, при охолоджені водою tп
=
200
С складає 4,97 м3/опер.
СПИСОК Л1ТЕРАТУРИ
1. Касаткин А.Г. Основные процессы .и аппараты химической технологам. - М-: Химия, 1973. - 750 с.
2 Павлов К. Ф., Романков П.Г., Носков А.А. Примеры и задачи по курсу процессов и аппаратов химической технологии. - Л.: Химия, 1987. - 576 с.
3 Александров И. А. Ректификационные и абсорбционные аппараты. - Изд. 3-е. Пер. - М.: Химия, 1978. - 280 с.
4. Стабников В.Н. Расчет и конструирование контактных устройств ректификационных и абсорбционных аппаратов. - Киев: Техника, 1970. -
207 с.
5. Рамм В.М. Абсорбция газов. - М.: Химия, 1966. - 356 с.
6. Хоблер Г. Массопередача и абсорбция. - М.: Химия, 1964. - 356 с.
7. Тютюнников А.Б., Товажнянский Л.Л., Готлинская А.П. Основы расчета и конструирования массообменных колон. - Киев: Вища шк., 1989. - 223 с.
9. Лащинский А.А., Толчинский А.Р. Основы конструирования и расчета химической аппаратуры. Справочник. - Л.: Машиностроение, 1970. - 752 с.
10. Лащинский А.А. Конструирование сварных химических аппаратов, справочник.-Л.: Машиностроение, 1981.-382 с.
.Борисов Г.С., Брыков В.П., Дытнерский Ю.И. и др. Основные процеси и аппараты химической технологии. Пособие по проектированию. -Изд. 2-е. Пер. и доп. Под ред. Ю.И. Дытнерского. - М, Химия, 1991 - 496 с.