Материал: Реакторы процесса получения элементарной серы
Реакторы процесса получения элементарной серы
МИНИСТЕРСТВО ОБРАЗОВАНИЯ И НАУКИ РОССИЙСКОЙ ФЕДЕРАЦИИ
ФЕДЕРАЛЬНОЕ ГОСУДАРСТВЕННОЕ БЮДЖЕТНОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ ВЫСШЕГО ПРОФЕССИОНАЛЬНОГО ОБРАЗОВАНИЯ
УФИМСКИЙ ГОСУДАРСТВЕННЫЙ НЕФТЯНОЙ ТЕХНИЧЕСКИЙ УНИВЕРСИТЕТ
КАФЕДРА
ТЕХНОЛОГИИ НЕФТИ И ГАЗА
Курсовая работа
по дисциплине "Химические реакторы"
на тему:
"Реакторы процесса получения элементарной серы"
Выполнил:
Аубакиров С.Б.
УФА
Содержание
Введение
1. Общие положения и назначение процесса
2. Характеристика сырья процесса
. Физико-химические свойства серы
4. Механизм и химизм реакций процесса получения серы методом Клауса
5. Термодинамические основы процесса Клауса
. Катализаторы процесса Клауса
. Влияние основных технологических параметров на процесс Клауса
.1 Влияние температуры
.2 Давление
.3 Время контакта
. Термическая ступень
. Каталитическая ступень
. Модификация установок Клауса
Заключение
Список
использованных источников
Введение
Как и во всех промышленных процессах, при
внедрении и эксплуатации установок получения серы возникают определенные
проблемы. Во-первых, несмотря на накопленный опыт в проектировании установок
Клауса, достаточно трудно поддерживать процесс на полном уровне конверсии в
промышленных условиях. Поскольку эксплуатировать установки, в ходе работы
которых наблюдаются пределы выбросов вредных веществ в атмосферу выше
допустимого значения, нельзя. Во-вторых, на большинстве существующих установок
отсутствуют установки доочистки отходящих газов и технологический режим не
соблюдается должным образом. В-третьих, высокая конкуренция на мировом рынке
серы, сложившаяся в наши дни, вынуждает решать еще одну важную задачу -
повышение качества получаемого товарного продукта. В-четвертых, объемы
перепроизводства серы сегодня показывают, что необходимо искать альтернативные
варианты ее применения.
1. Общие положения и назначение
процесса
Для утилизации сероводорода, получаемого в
процессе аминовой очистки углеводородных газов, а также с гидрогенизационных
процессов переработки сернистых и высокосернистых нефтей и газоконденсатов
обычно применяют хорошо известный в мировой практике процесс Клауса или его
различные модификации. Данный процесс назван по имени английского химика Карла
Фридриха Клауса, запатентовавшего в 1883 г. способ получения серы из
сероводорода, образуемого при переработке аммиачной воды в сульфат аммония, в
присутствии кислорода воздуха на катализаторах:
H2S + 0,5O2 =
H2O + 1/x · Sx, (1) где
x = 2 - 8.
Используемый на сегодняшний день в промышленных масштабах процесс Клауса - это эффективный процесс, включающий термическую и каталитическую стадию, отделение доочистки хвостовых газов, отделение дегазации жидкой серы, узел дожига отходящих газов.
Особенностью рассматриваемого процесса является
то, что путем термического окисления сероводорода до диоксида серы:
2H2S + 3O2
2SO2 + 2H2O + (0,53-0,57) МДж/моль, (2)
и каталитической окислительной конверсии
сероводорода и диоксида серы:
H2S+ SO2 3S + 2H2O + (0,087- 0,154)
МДж/моль, (3) получают высококачественную серу со степенью извлечения 99,5% без дополнительной очистки отходящих газов. Что касается отходящих газов, имеющих в своем составе 1-2% об. сероводорода, до 1% об. диоксида серы, небольшие количества серооксида углерода, сероуглерода, капельной и паровой серы, а также водорода, оксид углерода, углекислоту, водяные пары и азота, то их подвергают технологии дополнительной очистки по специально разработанному процессу, именуемому «Сульфрен». Но сера, получаемая на установках Клауса, содержит растворенный сероводород в виде свободного сероводорода и химически связанного полисульфида водорода, что приводит к его выделению во время хранения и транспортировки жидкой серы. Эти проблемы могут быть предотвращены в процессе дегазации серы.
Основными производителями серы в России, внедрившими в свою структуру установку Клауса, являются газоперерабатывающие предприятия ПАО «Газпром» (Астраханский и Оренбургский ГПЗ), на долю которых приходится около 90%. Остальное количество серы производится на НПЗ и металлургических предприятиях. Но практически на всех металлургических и нефтеперерабатывающих заводах России эксплуатируются установки данного процесса, введенные в производство в 60-80 годах, т.е. более чем 30 - 50 лет назад, а это значит, что ресурс оборудования практически исчерпан. Поэтому совершенствование процесса Клауса является актуальным направлением в газо- и нефтеперерабатывающей промышленности.
Достоинствами процесса Клауса являются решение проблемы утилизации сероводорода и получение в результате ценного товарного продукта - серы - одного из видов сырья для химической промышленности, значительно превосходящего по качеству самородную серу.
Как и во всех промышленных процессах, при
внедрении и эксплуатации установок получения серы возникают определенные
проблемы. Во - первых, несмотря на накопленный опыт в проектировании установок
Клауса, достаточно трудно поддерживать процесс на полном уровне конверсии в
промышленных условиях. Поскольку эксплуатировать установки, в ходе работы
которых наблюдаются пределы выбросов вредных веществ в атмосферу выше
допустимого значения, нельзя. Во - вторых, на большинстве существующих
установок отсутствуют установки доочистки отходящих газов и технологический
режим не соблюдается должным образом. В-третьих, высокая конкуренция на мировом
рынке серы, сложившаяся в наши дни, вынуждает решать еще одну важную задачу -
повышение качества получаемого товарного продукта. В-четвертых, объемы
перепроизводства серы сегодня показывают, что необходимо искать альтернативные
варианты ее применения.
2. Характеристика сырья процесса
Основным сырьем процесса производства серы методом Клауса является сероводородсодержащий (кислый) газ, получаемый при МЭА очистке природного газа, сероводородсодержащий газ с установок гидроочистки бензиновых и дизельных фракций и других промышленных производств.
Сырье, поступающее на установку, характеризуется концентрацией сероводорода в кислом газе, содержанием углеводородов и аммиака. Содержание сероводорода в кислых газах, получаемых при очистке природного газа, колеблется в довольно широких пределах - от 5 до 90%. Кислые газы, поступающие с НПЗ, в свою очередь, характеризуются высоким содержанием сероводорода - 70-95%. Стоит отметить, что получаемый на НПЗ кислый газ отличается от аналога, выделяемого при очистке природного газа содержанием более тяжелых газообразных углеводородов. Поэтому во избежание закоксовывания катализатора в конверторах на каталитической ступени установки необходимо как можно полнее удалить тяжелые углеводороды перед подачей в реакционную печь и обеспечить их полное сгорание на термической ступени.
Другой особенностью нефтезаводских сероводородсодержащих газов является наличие аммиака. В процессах гидроочистки и гидрокрекинга одновременно с превращением сернистых соединений нефтяных фракций в сероводород азотистые соединения крекируются и гидрируются в аммиак. Присутствие аммиака можно объяснить тем, что при атмосферной перегонке его впрыскивают в верхнюю часть ректификационной колонны с целью подавления сероводородной и хлористоводородной коррозии. В случаях, когда аммиак целиком или частично проходит через печь не сгорая, возникают побочные реакции, одной из которых является образование серной кислоты, которая помимо образования коррозионных проблем, усиливает сульфатирование катализатора. В целях лимитирования побочных реакций необходимо удалять аммиак из сырьевого потока на стадии термического сжигания.
Таким образом, от состава кислого газа,
поступающего на установку получения серы, существенным образом зависят
технико-экономические показатели процесса, качество получаемых товарных продуктов,
конструкционные особенности проектируемой установки.
3. Физико-химические свойства серы
Сера (лат. Sulfur)
является широко распространенным элементом и составляет 0,05% от массы земной
коры. Данный элемент относится к главной подгруппе 6-ой группы периодической
системы элементов Д.И. Менделеева, в третьем периоде. Порядковый номер 16.
Относительная атомная масса равна 32,06. Элемент является типичным активным
неметаллом. Известны три аллотропные модификации серы: ромбическая, или α
-
сера; моноклинная, или β - сера; и
пластическая, или каучукоподобная. Наиболее устойчивой является ромбическая
модификация, именно в таком виде сера встречается в природе в свободном
состоянии. Ромбическая сера состоит из циклических молекул S8,
в которых атомы серы соединены одинарными ковалентными связями:
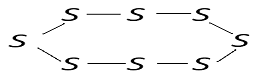
Рисунок 1 - Строение ромбической серы
Ромбическая сера - твердое кристаллическое вещество желтого цвета, не растворяется в воде, хорошо растворим в сероуглероде CS2, а также в некоторых других органических растворителях. Температура плавления ромбической серы + 112,8 °С, температура конденсации + 188 °С, при температуре + 444,6 °С сера кипит. Плотность 2,070 г/см3.
Одним из резко аномальных свойств серы является ее вязкость. С повышением температуры она резко увеличивается, а затем падает. Для чистой серы вязкость от минимального значения 0,065 пуаз при + 165 °С увеличивается до 933 пуаз при 187 °С и затем уменьшается до 0,93 пуаз при температуре кипения.
В природе она встречается в весьма разнообразных формах: самородная сера, сульфитные и сульфатные минералы, меркаптаны в природном и попутном газе, сложные сероорганические соединения в нефти, в растительных и животных организмах. Важнейшие из них следующие: FeS2 - пирит, или железный (серный) колчедан, CuS - медный блеск, Ag2S - серебряный блеск, PbS - свинцовый блеск. Что касается сульфатов, то они представлены следующими соединениями: гипс - CaSO4 · 2H2O, мирабилит, или глауберова соль - Na2SO4 · 10H2O, горькая (английская) соль - MgSO4 · 7H2O. Разведанные месторождения самородной серы содержат примерно 1,2 млрд т серы, месторождения углеводородов - свыше 5 млрд т.
Как было отмечено ранее, изучаемый элемент
образует многочисленные аллотропные модификации. Явление аллотропии - это
образование молекул с различным числом атомов и образование кристаллов
различных форм. Значит, наличие многочисленных модификаций серы можно объяснить
способностью ее атомов соединяться друг с другом с образованием кольцевых или
цепных молекул.
4. Механизм и химизм реакций процесса получения
серы методом Клауса
В современных ГПЗ и НПЗ процесс получения серы осуществляется на одной термической и двух - трех каталитических ступенях.
Термическая стадия представляет собой
высокотемпературное (температура реакции 900-1300 °С) сжигание кислого газа в
топочной камере печи реактора при подаче стехиометрического количества воздуха
по следующему уравнению:
Н2S
+ О2 → 2H2O
+ S2
+ Q, (4)
где Q - количество теплоты, выделившееся в результате реакции.
Однако не весь сероводород сгорает по этой
реакции. Часть его может не вступить в реакцию, а часть сгорает с образованием
диоксида серы SO2
по
следующей реакции:
H2S + 3O2 → 2SO2 + 2H2O + Q ; (5)
Объемное соотношение H2S и SO2 в продуктах горения 2:1.
Как видно по реакции (4), сера находится в виде S2. До серы сгорает примерно 64% сероводорода, до диоксида углерода примерно 12% сероводорода. На термической стадии по разным источникам образуется 90 - 92% всей серы.
Нежелательные компоненты (углекислый газ, водяные
пары, газообразные углеводороды, аммиак) [10], которые присутствуют в кислом
газе, также могут вступать в побочные реакции, приводящие к снижению конверсии
сероводорода в серу и образованию соединений, которые не участвуют в реакции
образования серы на последующих ступенях процесса. При температурах (900-1100
°С) термической ступени активно протекают побочные реакции с образованием
сероокиси углерода COS
и сероуглерода CS2
[11,
c. 94]:
СН4 + 2H2S → CS2 + 4H2 ; (6)
СН4 + S2 → 2H2 + CS2 ; (7)
СН4 + 2S2 → 2H2S + CS2 ; (8)2 + H2O → COS + H2S ; (9)
CS2 + SО2 → 2COS + 3/2S2 ; (10)
СН4 + 3/2O2 → CO + 2H2O ; (11)
СО + 1/2 S2 → COS ; (12)
СН4 + 3SО2 → 2CОS + 1/2 S2 + 4H2О ; (14)
СО2 + 3/2S2 → 2CОS + SО2 ; (15)
2NH3
+
1,5O2 →
N2
+ 3H2O.
(16)
Согласно приведенным реакциям кислород воздуха также расходуется на сжигание газообразных углеводородов, входящих в состав кислого газа. Углеводороды активнее реагируют с кислородом и он, в первую очередь идет на их сгорание, поэтому недостаток кислорода в термической стадии приводит:
к снижению выхода готовой продукции за счет снижения доли реакций (4) и (5) ;
к возможности образования сажи, которая затем осаждается на катализаторе в конверторах и снижает его активность.
Уменьшить содержание CS2 в технологическом газе можно повышением температуры в термической ступени более 1100 °С [12].
Таким образом, при выходе из термической ступени в технологическом газе кроме целевого продукта могут присутствовать и другие побочные продукты: H2S, CO2, COS, CS2, H2O, CO, H2, N2 и др.
На каталитических ступенях процесса
при температуре 200 - 300 °С происходит
взаимодействие сероводорода с диоксидом серы, которые не прореагировали на
термической ступени, с образованием элементарной серы на катализаторе по реакции:
2H2S + SО2
→ 3/n Sn + 2H2O,
(17)
где n = 2 - 8.
Реакция идет с поглощением тепла.
В то время как продукты побочных реакций
термической ступени на первой каталитической ступени подвергаются гидролизу в
присутствии паров воды:
СS2 + 2H2O
→ 2H2S + CO2 ; (18)+ H2O → CO2
+ H2S ; (19)
Также в каталитических ступенях могут
происходить следующие реакции:
2COS + SО2 → 3/n Sn + 2CO2 ; (20)
3S2 → S6 ; (21)
S2 →
S8 ;
(22)
Эти реакции идут с выделением тепла. Общий
тепловой каталитической стадии положительный. Необходимо отметить, что при
осуществлении этой стадии в две ступени технологический газ подвергают
промежуточному охлаждению до 150-160 °С в конденсаторах - коагуляторах, что
способствует увеличению выпуска серы, так как удаление серы из газовой фазы
сдвигает равновесие реакции в сторону образования серы и снижает точку росы
серы в технологическом газе. Подогрев технологических газов перед
каталитическими ступенями осуществляется путем сжигания части исходного кислого
газа. С последней каталитической ступени, после извлечения образовавшейся серы,
отходящий газ направляют на установку доочистки хвостовых газов процесса
Сульфрен.
5. Термодинамические основы процесса Клауса
В современных исследованиях с использованием
современных термодинамических данных и с учетом существования всех известных
разновидностей элементарной серы были получены и откорректированы кривые,
выражающие температурную зависимость равновесной конверсии стехиометрической
смеси чистого сероводорода и воздуха в элементарную серу при различном давлении
паров в системе, представленные на рисунке 2. На рисунке представлены две зоны,
разделенные пунктиром: высокотемпературная зона термического окисления с
интервалом температур 426-870 °С и низкотемпературная каталитическая с интервалом
температур 204-426 °С. в высокотемпературной зоне, обозначенной I,
согласно рисунку 1.2, с повышением давления степень превращения сероводорода в
серу снижается. В каталитической зоне, обозначенной II,
наблюдается обратная картина, т.к. давление способствует конденсации
элементарной серы и более полному выводу из зоны реакции.