Материал: Расчеты термодинамических функций металлургических процессов
Порядок и знак величины ΔG позволяет качественно предвидеть
положение равновесия реакции. Она является сводной функцией от энтальпии и
энтропии. Рассмотрим график зависимости ΔG от температуры (рис.3) . Видно, что
с увеличением температуры энергия Гиббса сначала понижается, а затем
возрастает. Она не имеет положительных значений в интервале температур от 298
до 1900°К, следовательно при рабочей температуре конвертера 1500°К реакция
окисления металлического железа кислородом оксида кобальта проходит
самопроизвольно в прямом направлении.
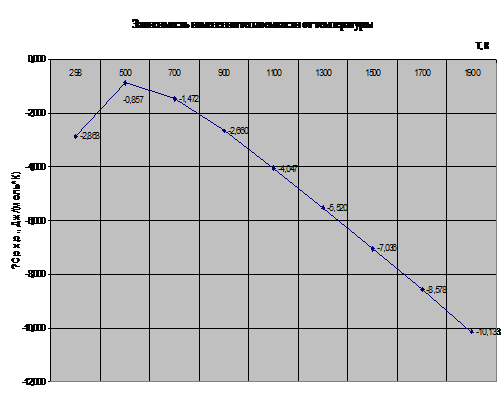
Рис. 4. Зависимость изменения теплоемкости от температуры
Рассмотрим график зависимости теплоемкости от
температуры (рис.4) . Видно, что с увеличением температуры СР сначала
увеличивается, затем уменьшается на интервале температур 500-1900 К, это
означает, что на этом интервале температур отношение изменения энтальпии
реакции к изменению температуры развивается регрессирующе - энтальпия
уменьшается тем быстрее, чем выше температура. Что подтверждается
соответствующим графиком и термодинамическими расчетами.
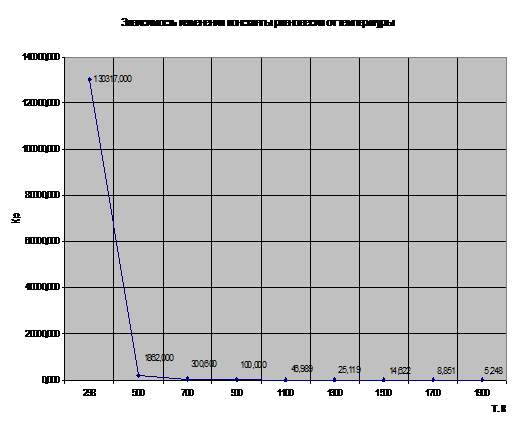
Рис. 5. Зависимость изменения константы равновесия от
температуры
Рассмотрим график зависимости константы равновесия от температуры (рис.5). С увеличением температуры Кр убывает. В интервале температур 298-1900К Кp>>1, следовательно равновесие реакции сместится в сторону образования продуктов реакции.
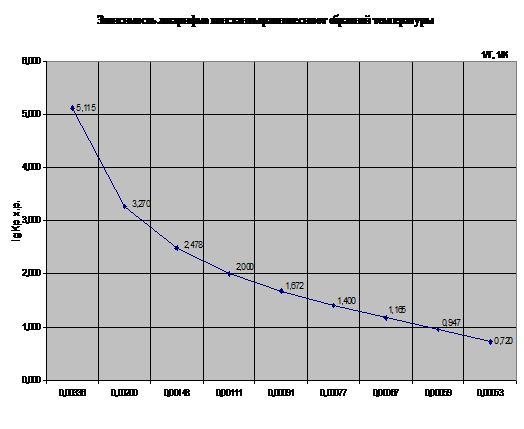
Рис. 6. Зависимость изменения логарифма константы
равновесия от обратной температуры
Рассматривая график LgKр от 1/Т (рис.6) видно, что с
увеличением обратной температуры LgKр уменьшается, что вытекает из
вышесказанного.
Вывод
Рассмотрим график зависимости Ср от температуры (рис.4). Из него видно, что с увеличением температуры Ср уменьшается, это означает, что отношение изменения энтальпии реакции к изменению температуры развивается регрессирующие - энтальпия уменьшается тем быстрее, чем выше температура.
Рассмотрим график зависимости ∆H от температуры (рис. 1). Из него видно, что с увеличением температуры энтальпия уменьшается. Энтальпия во всех расчетах отрицательная, следовательно реакция проходит с выделением тепла. ∆Sт энтропия (рис. 2) - это функция состояния термодинамической системы, а также количественная мера ее беспорядка. По графику видно что энтропия уменьшается, т.е. уменьшается беспорядочность системы. Это влияет, благоприятствует течению реакции в обратном направлении.
Из уравнения ∆Gх.р= ∆Hт-T∆Sт следует, что чем выше температура, тем меньше влияние энтропии на прямое течение процесса. Это объясняется тем, что с понижением температуры основное влияние оказывает изменение энергии, т.к. величина T∆Sт становится малой по сравнению с ∆Hт.
Порядок и знак изменения энергии Гиббса позволяет качественно предвидеть положение равновесия реакции. Рассмотрим график зависимости ∆G от температуры (рис.3). Из него видно, что с увеличением температуры изменение энергия Гиббса увеличивается. Несмотря на то что ∆Hт уменьшается, ∆G после 1700К становиться положительной, вследствие существенного влияния T∆Sт.
Рассмотрим график зависимости lgКр от температуры (рис. 5). На всем интервале температур lgКр убывает, что свидетельствует экзотермическому течению реакции. На всем интервале температур lgКр>0 следовательно равновесие сместится в сторону образования продуктов реакции.
Рассмотрим график lgКр
от 1/Т (рис. 6). На данном графике зависимости lg Kp обратной температуры кривая стремится к прямой линии, что
является следствием уравнения 2,3*lgКр=(-∆Hт/RT)+∆Sт/R
Часть 2. ПЛАВКА В ПЕЧИ ВАНЮКОВА (НМЗ)
. ФИЗИКО-ХИМИЧЕСКАЯ СУЩНОСТЬ ПРОЦЕССА
металлургический плавка печь термодинамический
Теоретические основы процесса Ванюкова разработаны группой научных сотрудников Московского института стали и сплавов под руководством доктора технических наук профессора А.В. Ванюкова, после смерти которого, его именем названа печь и технологический процесс. Рабочие проекты ПВ выполнены конструкторским отделом НФ «Института Норильскпроект» ООО «Института Гипроникель».
Процесс Ванюкова представляет собой плавку сульфидного сырья в интенсивно перемешиваемой шлако-штейновой ванне с использованием тепла окислительных реакций.
От других способов плавки процесс Ванюкова отличается подачей обогащенного кислоро-дом дутья и шихты в шлаковую ванну с небольшим содержанием штейна.
Процесс Ванюкова непрерывный, осуществляется в печах шахтного типа.
Обогащен-ное дутье подают в расплав через фурмы, расположенные симметрично с
обеих сторон печи. По осям фурм расплав в печи делится на две зоны: верхнюю
надфурменную (барботируемую) и нижнюю подфурменную, где расплав находится в
относительно спокойном состоянии.
1.1 Процессы плавления шихты
В процессе Ванюкова, как и в других автогенных процессах, элементарные стадии процесса плавления совмещены.
Нагрев шихты и диссоциация высших сульфидов начинается во время вертикального движения шихты к поверхности расплава и завершается в барботируемой области ванны.
При этом могут идти следующие реакции диссоциации высших сульфидов:
2CuFeS2 = Cu2S + 2FeS + 1/2 S2 (1)
CuFe2S3 = Cu2S + 4FeS + 1/2 S2 (2)
NiFeS2 = Ni3S2 + 3FeS + 1/2 S2 (3)S8
= 7FeS + 1/2 S2
(4)
Образующаяся сера частично окисляется кислородом дутья по реакции
/2 S2 + O2 = SO2 (5)
частично испаряется в виде элементной серы и частично окисляется над расплавом кислородом, подсасываемого воздуха.
В процессе Ванюкова отсутствует прямой контакт кислорода дутья с шихтой. Высокая скорость массообмена в барботируемой ванне приводит к образованию однородной шлако-штейновой эмульсии.
При этом кислород взаимодействует с сульфидом железа, растворенным как в штейновом, так и в шлаковом расплаве по реакции
+ 3/2O2 = FeO + SO2 (6)
Образующийся диоксид серы может выступать в качестве окислителя с выделением элементной серы по реакции
+ 1/2 SO2 = FeO + 3/4 S2 (7)
Оксид железа (FeO), полученный по реакциям (6) и (7), попадая в область
дутьевого факела, окисляется до магнетита (Fe3O4) по реакции
FeO + 1/2 O2 = Fe3O4 (8)
Магнетит, в интенсивно барботируемой ванне, контактирует с сульфидом
железа и снова восстанавливается до оксида железа по реакции
Fe3O4 + FeS + 5SiO2 = 5(FeO)2·SiO2 + SO2
(9)
Содержание магнетита в шлаке определяется равновесием между скоростями реакций (8) и (9).
Помимо сульфидов, в шихте процесса Ванюкова присутствуют диоксид кремния (SiO2), оксиды кальция (CaO) и магния (MgO), окись алюминия (Al2О3) и других, которые наряду с образующимися оксидами железа формируют шлак. Состав шлака зависит от содержания основных шлакообразующих компонентов: FeO, SiO2 и CaO. При плавке на силикатный шлак образуется расплав, близкий по составу к фаялиту (2FeO·SiO2). При плавке на шлаки, содержащие кальций, могут образовываться ферриты или силикаты кальция, например, 2CaO·Fe2O3 и 2CaO·SiO2
Процесс Ванюкова может идти как автогенно, т.е. за счет тепла экзотермических реакций окисления шихты, так и полуавтогенно, когда недостаток тепла компенсируется сжиганием природного газа по реакции
+ 2O2 = CO2 + 2H2O (10)
1.2 Процесс обеднения шлака
Шлак ПВ представляет собой сложный сплав оксидов, который формируется из оксидов пустой породы исходного сырья и специально вводимых флюсов. Важнейшими оксида-ми, составляющими основу шлаков, являются SiO2, FeО + Fe3O4, CaO, MgO и Al2O3. Содержание отдельных шлакообразующих оксидов в шлаках меняется в широких пределах, что приводит к значительному различию их физико-химических свойств. Необходимо стремиться к тому, чтобы выход шлака был минимальным, т. к. его увеличение приводит к повышению расхода флюсов, энергетических затрат, потерь металлов и др. Образующийся при плавке шлак, должен удовлетворять требованиям технологии.
К важным физико-химическим свойствам шлака относятся температура плавления, плотность и вязкость.
Температура плавления шлака - температура, при которой шлак становится жидко-текучим.
Плотность шлаков возрастает с увеличением содержания тяжелых компонентов магнетита (Fe3O4) и оксида железа (FeО) и снижается при добавках более легких диоксида кремния (SiO2) оксидов кальция (CaO) и магния (MgO). С повышением температуры плотность шлака прямо пропорционально понижается.
Вязкость шлаков оказывает влияние на кинетику металлургических реакций, разделение продуктов плавки (потери металлов со шлаками) и на массообмен в расплаве. С повышением температуры вязкость всех шлаков уменьшается.
В соответствии с законами распределения компонентов между продуктами плавки, шлаки всегда содержат некоторое количество извлекаемых металлов, то есть являются источником их потерь.
Потери цветных металлов со шлаками слагаются из механических и растворенных потерь.
Механические потери обусловлены недостаточным временем отстаивания мелких сульфидных капель. Растворенные потери, составляющие более 80 % от всех потерь, обусловлены окислением и растворением в шлаке цветных металлов.
Процесс Ванюкова обеспечивает хорошие условия для снижения обоих видов потерь.
Интенсивный массообмен повышает вероятность соударения штейновых включений
и вероятность их слияния в устойчивые, крупные, быстро оседающие капли с
размерами от 0,5 до 5,0 мм. Интенсивный массообмен также благоприятствует
взаимодействию оксидов цветных металлов с сульфидом железа по реакции
(MeO) + [FeS] = [MeS] + (FeO), (11)
где Me - медь, никель, кобальт.
Растворимость цветных металлов в шлаке тесно связана с массовой долей в
нем магнетита, с увеличением которой увеличиваются растворенные и суммарные
потери. Поэтому можно создать условия для разложения магнетита по реакции (9),
не допуская снижения температуры расплава, изменения отношения между загрузкой
сульфидной шихты и кислородом дутья, загрузки флюсующих компонентов.
1.3 Разделение продуктов плавки
По мере протекания процессов плавления непрерывно загружаемой шихты, в надфурменной зоне печи происходит направленное движение расплавов штейна и шлака сверху вниз за счет непрерывного раздельного выпуска продуктов плавки через соответствующие сифоны. Такое движение является одной из отличительных особенностей процесса Ванюкова.
Сформировавшиеся в надфурменной области капли штейна промывают подфурменный слой, и сливаясь с мелкой сульфидной взвесью, присутствующей в шлаке, дополнительно ее обедняют. Однако, на границе раздела штейн-шлак, из-за медленного слияния капель штейна со всем объемом фазы, образуется переходный слой толщиной от 200 до 300 мм с повышенной от 65 % до 75 % массовой долей штейна, в то время как в надфурменной области массовая доля штейна изменяется на величину до 10 %. Для предотвращения механи-ческого уноса капель штейна высота шлакового перетока должна быть примерно на 200 мм больше толщины переходного слоя. В процессе работы необходимо контролировать уро-вень штейна, не допуская его чрезмерного роста.
При снижении температуры в подфурменной зоне и высоком содержании магнетита, магнетит, может выделиться в самостоятельную фазу. Магнетит, имея промежуточное между штейном и шлаком значение плотности, образует слой на границе шлаковой и штейновой ванн, затрудняя разделение шлака и штейна. Наличие промежуточного слоя легко контролируется при измерении высоты штейновой ванны.
Штейн представляет собой расплав сульфидов меди, никеля, кобальта, железа, в котором растворен кислород, драгоценные металлы, редкие и рассеянные элементы. С увеличением суммы массовых долей меди и никеля в штейне, массовая доля кислорода в нем уменьшается.
Массовая доля серы в штейне снижается по мере его обогащения цветными металлами, что связано с меньшей массовой концентрацией серы (до 19 %) в сульфиде меди (Cu2S) по сравнению с сульфидом железа (до 36 %).
Шлак представляет собой расплав оксидов, в котором присутствует сера.
Химический состав шлака определяет такие его физические свойства, как
плотность, вязкость и поверхностное натяжение, а также способность растворять
магнетит и цветные металлы. При работе на силикатные шлаки представляет интерес
зависимость содержания магнетита в шлаке от содержания диоксида кремния. С
увеличением массовой доли диоксида кремния, уменьшается массовая доля
магнетита.
2. технико-экономические показатели
Основные технико-экономические показатели ПВ
|
Годовая производительность по концентрату, т/год |
1400000 |
|
|
Суточная производительность одной печи по концентрату, т/сут |
3835 |
|
|
Часовая производительность одной печи по кончентрату, т/час |
16 |
|
|
Площадь печи, м2 |
48 |
|
|
Удельный проплав по шихте, тонн/( м2*сутки) |
80 |
|
|
Соотношение шихты к концентрату |
100:60 |
|
|
Среднегодовой коэффициент использования ПВ в рабочем режиме |
0,91 |
|
|
Количество плавильных агрегатов ПВ |
1,66 |
|
|
Коэффициент запаса производительной мощности |
1,20 |
|
|
Температура в печи, °С |
1250-1300 |
|
|
Температура штейна, °С |
1200 |
|
|
Температура шлака, °С |
1300 |
|
|
Медно-никелевый концентрат, % в том числе: Cu-25.18; Ni-1.37; Fe-35.13; S-33.41; SiO2-1.59 |
|
|
|
Извлечение меди в штейн,% |
98 |
|
|
Извлечение никеля в штейн,% |
94 |
|
|
Содержание серы в штейне,% |
25 |
|
|
Степень десульфуризации,% |
73 |
|
|
Пылеунос серы, % |
0.4322 |
|
|
Штейн,% в том числе: Cu-30,3; Ni-2,12; Fe-4,43; S-10,7 |
|
|
|
Шлак,% в том числе: Cu-0,58; Ni-0,14; Fe-45,119; S-0,805; SiO2-27,495 |
|
|
3. Материальные потоки
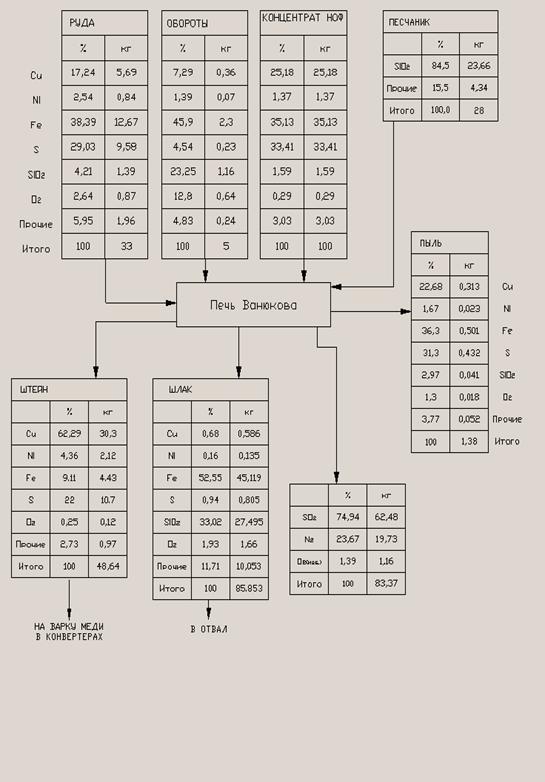
Рис.1. Схема материальных потоков.
Список литературы
1. Равдель, А.А. Краткий справочник физическо-химических величин [Текст] / А.А. Равдель, A.M. Пономарева. - Л.: Химия, 1983. - 231 с.
. Киреев, В.А. Краткий курс физической химии [Текст] / В.А. Киреев- М.: Химия, 1978. - 620 с.
. Справочник по расчетам металлургических реакций [Текст] / А.Н. Крестовников [и др.]. - М.: Металлургия, 1963. - 416 с.