Материал: Расчеты термодинамических функций металлургических процессов
![]() =
19,83+16,75×10-3·1300 = 41,605 Дж/моль·K;
=
19,83+16,75×10-3·1300 = 41,605 Дж/моль·K;
![]() =
48,28+8,54·10-3·1300 +
=
48,28+8,54·10-3·1300 + ![]() = 59,481 Дж/моль·K;
= 59,481 Дж/моль·K;
![]() =
17,24+24,77·10-3·1300 = 49,441 Дж/моль·K.
=
17,24+24,77·10-3·1300 = 49,441 Дж/моль·K.
Рассчитаем
теплоемкость для химической реакции:
![]()
![]()
![]()
![]()
![]() =
= ![]() = 1,4
= 1,4
Kp = 25,119
· Т = 1500 °К:
![]()
![]() =
19,83+16,75×10-3·1500 = 44,955 Дж/моль·K;
=
19,83+16,75×10-3·1500 = 44,955 Дж/моль·K;
![]() =
48,28+8,54·10-3·1500 +
=
48,28+8,54·10-3·1500 + ![]() = 61,164 Дж/моль·K;
= 61,164 Дж/моль·K;
![]() =
17,24+24,77·10-3·1500 = 54,395 Дж/моль·K.
=
17,24+24,77·10-3·1500 = 54,395 Дж/моль·K.
Рассчитаем
теплоемкость для химической реакции:
![]()
![]()
![]()
![]()
![]() =
= ![]() = 1,165
= 1,165
Kp = 14,622
· Т = 1700 °К:
![]()
![]() =
19,83+16,75×10-3·1700 = 48,305 Дж/моль·K;
=
19,83+16,75×10-3·1700 = 48,305 Дж/моль·K;
![]() =
48,28+8,54·10-3·1700 +
=
48,28+8,54·10-3·1700 + ![]() = 62,856 Дж/моль·K;
= 62,856 Дж/моль·K;
![]() =
17,24+24,77·10-3·1700 = 59,349 Дж/моль·K.
=
17,24+24,77·10-3·1700 = 59,349 Дж/моль·K.
Рассчитаем
теплоемкость для химической реакции:
![]()
![]()
![]()
![]()
![]() =
= ![]() = 0,947
= 0,947
Kp = 8,851
· Т = 1900 °К:
![]()
![]() =
19,83+16,75×10-3·1900 = 51,655 Дж/моль·K;
=
19,83+16,75×10-3·1900 = 51,655 Дж/моль·K;
![]() =
48,28+8,54·10-3·1900 +
=
48,28+8,54·10-3·1900 + ![]() = 64,552 Дж/моль·K;
= 64,552 Дж/моль·K;
![]() =
17,24+24,77·10-3·1900 = 60,303 Дж/моль·K.
=
17,24+24,77·10-3·1900 = 60,303 Дж/моль·K.
Рассчитаем
теплоемкость для химической реакции:
![]()
![]()
![]()
![]()
![]() =
= ![]() = 0,72
= 0,72
Kp = 5,248
Таблица 2. Рассчитанные теплоемкости для составляющих данной реакции при различных температурах
|
Т, °К |
CрFeO |
CрCo |
CрCoO |
CрFe |
DCрх.р |
|
|
Дж/моль×°К |
||||
|
298 |
49,64 |
24,82 |
52,705 |
24,621 |
-2,863 |
|
500 |
53,781 |
28,205 |
53,218 |
29,625 |
-0,857 |
|
700 |
56,151 |
31,555 |
54,599 |
34,579 |
-1,472 |
|
900 |
58,14 |
34,905 |
56,172 |
39,533 |
-2,66 |
|
1100 |
59,997 |
38,255 |
57,812 |
44,487 |
-4,047 |
|
1300 |
61,797 |
41,605 |
59,481 |
49,441 |
-5,52 |
|
1500 |
63,568 |
44,955 |
61,164 |
54,395 |
-7,036 |
|
1700 |
65,322 |
48,305 |
62,856 |
59,349 |
-8,578 |
|
1900 |
67,067 |
51,655 |
64,552 |
64,303 |
-10,133 |
Таблица 3. Рассчитанные термодинамические величины для составляющих данной реакции при различных температурах
|
Т, °К |
DHх.р, кДж/моль |
DSх.р, Дж/моль |
DGх.р, кДж/моль |
lgKрх.р |
|
298 |
-25,940 |
10,710 |
-29,132 |
5,115 |
|
500 |
-26,113 |
10,266 |
-31,246 |
3,270 |
|
700 |
-26,532 |
9,453 |
-33,149 |
2,478 |
|
900 |
-27,541 |
7,770 |
-34,534 |
2,000 |
|
1100 |
-29,186 |
5,425 |
-35,153 |
1,672 |
|
1300 |
-31,471 |
2,579 |
-34,824 |
1,400 |
|
1500 |
-34,397 |
-0,661 |
-33,406 |
1,165 |
|
1700 |
-37,966 |
-4,227 |
-30,780 |
0,947 |
|
1900 |
-42,141 |
-8,426 |
-26,132 |
0,720 |
По полученным данным строим графики зависимостей DH, DS, DG, Kp, DCp как
функций от температуры и зависимость lgKp как функции от обратной температуры 1/Т.
3.2 Приближенный расчет по методу Л.П.
Владимирова
Воспользуемся рассчитанными данными из таблицы 3, тогда:
DH°х.р = -34,397кДж/моль;
DS°х.р = -0,661 Дж/моль.
Рассчитаем теперь lgKp
для рабочей температуры (Траб = 1500 °К):
lgКр = ![]() , где
, где
М
= ![]() =
= ![]()
lgКр = ![]() -0,0346 = 1,165
-0,0346 = 1,165
Кр
= 14,622
3.3 Расчет lgKp методом Темкина-Шварцмана
Проведем
расчеты DH при
Т = 298 °К для химической реакции:
![]()
Проведем
расчеты DS при
Т = 298 °К для химической реакции:
![]()
Для рабочей температуры (Траб = 1500 °К) рассчитаем Dа, Db и Dс:
Dа =![]() = (50,8 + 19,83) - (48,28+17,24) = 5,11;
= (50,8 + 19,83) - (48,28+17,24) = 5,11;
Db =![]() =
(8,61+16,75) - (8,54+24,17) = -7,95;
=
(8,61+16,75) - (8,54+24,17) = -7,95;
Dс =![]() = -3,31 - 1,67 = -4,98.
= -3,31 - 1,67 = -4,98.
Расчет по этому методу требует отыскания по вспомогательной таблице значений температурных функций M0, M1, M2 и M-2, которые были заранее вычислены для соответствующих температур.
В
случае отсутствия в таблице необходимых значений этих функций для какой-либо
температуры, их можно вычислить по следующим формулам:
M0 = ![]() M1 =
M1 = ![]()
M2 = ![]() M-2 =
M-2 = ![]()
Таким
образом значения для Т = 1500°К равны:
М0 = 0,8144; М1×103 = 0,482; М-2×10-5 = 0,361.
Рассчитываем энергию Гиббса, lgКр и Кр:
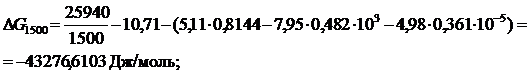
lgKр1500 = 1,5095
Кр
= 32,3221
3.4 Расчет lgKр по методу Л.П. Владимирова
Необходимо составит таблицу с данными, рассчитанными по формулам:
![]() ;
; ![]() ;
; ![]() ;
; ![]() ;
; ![]()
· СоО:
![]() ;
; ![]() ;
;
![]() ;
; ![]() ;
;
![]()
· Fe:
![]() ;
; ![]() ;
;
![]() ;
; ![]() ;
;
![]()
· FeО:
![]() ;
; ![]() ;
;
![]() ;
; ![]() ;
;
![]()
· Со:
![]() ;
; ![]() ;
;
![]() ;
; ![]() ;
;
![]()
Δƒ(М·103) = 13,8576 - 12,4999 = 1,3577
Δƒ(N) = (3,1785 + 1,5717) - (2,7693 + 1,4205) = 0,5604
Δƒ(С0) = (2,6579 + 1,0375) - (2,5260 + 0,9020) = 0,2674
Δƒ(С1·10-3) = (0,4505 + 0,8674) - (0,4468 + 1,2960) = -0,4250
Δƒ(С-2·105) = (-0,1732) - 0,0873 = -0,2605
Значения
температурных функций f(T) возьмем из «Справочника по расчетам равновесий
металлургических реакций» А.Н. Крестовникова.
[Δƒ * ƒ(T)] = 1,3577 * 0,6667 = 0,9052
[Δƒ * ƒ(T)] = 0,5604
[Δƒ * ƒ(T)] = 0,2674 * 0,8141 = 0,2178
[Δƒ * ƒ(T)] = -0,4250 * 0,4820 = -0,2049
[Δƒ * ƒ(T)] = -0,2605 *
0,3610 = -0,0940
Таблица 4. Термодинамические данные
|
Реагент |
М·10-3 |
N |
С0 |
С1·103 |
С-2·10-5 |
lgKр |
|
CoO |
12.4999 |
2,7693 |
2,5260 |
0,4468 |
0,0873 |
- |
|
Fe |
0 |
1,4205 |
0,9020 |
1,2960 |
0 |
- |
|
FeO |
13,8576 |
3,1785 |
2,6579 |
0,4505 |
-0,1732 |
- |
|
Co |
0 |
1,5717 |
1,0375 |
0,8674 |
0 |
- |
|
Df |
1,3577 |
0,5604 |
0,2674 |
-0,4250 |
-0,2605 |
- |
|
f(T) |
0,6667 |
- |
0,8141 |
0,4814 |
0,3610 |
- |
|
Df·f(T) |
0,9052 |
0,5604 |
0,2178 |
-0,2049 |
0,094 |
1,5095 |
По данным табл. 4 Kр =
32,3221
3.5 Расчет ошибки методов
Логарифмы Kр, найденные
различными методами, заносим в таблицу 5.
Таблица 5. Результаты lgKр и Kр
|
Методы |
lgKр |
Kр |
D, % |
|
По графику |
1,165 |
- |
77,17 |
|
Крестовникова |
1,165 |
- |
|
|
Владимирова (прибл.) |
1,165 |
- |
|
|
Темкина-Шварцмана |
1,5095 |
- |
- |
|
Владимирова (точн.) |
1,5095 |
- |
|
Так как разных LgKр
только два показателя, то расчет ошибки будет один:
D = ![]() =
= ![]() =
77,17%.
=
77,17%.
3.6 Построение и анализ графиков
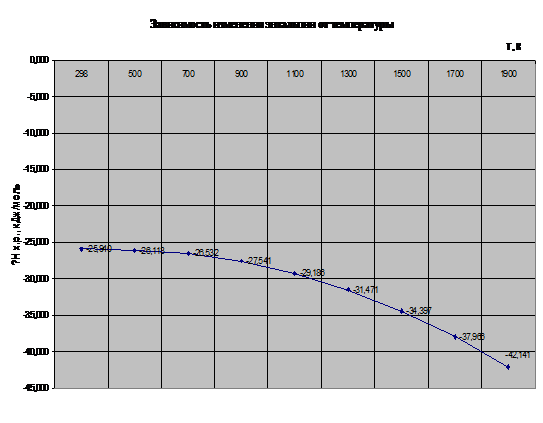
Рис. 1. Зависимость изменения энтальпии от температуры
Рассмотрим график зависимости энтальпии от температуры (рис.1) . Видно,
что с увеличением температуры энтальпия уменьшается, следовательно, реакция
экзотермична, т.е. идет с выделением тепла. В этом случае реакция окисления
металлического железа кислородом оксида кобальта в процессе конвертирования
никелевого штейна в конвертере будет самопроизвольно протекать в прямом
направлении, только при условии, что ΔS >0.
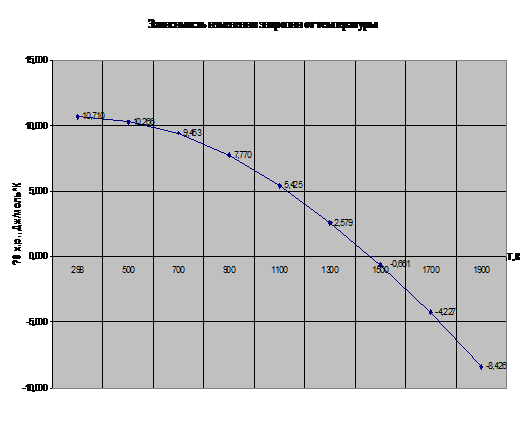
Рис. 2. Зависимость изменения энтропии от температуры
Рассмотрим график зависимости энтропии от температуры (рис.2) . Так как энтропия - это функция состояния термодинамической системы, а также количественная мера ее беспорядка, то можно сказать, что с увеличением температуры, уменьшается хаотичность движения частиц, т.е. уменьшается беспорядочность термодинамической системы.
Из
уравнения ΔG0х.р.= ΔH0х.р.
- ΔS0х.р.![]() Т следует, что чем выше температура, тем больше
влияние энтропии на направление процесса. Это объясняется тем, что с ростом
температуры увеличивается интенсивность теплового движения, которое
преодолевает связи между частицами. При низких температурах, наоборот, основное
влияние оказывает изменение энергии, т.к. величина ΔS0
Т следует, что чем выше температура, тем больше
влияние энтропии на направление процесса. Это объясняется тем, что с ростом
температуры увеличивается интенсивность теплового движения, которое
преодолевает связи между частицами. При низких температурах, наоборот, основное
влияние оказывает изменение энергии, т.к. величина ΔS0 ![]() T становится
малой по сравнению с ΔH.
Как видно из графика при рабочей температуре 15000 именно энтропия оказывает
решающее воздействие на реакцию окисления металлического железа кислородом
оксида кобальта.
T становится
малой по сравнению с ΔH.
Как видно из графика при рабочей температуре 15000 именно энтропия оказывает
решающее воздействие на реакцию окисления металлического железа кислородом
оксида кобальта.
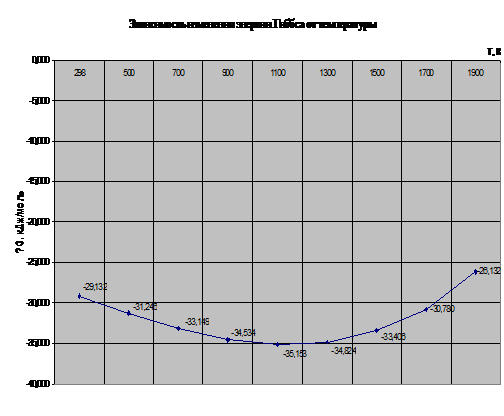
Рис. 3. Зависимость изменения энергии Гиббса от
температуры