Материал: Производство серной кислоты нитрозным методом
где ![]() -парциальное давление
-парциальное давление ![]() ,
, ![]() ,
, ![]() в газовой фазе соответственно,0,1 МПа;
Р- общее давление газа,0,1 МПа;X-равновесная
степень окисления
в газовой фазе соответственно,0,1 МПа;
Р- общее давление газа,0,1 МПа;X-равновесная
степень окисления ![]() ,доли единицы;n-объем кислорода в
,доли единицы;n-объем кислорода в ![]() газа,
газа, ![]() ;m-объем
;m-объем ![]() в 1
в 1 ![]() газа,
газа, ![]() .
.
Чтобы определить степень окисления ![]() при определенной температуре и заданном составе исходной главной смеси, необходимо в это уравнение подставить значение
при определенной температуре и заданном составе исходной главной смеси, необходимо в это уравнение подставить значение ![]() при
данной температуре,
найденное по уравнению (3). При температуре ниже 200 °С содержание
при
данной температуре,
найденное по уравнению (3). При температуре ниже 200 °С содержание ![]() в равновесной газовой смеси
в равновесной газовой смеси ![]() ,
, ![]() и
и ![]() ничтожно. Поэтому можно
принять, что в нитрозном процессе скорость диссоциации
ничтожно. Поэтому можно
принять, что в нитрозном процессе скорость диссоциации ![]() очень мала и при подсчете скорости окисления
очень мала и при подсчете скорости окисления ![]() по реакции (1) скорость обратной реакции можно не учитывать. В этих условиях время
по реакции (1) скорость обратной реакции можно не учитывать. В этих условиях время ![]() , необходимое для окисления
, необходимое для окисления ![]() до степени X, можно найти из уравнения
до степени X, можно найти из уравнения
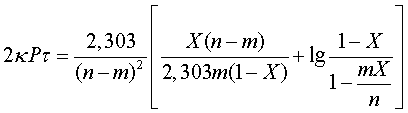 (18)
(18)
где ![]() -константа скорости реакции окисления
-константа скорости реакции окисления ![]() по реакции (1).
по реакции (1).
Отсюда время окисления половины всего оксида азота (Х=0,5) составит
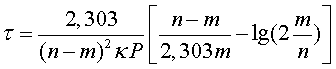 (19)
(19)
Ниже приведена зависимость
константы ![]() скорости
реакции (1)
от температуры t (содержание компонентов выражено через парциальные давления в МПа):
скорости
реакции (1)
от температуры t (содержание компонентов выражено через парциальные давления в МПа):
![]() 0 30 60 90
140 200 240
0 30 60 90
140 200 240
Из этих данных следует, что
скорость реакции окисления уменьшается с повышением температуры.
Это и отличает реакцию (1) от большинства гомогенных газовых реакций.
Список использованных источников
1. Амелин А.Г: Технология серной кислоты. учебное пособие для вузов.-2-ое изд.,перераб.-М.,Химия,1983.-360 с.,ил.
2.Боресков Г.К.: Катализ в производстве серной кислоты.М.Госхимиздат,1954.
3. Материалы с сайте URL: http://www.engineer-oht.ru
4. Боресков Г.К, Слинько М.Г, Бесков В.С.-Количество
катализатора, устойчивость и параметрическая чувствительность в контактных
аппаратах окисления двуокиси серы. Химпром.,1968,№ 3,с. 13.
Содержание
с.
Производство серной кислоты нитрозным методом 2
Физико-химические основы нитрозного процесса 6
Свойства нитрозы 8
Скорость абсорбции оксидов азота 10
Абсорбции диоксида серы нитрозой 13
Окисление диоксида серы нитрозой 14
Удаление оксидов азота из нитрозы(денитрация) 15
Окисление NO кислородом в газовой фазе 16
Список использованных источников 19