Материал: Производство серной кислоты нитрозным методом
Производство серной кислоты нитрозным методом
Производство серной кислоты нитрозным методом
Сущность нитрозного метода состоит в том, что обжиговый газ после очистки от пыли обрабатывается серной кислотой, в которой растворены оксиды азота, — так называемой нитрозой. Диоксид серы поглощается нитрозой и затем окисляется оксидами азота по реакции
![]()
Образующийся ![]() плохо растворим в нитрозе
и поэтому выделяется из нее, а затем
частично окисляется кислородом в газовой фазе до диоксида
плохо растворим в нитрозе
и поэтому выделяется из нее, а затем
частично окисляется кислородом в газовой фазе до диоксида ![]() . Смесь оксидов азота
. Смесь оксидов азота ![]() и
и ![]() вновь
поглощается серной кислотой и т. д. Оксиды азота, по существу,
не расходуются в нитрозном процессе и возвращаются в
производственный цикл. Однако вследствие неполного
поглощения их серной кислотой они частично уносятся отходящими газами; это
составляет невозвратимые потери оксидов.
вновь
поглощается серной кислотой и т. д. Оксиды азота, по существу,
не расходуются в нитрозном процессе и возвращаются в
производственный цикл. Однако вследствие неполного
поглощения их серной кислотой они частично уносятся отходящими газами; это
составляет невозвратимые потери оксидов.
Процесс производства серной кислоты нитрозным методом состоит из следующих стадий:
1)получение ![]() ;
;
2)поглощение
![]() нитрозой;
нитрозой;
3)окисление
![]() нитрозой;
нитрозой;
4)освобождение нитрозы от оксидов азота (денитрация);
5)окисление
выделившегося из нитрозы оксида азота кисло
родом в газовой фазе;
6)поглощение оксидов азота серной кислотой.
Раньше нитрозный процесс
осуществляли в свинцовых камерах, потому он назывался камерным
способом. В настоящее время этот способ, как малопроизводительный,
в СССР не применяется. Вместо него применяют башенный способ, по которому
все основные и промежуточные процессы переработки ![]() протекают
не в камерах, а в башнях, заполненных насадкой и орошаемых серной кислотой.
протекают
не в камерах, а в башнях, заполненных насадкой и орошаемых серной кислотой.
На рис.1 изображена принципиальная схема
производства серной кислоты башенным
способом. Первая башня, в которую поступает
горячий обжиговый газ, предназначена для выделения оксидов азота из кислоты, орошающей башню. Этот
процесс называют денитрацией серной
кислоты, а башня 1 носит название денитрационной. Около ![]() денитрационной кислоты, вытекающей из этой башни, передают на склад как
готовую продукцию, а остальное
поступает на орошение последней башни 4.
денитрационной кислоты, вытекающей из этой башни, передают на склад как
готовую продукцию, а остальное
поступает на орошение последней башни 4.
Рис.1 Принципиальная схема башенной системы.
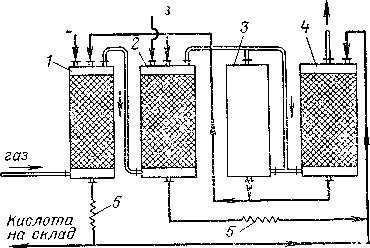
1-денитрационная башня;
2-продукционная башня;
3-окислительная башня;
4-абсорбционная башня;
5-холодильники кислоты.
Денитрационная башня
орошается небольшим количеством серной кислоты, поэтому
кислота в ней сильно нагревается, что способствует выделению оксидов азота.
Одновременно с денитрацией кислоты в башне 1 диоксид серы
частично абсорбируется серной кислотой и окисляется оксидами
азота. По характеру протекающих процессов первую башню можно схематически разделить
на три зоны. В нижней зоне происходит упаривание серной кислоты с
выделением паров воды в газовую фазу, в средней зоне оксиды азота выделяются из
нитрозы в результате наибольшего ее разбавления, в верхней зоне
конденсируются поступающие снизу пары воды и, следовательно,
происходит разбавление нитрозы и частичное окисление растворяющегося
в ней ![]() .
.
Строгого разделения
перечисленных процессов по зонам провести нельзя, так как
частично они совмещаются друг с другом. Кроме протекания этих процессов, в
первой башне из газа улавливаются также остатки пыли, поглощаются
мышьяковистый ангидрид и диоксид селена, конденсируются пары серной кислоты (образуются из ![]() , присутствующего в обжиговом газе) и др. Туман серной кислоты лишь частично
поглощается в первой башне, большая
часть его поступает в последующие башни системы, где вследствие большой суммарной поверхности частиц тумана он
оказывает существенное влияние на протекающие в башнях процессы.
, присутствующего в обжиговом газе) и др. Туман серной кислоты лишь частично
поглощается в первой башне, большая
часть его поступает в последующие башни системы, где вследствие большой суммарной поверхности частиц тумана он
оказывает существенное влияние на протекающие в башнях процессы.
Готовую продукцию в башенных системах отводят только из денитрационной башни, где почти полностью улавливаются все примеси обжигового газа, поэтому башенная кислота загрязнена мышьяком, селеном, огарковой пылью и другими примесями.
Основное назначение второй башни— абсорбция
диоксида серы из обжигового газа серной
кислотой и окисление ![]() нитрозой.
В этой башне образуется большая часть серной кислоты (70—80% всей
продукции), поэтому ее часто называют продукционной
башней. Процесс образования кислоты протекает по всей высоте башни 2,
однако основное количество
нитрозой.
В этой башне образуется большая часть серной кислоты (70—80% всей
продукции), поэтому ее часто называют продукционной
башней. Процесс образования кислоты протекает по всей высоте башни 2,
однако основное количество ![]() окисляется в ее нижней части, где создаются условия,
наиболее благоприятные для этого
процесса. Оксиды азота, выделяющиеся
из нитрозы при окислении
окисляется в ее нижней части, где создаются условия,
наиболее благоприятные для этого
процесса. Оксиды азота, выделяющиеся
из нитрозы при окислении ![]() ,
частично поглощаются в верхней части башни орошающей ее нитрозой,
но большая часть оксидов поступает вместе с газовым потоком в
окислительную башню
3. Здесь окисляется такое количество оксида азота, которое требуется,
чтобы соотношение между
,
частично поглощаются в верхней части башни орошающей ее нитрозой,
но большая часть оксидов поступает вместе с газовым потоком в
окислительную башню
3. Здесь окисляется такое количество оксида азота, которое требуется,
чтобы соотношение между ![]() и
и ![]() соответствовало
образованию
соответствовало
образованию ![]() ; в
таком виде оксиды азота наиболее полно поглощаются в абсорбционных
башнях.
; в
таком виде оксиды азота наиболее полно поглощаются в абсорбционных
башнях.
В башне 3 ![]() окисляется кислородом,
содержащимся в газе. Степень его окисления
регулируют, пропуская часть газа по обводному
газопроводу помимо башни (байпас). Из окислительной башни газ поступает
в башню 4, где оксиды азота поглощаются
орошающей ее серной кислотой; эту башню называют абсорбционной, или поглотительной.
окисляется кислородом,
содержащимся в газе. Степень его окисления
регулируют, пропуская часть газа по обводному
газопроводу помимо башни (байпас). Из окислительной башни газ поступает
в башню 4, где оксиды азота поглощаются
орошающей ее серной кислотой; эту башню называют абсорбционной, или поглотительной.
При охлаждении обжигового газа и
образовании серной кислоты выделяется большое количество тепла,
поэтому в денитрационной и продукционных башнях орошающая кислота нагревается
и перед возвратом на орошение ее приходится охлаждать. Для этого установлены холодильники 5.
При производстве башенной кислоты
неизбежны потери оксидов азота с
отходящими газами, с продукционной кислотой и др. Для восполнения этих потерь в денитрационную башню 1 и
продукционную башню 2 подается азотная кислота. Вода, необходимая для образования серной кислоты, также вводится
в эти башни.
Физико-химические основы нитрозного процесса
В нитрозном процессе окисление ЗО2 происходит с помощью оксидов азота, растворенных в серной кислоте, поэтому прежде всего необходимо рассмотреть свойства оксидов азота и абсорбцию их серной кислотой.
Оксид азота ![]() представляет собой
бесцветный газ, сжижающийся в бесцветную
жидкость при атмосферном давлении и температуре — 151,8 °С. Кислород
окисляет
представляет собой
бесцветный газ, сжижающийся в бесцветную
жидкость при атмосферном давлении и температуре — 151,8 °С. Кислород
окисляет ![]() в газовой фазе
в газовой фазе
![]() кДж (1)
кДж (1)
Эта реакция отличается от большинства гомогенных реакций тем, что ее скорость понижается с повышением температуры.
В зависимости от температуры и концентрации ![]() и
и ![]() в газовой фазе устанавливается определенное равновесие между компонентами реакционной массы. Зависимость
константы равновесия
в газовой фазе устанавливается определенное равновесие между компонентами реакционной массы. Зависимость
константы равновесия ![]() реакции (1)
реакции (1)
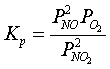 (2)
(2)
от абсолютной температуры Т выражается уравнением
![]() (3)
(3)
где ![]() -парциальные давления
-парциальные давления ![]() в газовой фазе,МПа.
в газовой фазе,МПа.
Следует полагать, что окисление ![]() кислородом протекает также и в жидкой фазе
кислородом протекает также и в жидкой фазе
![]() (4)
(4)
Диоксид азота ![]() — темно-бурый газ, сжижающийся при атмосферном давлении уже в условиях комнатной
температуры (20,7 °С). Диоксид азота превращается в тетраксид (бесцветный газ) по реакции
— темно-бурый газ, сжижающийся при атмосферном давлении уже в условиях комнатной
температуры (20,7 °С). Диоксид азота превращается в тетраксид (бесцветный газ) по реакции
![]() кДж (5)
кДж (5)
Зависимость константы равновесия этой реакции
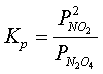 (6)
(6)
от температуры выражается уравнением
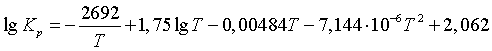 (7)
(7)
где ![]() ,
,
![]() -парциальные давления
-парциальные давления ![]() и
и ![]() в газовой фазе, МПа.
в газовой фазе, МПа.
В нитрозных газах общее
содержание оксидов азота меньше 15%, а степень окисления ![]() редко превышает 0,5,
поэтому из уравнения (7) следует, что возможное содержание
редко превышает 0,5,
поэтому из уравнения (7) следует, что возможное содержание ![]() в газах нитрозного процесса
очень мало.
в газах нитрозного процесса
очень мало.
С серной кислотой диоксид азота образует нитрозилсерную и азотную кислоты
![]() кДж (8)
кДж (8)
Оксид азота ![]() (азотистый ангидрид) при
комнатной температуре представляет собой газ; это соединение
устойчиво только
при высоком давлении. При 25 °С и давлении 0,1 МПа лишь 10,5% эквимолекулярной
смеси оксидов азота
(азотистый ангидрид) при
комнатной температуре представляет собой газ; это соединение
устойчиво только
при высоком давлении. При 25 °С и давлении 0,1 МПа лишь 10,5% эквимолекулярной
смеси оксидов азота ![]() находится
в виде
находится
в виде ![]() ; остальное количество
азотистого ангидрида разлагается на
; остальное количество
азотистого ангидрида разлагается на ![]() и
и ![]() . При температуре 3,5 °С азотистый ангидрид снижается с образованием жидкости
сине-голубого цвета, которая также быстро разлагается.
. При температуре 3,5 °С азотистый ангидрид снижается с образованием жидкости
сине-голубого цвета, которая также быстро разлагается.
Равновесие реакции образования азотистого ангидрида
![]() кДж (9)
кДж (9)
сдвигается вправо при понижении температуры и повышении давления, причем состояние равновесия устанавливается очень быстро. Константа равновесия этой реакции
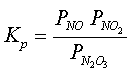 (10)
(10)
определяется при различной температуре следующими уравнениями
при ![]()
![]() (11)
(11)
при ![]()
![]() (12)
(12)
где М - условная мольная концентрация всех оксидов азота.
В пересчете на ![]() (в моль/л) условная мольная концентрация составляет
(в моль/л) условная мольная концентрация составляет
![]() (13)
(13)
В условиях нитрозного процесса
содержание азотистого ангидрида в газе по сравнению с суммарным
содержанием ![]() весьма незначительно.
весьма незначительно.
С серной кислотой ![]() образует нитрозилсерную
кислоту
образует нитрозилсерную
кислоту
![]() кДж (14)
кДж (14)
Свойства нитрозы
В технике нитрозой называют
растворы оксидов
азота (![]() ) в водных растворах серной кислоты. Оксиды азота в зависимости от степени их окисления
образуют нитрозилсерную кислоту в соответствии с уравнением (14) или
нитрозилсерную и азотную кислоты - с уравнением (8).
) в водных растворах серной кислоты. Оксиды азота в зависимости от степени их окисления
образуют нитрозилсерную кислоту в соответствии с уравнением (14) или
нитрозилсерную и азотную кислоты - с уравнением (8).
Нитрозилсерная кислота представляет собой бесцветные
гигроскопические кристаллы (т. пл. ![]() ),расплывающиеся при соприкосновении
с влажным атмосферным воздухом. Нитрозилсерная кислота, полученная при растворении
оксидов азота в безводной серной кислоте, вполне устойчива, в водных же
растворах серной кислоты она гидролизуется
),расплывающиеся при соприкосновении
с влажным атмосферным воздухом. Нитрозилсерная кислота, полученная при растворении
оксидов азота в безводной серной кислоте, вполне устойчива, в водных же
растворах серной кислоты она гидролизуется
![]() (15)
(15)
Степень гидролиза
нитрозилсерной кислоты увеличивается с повышением температуры и
понижением конденсации серной кислоты. В зависимости от содержания ![]() в исходной кислоте
степень гидролиза нитрозилсерной кислоты при комнатной температуре
изменяется следующим образом:
в исходной кислоте
степень гидролиза нитрозилсерной кислоты при комнатной температуре
изменяется следующим образом:
Содержание ![]() , % 98 95 92 90 87
80 70 57
, % 98 95 92 90 87
80 70 57
Степень гидролиза
![]() , % . . . . 1,1 4,0 7,3
12,4 19,4 27,7 49,8 100
, % . . . . 1,1 4,0 7,3
12,4 19,4 27,7 49,8 100
![]() (16)
(16)
Растворимость ![]() в водных растворах
серной кислоты очень мала; в нитрозе она
несколько больше, растворимость повышается
при увеличении концентрации нитрозилсерной кислоты и исходной серной кислоты и понижается с ростом
температуры. Ниже приведены данные о
растворимости оксида азота в нитрозе (в %) при давлении, равном 0,1 МПа
(760 мм рт. ст.) и температуре 40 °С:
в водных растворах
серной кислоты очень мала; в нитрозе она
несколько больше, растворимость повышается
при увеличении концентрации нитрозилсерной кислоты и исходной серной кислоты и понижается с ростом
температуры. Ниже приведены данные о
растворимости оксида азота в нитрозе (в %) при давлении, равном 0,1 МПа
(760 мм рт. ст.) и температуре 40 °С: