Материал: Проектирование в условиях г. Владикавказа отделения обжига гранулированного молибденитового концентрата производительностью 6800 т/год
Ковеллин:
![]()
![]()
Аурипигмент:
![]()
![]()
Сульфид рения:
![]()
![]()
Всего серы в сульфидах:
![]()
что соответствует анализу (в дальнейших расчетах используем уточненное значение, полученное расчетом).
Шеелит:
![]()
![]()
![]()
![]()
Апатит:
![]()
![]()
![]()
![]()
Израсходовано СаО:
![]()
Остаток
СаО = 0,8 - ![]()
![]() = 0,654
кг связан в кальцит:
= 0,654
кг связан в кальцит:
![]()
![]()
![]()
Таблица 2
Рациональный состав концентрата (на 100 кг влажного)
|
Компонент |
Mo |
Fe |
Cu |
As |
Re |
S |
CaO |
WO3 |
CO2 |
P2O5 |
SnO2 |
SiO2 |
H2O |
Флото реаг. |
Прочие |
Итого |
Плот ность |
Объем |
|
MoS2 |
52,800 |
|
|
|
|
35,288 |
|
|
|
|
|
|
|
|
|
88,088 |
4,8 |
17,935 |
|
FeS2 |
|
1,500 |
|
|
|
1,722 |
|
|
|
|
|
|
|
|
|
3,222 |
5 |
0,859 |
|
CuS |
|
|
0,650 |
|
|
0,328 |
|
|
|
|
|
|
|
|
|
0,978 |
4,6 |
0,196 |
|
As2S3 |
|
|
|
0,050 |
|
0,032 |
|
|
|
|
|
|
|
|
|
0,082 |
3,43 |
0,024 |
|
ReS2 |
|
|
|
|
0,060 |
0,021 |
|
|
|
|
|
|
|
|
|
0,081 |
7,5 |
0,007 |
|
CaWO4 |
|
|
|
|
|
|
0,092 |
0,378 |
|
|
|
|
|
|
|
0,470 |
6,06 |
0,039 |
|
Ca3(PO4)2 |
|
|
|
|
|
0,054 |
|
|
0,046 |
|
|
|
|
|
0,100 |
3,14 |
0,048 |
|
|
CaCO3 |
|
|
|
|
|
|
0,654 |
|
0,513 |
|
|
|
|
|
|
1,167 |
2,7 |
0,775 |
|
SnO2 |
|
|
|
|
|
|
|
|
|
|
0,038 |
|
|
|
|
0,038 |
6,95 |
0,005 |
|
SiO2 |
|
|
|
|
|
|
|
|
|
|
|
3,200 |
|
|
|
3,200 |
2,65 |
1,208 |
|
H2O |
|
|
|
|
|
|
|
|
|
|
|
|
2,000 |
|
|
2,000 |
1 |
2,000 |
|
флотореаг. |
|
|
|
|
|
|
|
|
|
|
|
|
|
0,250 |
|
0,250 |
1 |
0,300 |
|
Прочие |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0,324 |
0,324 |
2,65 |
0,212 |
|
Итого |
52,800 |
1,500 |
0,650 |
0,050 |
0,060 |
37,391 |
0,800 |
0,378 |
0,513 |
0,046 |
0,038 |
3,200 |
2,000 |
0,250 |
0,324 |
100,000 |
4,236 |
23,608 |
Касситерит:
![]()
![]()
Кварц: 3,20 кг.
В
нем ![]()
![]()
Всего связанного кислорода в сухом концентрате:
![]()
![]() + 0,041
+
+ 0,041
+ ![]()
![]() + 0,008
+ 1,704 = 2,417 кг.
+ 0,008
+ 1,704 = 2,417 кг.
Составляем таблицу рационального состава концентрата (табл. 2.1).
.3 Расчет состава и выхода огарка и пыли из 100 кг концентрата
Образованием MоO2 при обжиге в кипящим слое пренебрегаем. Принимаем, что весь мышьяк (в виде Аs2S3) окисляется до нелетучего As2O5 (хотя на практике часть мышьяка отгоняется в виде As2O3, мы этим пренебрежем ввиду малого содержания мышьяка в концентрате).
"Прочие" компоненты при обжиге не изменяются.
Вода испаряется и переходит в газы.
Основные реакции при обжиге молибденитового концентрата:
MoS2 + 3,5О2 = МоО3 + 2SО2; (2.2)
FeS2 + 11О2 =2FeO + 8SО2; (2.3)
4FeS2 + 11О2 = FeO + 2SО2; (2.4)+ 1,5O2 = CuO + S02; (2.5)
As2S3 + 11O2 = As2O3 + 2S02; (2.6)
ReS2 + 15O2 = Re2O7 + 2S02; (2.7)
Припишем, что фотореагенты представлены керосином, который сгорает по
реакции:
CI0H22 + I5,5О2 = 10CO2 +
11H2O; (2.8)
Побочные реакции при обжиге - образование сульфатов и молибдатов тяжелых
металлов и кальция, перрената кальция:
2SO2 + O2 = 2SO3; (2.9)
FeO + SО3 = FeSO4; (2.10)+ SO3 = CuSO4; (2.11)+ SO3 = CaSO4 + CO2; (2.12)
FeO + MoO3 = FeMoO4; (2.13)+ MoO3 = CuMoO4; (2.14)О3 + MoO3 = CaMoO4 + CО2; (2.15)О7 + CaCO3 = Ca(ReO4)2 + CO2 (2.16)
По данным А.Н. Зеликмана, СаО кальцита на 10 % переходит при обжиге в СаМоО4 и на 90% в СаSО4 10%; Сu образует СuМоО4, 30% Сu образует CuSO4, остальная медь связана в СuО; 8% Fе образует FeSO4, остальное железо связано в Fe2O3; вся сульфидная сера в огарке (и пылях) связана с молибденом; MgO, SiО2, CaWO4, Са3(PO4)2, CaMoO4, Al2O3 переходят в огарок и пыль, без изменения.
Для определения количеств твердых продуктов обжига (огарка, циклонной
пыли, пыли электрофильтров и скруббера) сначала определим состав и количество
побочных продуктов обжига на 100 кг концентрата.
Молибдат кальция:
![]()
![]()
![]()
![]()
Сульфат кальция:
![]()
![]()
![]()
![]()
Молибдат меди:
![]()
![]()
![]()
![]()
Сульфат меди:
![]()
![]()
![]()
![]()
Оксид меди:
![]()
![]()
![]()
Молибдат железа:
![]()
![]()
![]()
![]()
Сульфат железа:
![]()
![]()
![]()
![]()
Оксид железа:
![]()
![]()
![]()
Пентаоксид мышьяка:
![]()
![]()
Семиокись рения:
![]()
![]()
![]() ,
,
из
них 5%, т.е. ![]()
![]() кг
(0,003 кг рения), останется в огарке; 50 + 40 = 90% осаждается и улавливается в
электрофильтрах и скруббере, т.е. это
кг
(0,003 кг рения), останется в огарке; 50 + 40 = 90% осаждается и улавливается в
электрофильтрах и скруббере, т.е. это ![]()
![]() кг
(0,054 кг рения); остальное, т.е.
кг
(0,054 кг рения); остальное, т.е. ![]()
![]() кг Re2O7
(0,06 - 0,003 - 0,054 = 0,003 кг рения), теряется со сбросными газами.
кг Re2O7
(0,06 - 0,003 - 0,054 = 0,003 кг рения), теряется со сбросными газами.
Горение фотореагентов по реакции (2.8):
![]()
![]()
![]()
Количество углекислого газа, выделяющегося по реакциям (2.12), (2.15) и (2.16), составляет 0,513 кг (из рационального состава концентрата).
В нем кислорода: ![]()
Общее количество побочных продуктов обжига из 100 кг концентрата
представлено в таблице 2.2.
Таблица 2.2
Общее количество продуктов обжига из 100 кг концентрата
|
№ |
Компоненты |
Масса, кг |
В том числе, кг |
||
|
|
|
|
Mo |
SSO4 |
Кислород |
|
1 |
CaMoO4 |
|
|
|
|
|
2 |
CuMoO4 |
0,228 |
0,098 |
|
0,065 |
|
3 |
FeMoO4 |
0,464 |
0,206 |
|
0,138 |
|
4 |
CaSO4 |
1,430 |
|
0,337 |
0,672 |
|
5 |
CuSO4 |
0,489 |
|
0,098 |
0,196 |
|
6 |
FeSO4 |
0,408 |
|
0,086 |
0,172 |
|
7 |
CuO |
0,488 |
|
|
0,098 |
|
8 |
Fe2O3 |
1,759 |
|
|
0,529 |
|
9 |
As2O5 |
0,077 |
|
|
0,027 |
|
10 |
SiO2 |
3,2 |
|
|
1,704 |
|
11 |
SnO2 |
0,038 |
|
|
0,008 |
|
12 |
CaWO4 |
0,470 |
|
|
0,104 |
|
13 |
Ca3(PO4)2 |
0,100 |
|
|
0,041 |
|
14 |
Прочие |
0,324 |
|
|
- |
|
Итого: |
9,707 |
0,415 |
0,521 |
3,828 |
|
Расчет выхода твердых продуктов обжига из 100 кг концентрата для разных степеней окисления
Выход твердого продукта обжига со степенью окисления, соответствующей
огарку, т.е. 98 %
![]()
![]()
![]()
В 100 кг концентрата находится 52,8 кг молибдена. В продукте обжига будет
Мо в виде Мо03:
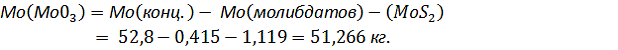
Масса триоксида молибдена:
![]()
Суммарная масса твердого продукта обжига, соответствующего по степени
окисления огарку:
m = m(Мо03)
+ m (MoS2) + m(ост.) = ![]()
![]() +
+ ![]()
![]() + 9,707=
88,489 кг,
+ 9,707=
88,489 кг,
(Re2O7 будет учтен позже),
m(ост.) - масса побочных продуктов обжига.
Выход твердого продукта обжига со степенью окисления, соответствующей циклонной пыли, т.е. 90 %:
![]()
![]()
![]()
![]()
![]()
Суммарная масса твердого продукта обжига, соответствующего по степени окисления циклонной пыли:
m = ![]()
![]() +
+ ![]()
![]() + 9,707=
89,093 кг
+ 9,707=
89,093 кг
Выход твердого продукта обжига со степенью окисления, соответствующей пыли электрофильтров и скруббера, т.е. 99 %
![]()
![]()
![]()
![]()
![]()
Суммарная масса твердого продукта обжига, соответствующего по степени окисления пыли электрофильтров и скруббера:
m = ![]()
![]() +
+ ![]()
![]() + 9,707 =
88,395 кг
+ 9,707 =
88,395 кг
(Re2O7 будет учтен позже).
Расчет одновременного выхода твердых продуктов обжига из 100 кг концентрата
х - доля концентрата, из которой формируется огарок, доли ед.;
у - доля концентрата, из которой формируется циклонная пыль, доли ед.;
z - доля концентрата, из которой формируется пыль электрофильтров и скруббера, доли ед.