Материал: Процессы гидрирования и дегидрирования органических соединений
Из соотношения продуктов превращения циклогексана в бензол и метилциклопентан и метилциклопентана в бензол и циклогексан Гензель и сотр. сделали вывод, что при действии сернистых соединений утрачивается активность фторированного алюмоплатинового катализатора по отношению к стадии превращения циклогексена в бензол, но не циклогексана в циклогексен, и, следовательно, что указанные реакции протекают на разных активных центрах. Подразделение активных центров катализаторов на такие, которые дегидрируют парафины и олефины.
К выводу о том, что для разграничения активных центров дегидрирования парафинов и олефинов нет достаточных оснований, приходим и при анализе экспериментального материала по влиянию химического состава на активность катализатора. Как правило, все активные катализаторы дегидрирования парафинов оказываются активными и в дегидрировании олефинов. О том, что это так, свидетельствуют хотя бы данные о промежуточном образовании олефинов при ароматизации парафинов, которое в противном случае не могло бы иметь места.
Наблюдается параллелизм, с одной стороны, в относительной реакционной способности насыщенных и ненасыщенных углеводородов на катализаторах различной природы, и, с другой стороны, - в соотношении активностей различных катализаторов по отношению к дегидрированию указанных углеводородов. Так, реакционная способность углеводородов возрастает с увеличением ненасыщенности на алюмохромовом, алюмомолибденовом катализаторах, платине, никеле и др.
Также наиболее активными катализаторами для реакций дегидрирования низших
парафинов в олефины и ароматизации парафинов С≥6 являются промотированные
алюмохромовые катализаторы, причем, как правило, вводимые в катализатор добавки
или изменение способа приготовления или обработки катализатора оказывают
аналогичное влияние (активация, разрабатываемость и т.д.) на реакции, а также
на дегидрирование шестичленных нафтенов (табл. 2).
Таблица 2
Влияние добавок некоторых веществ на свойства катализаторов дегидрирования
|
Исходные вещества |
Добавки |
Углеводороду |
Влияние на каталитические свойства |
|
Cr2O3 - AI2O3 |
Оксиды щелочных металлов |
Парафины C3-C7 циклогексан, изопентены |
Повышение активности |
|
То же |
CaO, SrO, BaO |
n-Бутан, n-гептан, циклогексан |
То же |
|
» |
Оксиды Fe |
n-Бутан, n-гексан |
Уменьшение активности |
|
» |
Оксиды щелочных металлов |
Изопентан, n-гептан, циклогекссан |
Замедление разработки |
|
» |
K2O |
n-Бутан, n-гептан |
Уменьшение коксообразования |
|
MoO3 - AI2O3 |
Оксиды K, Rb, Cs, Ce, Nd, HI |
n-Гексан, n-гептан, циклогесксан |
Повышение активности |
|
Pt - AI2O3 |
Na2O |
n-Гексан, циклогексан |
Активность проходит через максимум |
|
Pd - AI2O3с добав. HF |
Оксиды редкоземельных элементов |
n-Гексан, циклогексан, метилциклогексан |
Повышение активности |
Различия в удельных активностях отдельных металлов по отношению к реакциям дегидрирования циклогексана, циклогексена и циклогексадиена достигают нескольких порядков.
Если пренебречь сравнительно небольшими изменениями (в 2-3 раза), то
удельные активности металлов для дегидрирования всех трех углеводородов
располагаются в ряд:
Pd ≈ Pt ≈ Rh ≈ Ir > Ni > Ag ≈ Cu ≈ Co ≈ Fe
Естественно, представление об однотипности активных центров для дегидрирования насыщенных и ненасыщенных углеводородов не означает того, что для обеих реакций оптимальными должны быть одни и те же катализаторы.
Индивидуальные особенности углеводородов могут проявляться в побочных реакциях и вторичных превращениях продуктов. Так, например, способность к закоксовыванию катализатора у бутадиена значительно больше, чем у бутана или бутилена. Для уменьшения коксообразования процесс дегидрирования n-бутилена в дивинил проводят в присутствии водяного пара, а пары воды отравляют алюмохромовые катализаторы. Поэтому для дегидрирования n-бутилеиов применяют не алюмохромовый, а другие катализаторы, стойкие по отношению к воде, например железохромокалиевый.
Разумеется, могут иметь значение и другие факторы, например соотношение
скоростей отдельных элементарных стадий. Так, если лимитирующей стадией
дегидрирования менее реакционно-способного из двух сравниваемых углеводородов
является химическое превращение, то на скорость реакции дегидрирования более
реакционно-способного углеводорода на том же катализаторе будут, возможно,
оказывать влияние и такие факторы, как скорость адсорбции или внутренней
диффузии. Поэтому для обоих углеводородов оптимальные катализаторы должны быть
разными [2].
3.2 Современные представления о природе активной поверхности катализаторов дегидрирования
Оксиды хрома и некоторые другие оксидные катализаторы.
По современным представлениям, адсорбированный углеводород на оксидах металлов присоединяется к ионам металла, а не кислорода. Образование связи между адсорбированным углеводородом и ионом переходного металла происходит за счет незаполненных d-уровней металла или путем образования s-d-связи.
Некоторые авторы установили корреляцию между количеством Сr6+, содержащейся в алюмохромовом катализаторе, и его дегидрирующей активностью, и в связи с этим высказали предположение, что носителем каталитической активности является содержащийся в катализаторе шестивалентный хром.
Это предположение, однако, недостаточно обосновано, так как в условиях реакции восстановление Сr6+ и других возможных соединений с валентным состоянием хрома выше трех происходит быстро, а активность алюмохромового катализатора сохраняется продолжительное время. При регенерации алюмохромового катализатора в токе СO2 высшие оксиды хрома не образуются, а вместе с тем такие катализаторы не менее активны, чем регенерированные воздухом.
Ван-Рейн из измерений магнитных моментов и сигналов ЭПР алюмохромовых
катализаторов, подвергавшихся различной окислительно-восстановительной
обработке, сделали вывод, что высшие оксиды хрома восстанавливаются в токе
сухого водорода, т.е. в условиях, благоприятствующих получению активного
алюмохромового катализатора, не только до трех-, но и до двухвалентного хрома
[2]. Соотношение между 2- и 3-валентными оксидами хрома определяется
равновесием:
![]()
Дальнейшие экспериментальные подтверждения образования двухвалентного хрома при восстановлении алюмохромовых катализаторов были получены Рубинштейном [2]. Так, при обработке тщательно восстановленных алюмохромовых катализаторов водой наблюдается выделение водорода. При обработке Н2O катализатора, восстановленного дейтерием, в газе обнаружен только протий. Это значит, что водород образуется при разложении воды ионами Сr2+, обладающими восстановительными свойствами, а не выделяется в результате десорбционного вытеснения водой.
Особенно активной катионной структурой в реакциях с участием водорода на полупроводниках является d3. Такую электронную конфигурацию имеет ион хрома в Сr2O3. Согласно Казанскому и Швецу, активными центрами дегидрирования являются координационно ненасыщенные ионы Сr+.
В образцах, содержащих адсорбированную воду, все ионы Сr+ находятся в октаэдрической конфигурации. При отщеплении одной молекулы воды координация понижается до квадратной пирамиды:
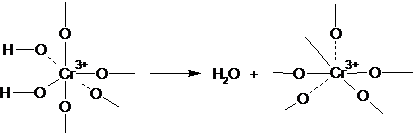
а отщепление следующих молекул воды может приводить к дальнейшему понижению координации. Для выяснения, являются ли присутствующие на поверхности катализаторов, десорбировавших воду при высокой температуре, координационно ненасыщенные ионы Сr3+ активными центрами дегидрирования, необходимы дальнейшие исследования.
Крылова, Козуненко и Кобозев [2] наблюдали максимум содержания стирола в катализаторе дегидрирования этилбензола и парамагнитной восприимчивости при содержании хрома в катализаторе ≈ 2%. Максимум удельной восприимчивости при небольшом содержании хрома связан, по-видимому, с образованием δ-фазы Сr2O3. Что касается активности катализатора, то следует иметь в виду, что оксид хрома достаточно активна сама по себе, и смешанная алюмохромовая структура, если бы она играла существенную роль в катализе, должна была бы быть весьма активной.
Однако испытанные в работе образцы были мало активнымии, повидимому, обладали значительной кислотностью. Поэтому наблюдавшееся при увеличении содержания хрома свыше 2% снижение выходов стирола могло быть связано с образованием побочных продуктов. Действительно, при дегидрировании менее реакционно-способных углеводородов - парафинов - не наблюдалось максимума активности при столь небольших добавках хрома, как 2%.
Буянов связывает активность железохромовоцинковых катализаторов в реакции дегидрирования бутиленов с присутствием в нем хромовой шпинели. Однако значительной дегидрирующей активностью обладают оксид железа или оксид цинка, не содержащие хрома, не говоря уже о самой оксида хрома. Поэтому в железохромоцинковых катализаторах активными центрами могут быть, ионы любого металла, входящего в состав катализатора. Образование же твердых растворов и смешанных структур скорее способствует стабильности катализатора, препятствуя рекристаллизации и нежелательным химическим превращениям катализатора, что может быть особенно важно при дегидрировании бутилена и других олефинов ввиду жесткости условий эксплуатации этих катализаторов.
Имеющиеся данные не дают также оснований полагать, что дегидрирующая способность хромовомагниевых или хромосиликагелевых катализаторов обусловлена образованием активных смешанных структур. Остается неясной природа активирующего действия малых количеств воды. Полностью обезвоженные катализаторы дегидрирования неактивны. При увеличении содержания воды в сырье активность алюмохромовых катализаторов проходит через максимум.
Можно
предположить, что вода входит в состав активных центров катализатора, оказывая
промотирующее действие. Обратимое отравление алюмохромового катализатора более
значительными ее количествами может быть объяснено блокированием активных
центров [2].
3.3 Процесс дегидрирования
Отщепление водорода от алканов (дегидрирование) является обратимым высокотемпературным каталитическим процессом и используется главным образом в промышленности. Ввиду сложности протекания гетерогенных каталитических реакций будут рассмотрены только некоторые общие закономерности.
В качестве катализаторов дегидрирования применяют оксиды металлов (Сr2Оэ, Fe2O3, ZnO и др.), а также металлы (Pt, Pd, Ni, Fe); при катализе оксидами температура процесса 450-650 °С, при катализе металлами - около 300 оС.
Низшие алканы (С2-С4) при дегидрировании превращаются в алкены, а из
бутана, в зависимости от применяемого катализатора и условий реакции, может
получаться и бутадиен-1,3:
 Алканы,
содержащие пять атомов углерода в цепи (но не более), подвергаются
дегидроциклизации с образованием циклопентанового углеводорода:
Алканы,
содержащие пять атомов углерода в цепи (но не более), подвергаются
дегидроциклизации с образованием циклопентанового углеводорода:
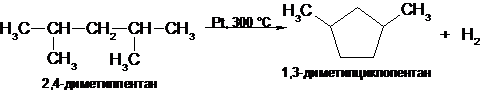
Если
в цепи алкана содержится шесть и более атомов углерода, то образующийся в
подобных условиях циклогексан (или его гомологи) подвергается дальнейшему
дегидрированию с образованием энергетически выгодного ароматического кольца:
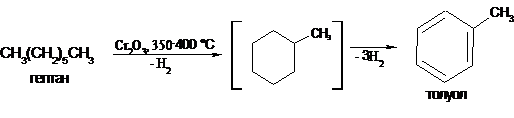
Дегидрирование алканов - реакция, обратная гидрированию ненасыщенных углеводородов. Положение равновесия определяется температурой и давлением. Обычно дегидрирование проводят при более высоких температурах, а гидрирование - при сравнительно низких (до 200 °С), согласно принципу Лe Шателье.
Принцип Ле Шателье-Брауна (1884 <http://ru.wikipedia.org/wiki/1884>) - если на систему, находящуюся в устойчивом равновесии, воздействовать извне, изменяя какое-либо из условий равновесия (температура <http://ru.wikipedia.org/wiki/%D0%A2%D0%B5%D0%BC%D0%BF%D0%B5%D1%80%D0%B0%D1%82%D1%83%D1%80%D0%B0>, давление <http://ru.wikipedia.org/wiki/%D0%94%D0%B0%D0%B2%D0%BB%D0%B5%D0%BD%D0%B8%D0%B5>, концентрация <http://ru.wikipedia.org/wiki/%D0%9A%D0%BE%D0%BD%D1%86%D0%B5%D0%BD%D1%82%D1%80%D0%B0%D1%86%D0%B8%D1%8F>, внешнее электромагнитное поле <http://ru.wikipedia.org/wiki/%D0%AD%D0%BB%D0%B5%D0%BA%D1%82%D1%80%D0%BE%D0%BC%D0%B0%D0%B3%D0%BD%D0%B8%D1%82%D0%BD%D0%BE%D0%B5_%D0%BF%D0%BE%D0%BB%D0%B5>), то в системе усиливаются процессы, направленные на компенсацию внешнего воздействия.
Анри Ле Шателье <http://ru.wikipedia.org/wiki/%D0%9B%D0%B5_%D0%A8%D0%B0%D1%82%D0%B5%D0%BB%D1%8C%D0%B5,_%D0%90%D0%BD%D1%80%D0%B8_%D0%9B%D1%83%D0%B8> (Франция <http://ru.wikipedia.org/wiki/%D0%A4%D1%80%D0%B0%D0%BD%D1%86%D0%B8%D1%8F>) сформулировал этот термодинамический принцип подвижного равновесия, позже обобщённый Карлом Брауном <http://ru.wikipedia.org/wiki/%D0%91%D1%80%D0%B0%D1%83%D0%BD,_%D0%9A%D0%B0%D1%80%D0%BB_%D0%A4%D0%B5%D1%80%D0%B4%D0%B8%D0%BD%D0%B0%D0%BD%D0%B4>.
Принцип устойчивости применим к равновесию любой природы: механическому, тепловому, химическому, электрическому (эффект Ленца <http://ru.wikipedia.org/wiki/%D0%9F%D1%80%D0%B0%D0%B2%D0%B8%D0%BB%D0%BE_%D0%9B%D0%B5%D0%BD%D1%86%D0%B0>, явление Пельтье <http://ru.wikipedia.org/wiki/%D0%AD%D1%84%D1%84%D0%B5%D0%BA%D1%82_%D0%9F%D0%B5%D0%BB%D1%8C%D1%82%D1%8C%D0%B5>) [3].
Дегидрированию благоприятствует пониженное давление; на практике используют давление 1-10атм (1атм = 101,3 кПа.), а иногда - ниже атмосферного. Кроме того, для каждого соединения существует довольно узкий диапазон температур, в котором протекает прямой или обратный процесс [6,7,8].
Заключение
Роль катализаторов в химическом производстве исключительно велика. Получение серной кислоты, синтез аммиака, получение из твердого угля жидкого топлива, переработка нефти и природного газа, получение искусственного каучука, пластмасс, гидрогенизация жиров - вот далеко не полный перечень важнейших производств, где применяются катализаторы. Очевидно, поиски новых, все более совершенных катализаторов будут способствовать повышению производительности труда и снижению себе стоимости продукции.
Особую роль играют биологические катализаторы - ферменты. При их участии протекают сложные химические процессы в растительных и животных организмах [9].
Для катализаторов гидрирования наибольшее внимание уделено нанесенным Ni-катализаторам, в последнее время все шире применяющимся не только в крупнотоннажных процессах, но и в тонком органическом синтезе. Обсуждены катализаторы на основе благородных металлов (Pt, Pd, Ru, Rh, Ir), нанесенные сульфидные катализаторы гидроочистки и принципиально новые катализаторы гидрирования, такие как карбиды металлов, исследование которых быстро развивается в последние годы. Приведены некоторые примеры использования приемов механохимии для приготовления катализаторов, а также контактов, обеспечивающих получение экологически чистых моторных топлив.
В настоящее время наибольшее распространение имеют катализаторы,
приведённые в таблице 3.
Таблица 3
Наиболее распространённые процессы и соответствующие катализаторы
|
Процесс |
Катализатор |
|
Гидрирование олефинов |
Нанесенные Ni, Сu, Pt, Pd, Ru, Rh |
|
Гидрирование ацетиленовых Углеводородов |
Нанесенные Ni, Pd, Ni - Pd,Со - Pd, Сu - Pd |
|
Гидрирование ароматических Углеводородов |
Нанесенные Ni, Pd, Rh, Pt, Со - Мо, скелетный Ni |
|
Гидрооблагораживание моторных топлив |
Ni, Ni - Мо, Со - Мо на АI2О3 икзельгуре |
|
Гидрирование карбонильных соединений |
Скелетные и нанесенные Ni и Со, нанесенные Pd, Rh и Pt, Сu - Сr - О, Сu на кизельгуре |
|
Гидроочистка (гидродесульфуризация) |
Ni - Мо, Ni - W, Со - Мо, Со - W, Ru на АI2O3 и углероде, карбиды Мо и W |
|
Гидрирование нитрилов |
Нанесенные Ni, Pd, Pt |
|
Гидрирование СО и СО2(метанирование) |
Нанесенные Ni, Си, Со, Fe, Pt, Rh, сетки Pt, карбиды Мо и W |