Материал: Процессы гидрирования и дегидрирования органических соединений
2.2 Современные тенденции в разработке и использовании новых кат
ализаторов гидрирования
В 1980-х годах была проведена серия исследований, направленных на создание никелевых катализаторов гидрирования на носителях, не уступающих по активности и другим параметрам скелетным катализаторам. Такими свойствами обладает, например, катализатор Еurо-Ni-1 (состава 25% Ni/SiO2), разработанный большой группой исследователей из разных стран во главе с Кененом. Этот катализатор готовят методом гомогенного осаждения, при котором часть никеля образует на носителе гидросиликат. Гомогенное осаждение Ni ведут в присутствии мочевины на суспендированном в водной среде микросферическом силикагеле, который получают пиролизом SiCI4 в пламени. В присутствии SiО2 рН водного раствора соли никеля Ni(NО3)2. 6Н2О не превышает 5,3-5,5, тогда как в его отсутствие при осаждении гидроксида никеля значение рН достигает 5,8 и остается постоянным.
На сильное взаимодействие Ni и SiО2 в процессе приготовления катализатора указывает трудность восстановления последнего, особенно по сравнению с ненанесенным гидроксидом никеля. Для полного восстановления катализатора Еurо-Ni-1 требуются температуры выше 400 °С, вплоть до 600 °С.
При нанесении Ni на SiО2 развитие поверхности может происходить за счет образования промежуточного гидросиликата никеля. Однако это зависит от условий приготовления, соотношения Ni : SiО2 и реакционной способности SiО2. Наряду с Euro-Ni-1 в последние годы с помощью новых технологий были приготовлены катализаторы Ni/SiO2 с меньшим содержанием металла (10-15%) для гидрирования ацетона.
Предприняты и другие попытки увеличить удельную поверхность Ni на носителе при уменьшении его содержания до 4-10%. Для этого использовали как метод пропитки, так и металлоорганические комплексы, модифицирующие поверхность носителей SiО2 и Аl2О3, в органических растворителях.
Большой интерес в 1980-х годах в России вызвали так называемые «сорбционные» катализаторы. Метод их получения, заключающийся в связывании металлоорганических комплексов поверхностью носителя, достаточно сложен и дорог.
Для гидроочистки прямогонных бензинов применяют в основном соосажденные Al-Co-Мо-катализаторы, способные удалять серу. Гидрирование ароматических углеводородов осуществляется на них лишь частично. Такие катализаторы вообще недостаточно активны в реакциях гидрирования ароматических и ненасыщенных соединений. Для этой цели в некоторых случаях более пригодны Ni-W-Al- либо Ni-Мо-Al-катализаторы.
В последнее время большое внимание уделяют новым видам Со-Мо-, Ni-Мо- и Ni-W- катализаторов на носителях, а также катализаторам на основе благородных металлов.
Сероустойчивые катализаторы широко используют как в одно-, двухстадийных процессах гидрирования ароматических веществ. Установлено, что катализатор Ni-W/Аl2О3 отравляется серой более интенсивно, чем Ni-Мо/Аl2О3. Поэтому двухступенчатый процесс гидроочистки организуют таким образом, что на первой ступени (в основном, гидрирование сернистых соединений) применяют Ni-Мо-, а на второй ступени («догидрирование») - низкопроцентный Ni-W-катализатор (например: 6%Ni + 20% WОз/Аl2Оз).
С конца 1980-х годов разработкой новых Ni-W- катализаторов на носителях занимается ряд фирм, ориентированных на гидроочистку моторных топлив. Недостатком предложенных катализаторов является значительное содержание в них WО3; кроме того, для осуществления на этих катализаторах эффективной гидроочистки требуется применение высоких давлений (до 10 МПа) и температур (до 360 °С).
Таким образом, в настоящее время наиболее привлекательными и дешевыми
катализаторами гидрирования ненасыщенных углеводородов (включая ароматические
соединения) являются модифицированные оксидами вольфрама или молибдена
никельсодержащие катализаторы на носителях [1].
2.3 Катализаторы на основе благородных металлов
Никельсодержащие катализаторы дешевле катализаторов на основе благородных металлов (Pt, Pd, Ru, Rh, Ir, Os). Однако в целом ряде промышленных процессов гидрирования предпочтение отдается последним. Это обусловлено их высокой каталитической активностью, позволяющей использовать более низкие температуры и давления. Срок жизни таких катализаторов нередко исчисляется годами. Особенно большой интерес вызывают Pd-, Pt-, Ru- и Rh- катализаторы на носителях и биметаллические системы. Применение специальных носителей позволило снизить содержание благородного металла до 0,01-0,005% и тем самым удешевить катализатор, сохранив его качество.
Применение современных физико-химических методов исследования дает возможность изучать механизм действия этих катализаторов, оптимизировать их состав, используя различные носители и модификаторы, разрабатывать способы регулирования дисперсности металла на поверхности носителя. Некоторые катализаторы на основе благородных металлов устойчивы к отравлению S- и N- содержащими соединениями.
Гидрирование ненасыщенных углеводородов.
В некоторых случаях в качестве катализаторов гидрооблагораживания моторных топлив (деароматизации, гидрирования олефинов) предпочитают применять благородные металлы, а не никель. Катализаторы на основе благородных металлов более активны и меньше отравляются сернистыми соединениями. Платина и палладий, нанесенные на Аl2O3, легко дезактивируются при концентрации серы менее 1·10-4%, однако их устойчивость к сере растет при использовании таких кислотных носителей, как цеолиты. В частности, на Pd/LaY даже при давлении H2S 63 кПа, т.е. в условиях, при которых весь палладий должен был бы превратиться в PdS, 98% продуктов гидрокрекинга додекана составляют алканы, а активность и селективность катализатора сохраняются неизменными. Столь необычное поведение благородного металла объясняют эффектом SMSI или изменением электронного состояния палладия при взаимодействии с кислотными центрами цеолита.
Платиновые катализаторы получают ионным обменом или пропиткой носителя раствором соли Pt(NH3)4CI; последняя связывается с кислотным центром цеолита ≡Аl-O-. Далее следует важная стадия образования центров 2(≡Аl-O-)Pt2+, которые формируются при прокаливании на воздухе с последующим восстановлением водородом. При этом платина входит в состав кластеров типа m(≡Аl-O-H)••• Ptn. Кластеры находятся в тесном контакте с сильными кислотными центрами, что делает возможным переход электронов от благородного металла и приводит к формированию электронодефицитных частиц металла (Ptδ+), определяющих особые свойства катализатора.
Чаще всего для гидрирования применяют палладиевые катализаторы на носителях. В табл. 1 приведены результаты исследования реакций гидрирования СO, альдегидов и ненасыщенных углеводородов на катализаторах Pd/TiO2, полученных различными способами и отличающихся размерами частиц и величиной активной поверхности металла.
Как видно из табл. 1, скорости гидрирования СO и низкотемпературного гидрирования пропионового альдегида в спирт возрастают с увеличением дисперсности Pd. Однако при гидрировании двойных связей C=C в этилене, бутадиене и акролеине наблюдается обратный порядок изменения активности, что особенно заметно в реакции гидрирования сопряженных связей бутадиена.
Средняя активность (число оборотов катализаторов в секунду) различных катализаторов Pt/TiO2 в реакциях гидрирования CO, альдегидов и олефинов
|
Характеристики катализатора |
Средняя активность катализатора при гидрировании |
||||||||
|
[Pd], % |
Sуд, м2 r -1 |
D, Нм |
H : Pd |
CO (метании-рование) |
CO в CH3OH (230 ºС) |
связи C=O в Пропионо-вомальде-гиде (80 ºС) |
C2H4 (80 ºС) |
связи C=C в акролеине (80 ºС) |
C4H6 (80 ºС) |
|
5,5 |
207 |
4,5-6,5 |
0,32-0,67 |
7,3·10 -4 |
4,3·10 -4 |
0,16 |
380 |
0,09 |
150 |
|
5,2 |
9 |
186 |
0,17 |
2,8·10 -4 |
4,0·10 -5 |
4,5·10 -3 |
500 |
- |
680 |
|
4,4 |
9 |
295 |
0,067 |
5,5·10 -4 |
0 |
4,5·10 -3 |
580 |
0,4 |
1,05·10 -3 |
Связь между каталитическими свойствами нанесенного палладия и его дисперсностью активно обсуждается в литературе. В одних работах это явление объясняют изменением электронного состояния Pd в результате SMSI, в других - участием в реакции не только металла, но и носителя. Представленные в табл. 1 три Pd-катализатора на одном и том же носителе (TiO2) проявляют различную активность и селективность. Поэтому причину различий следует искать в свойствах частиц самого палладия: в изменении их размеров, формы, электронной структуры и характера взаимодействия с гидрируемыми молекулами [1].
.4 Процесс гидрирования
Реакцию гидрирования ненасыщенных соединений водородом можно
рассматривать как реакцию восстановления. При этом атомы углерода кратной связи
восстанавливаются, а молекулярный водород окисляется. Присоединение водорода к
алкенам происходит только в присутствии катализаторов:
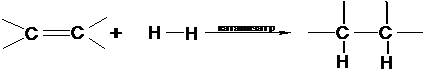
В качестве катализаторов применяют тонкоизмельченные металлы - платину, палладий, никель. Наиболее часто используются никель Ренея и катализатор Адамса. Никель Ренея получают обработкой никель-алюминиевого сплава гидроксидом натрия, в результате чего получают тонко измельченный никель, насыщенный водородом. Катализатор Адамса - это платиновая чернь, получаемая восстановлением оксида платины(IV) водородом непосредственно в процессе реакции. Палладий для увеличения поверхности наносят на инертный материал - уголь. Все эти катализаторы не растворяются в органических растворителях.
Водород
и алкен адсорбируются на большой поверхности тонкоизмельченного металла, где и
происходит реакция. Оба атома водород присоединяются с одной стороны π-связи, т.е. процесс идет как син-присоединение:

Молекула
ненасыщенного соединения может содержать другие функциональные группы,
способные к восстановлению. Во многих случаях удается подобрать условия, при
которых происходит селективное восстановление двойной связи. В приведенных ниже
примерах восстановление не затрагивает бензольное кольцо и карбонильную группу:
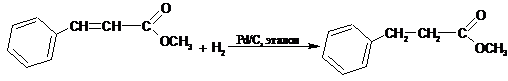
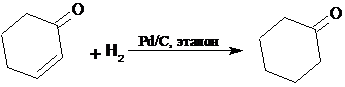
Гидрирование является экзотермической реакцией. Значения теплот гидрирования дают ценную информацию об относительной устойчивости ненасыщенных соединений. На основании этих данных было установлено, что чем более замещенным является алкен, тем он термодинамически стабильнее [7,8].
3. Процесс дегидрирования органических веществ
Дегидрирование или дегидрогенизация - это химическая реакция отщепления водорода от молекул органических соединений; одна из фаз процесса биологического окисления. Осуществляется в присутствие катализаторов или под действием акцепторов водорода. Каталитическое дегидрогенизация и обратная реакция - гидрирование - связаны подвижным термодинамическим равновесием. Протеканию дегидрогенизация способствует повышение температуры и понижение давления. Осуществляют дегидрогенизация обычно при температуре > 300 °С и давлении 0,1-5 МПа; при необходимости применение более высоких давлений сочетают с соответствующим повышением температуры. Катализаторы дегидрогенизации - обычно многокомпонентные системы, содержащие переходные металлы, их оксиды или сульфиды. При дегидрогенизации молекула реагирующего соединений образует комплекс с катализатором, распадающийся затем на Н2 и продукт, десорбируемые с поверхности катализатора [3,5].
Дегидрогенизация парафинов в ароматических соединениях
(дегидроциклизация) - одна из стадий каталитического риформинга; осуществляется
на оксиднохромовом катализаторе при 330-400 °С, давление 0,2-0,8 МПа.
Каталитическая дегидрогенизации используют в промышленности для получения
1,3-бутадиена, изопрена, стирола и др. В СССР в 1984 путем дегидрогенизация
было получено более 2 млн. бутадиена и около 11 млн. стирола. К каталитической
дегидрогенизации относят также так называемая окислительная дегидрогенизации,
протекающее в газовой фазе под действием окислителей (например: О2, SO2, H2O2,
I2, Вr2 и др.). Реакция практически необратима, что способствует увеличению
выхода целевых продуктов. Так, метанол в присутствии серебра (Ag) окисляется О2
воздуха при ≈ 400 °С в формальдегид с выходом около 80%. Окислительное
дегидрогенизация олефинов и алкилбензолов осуществляют в присутствие фосфатов
алюминия, молибдатов висмута, цеолитoв, активированного угля и др.
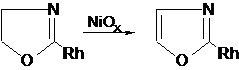
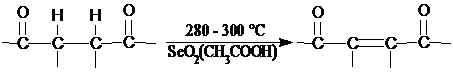
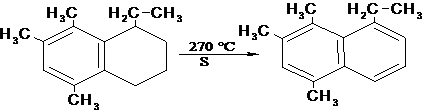
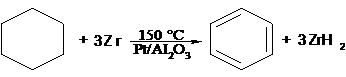
В
качестве акцепторов водорода при дегидрогенизация используют обычно
2,3-дициано-1,4-бензохинон, пероксиды Ni, SeO2, Se, S, а также металлы,
способные образовывать гидриды (Zr, Ti, интерметаллиды и др.). Выше указаны
некоторые примеры [5].
3.1 Разновидности дегидрирующего действия катализаторов
Катализаторы дегидрирования весьма многочисленны и разнообразны по своему химическому составу. Так, еще по сводке из книги Платэ количество элементов, упоминаемых в качестве активных компонентов катализаторов ароматизации парафинов, составляло 51 и включало элементы почти всех групп периодической системы, а главным образом IV-VI групп. Число известных катализаторов и способов их приготовления непрерывно пополняется.
Один и тот же катализатор, если он достаточно активен, способен к дегидрированию углеводородов различных гомологических рядов и строения. Так, на алюмохромокалиевых катализаторах были получены достаточно высокие выходы продуктов дегидрирования низших n-парафинов С3-С5 и ароматизации n-парафинов С6-С7, циклогексана, дегидрирования этилбензола, олефинов, разветвленных парафинов, пятичленных нафтенов, алкилгидроароматических и других углеводородов.
Недегидрирующие побочные и вторичные реакции.
Как правило, не наблюдается параллелизма между дегидрирующей активностью катализаторов и активностью их в реакциях крекинга и изомеризации. Это говорит о том, что реакции изомеризации и крекинга обусловлены не теми активными центрами, которые ответственны за дегидрирование.
Изомеризация углеводородов на дегидрирующем катализаторе может не только быть побочной реакцией, но и в некоторых случаях является важной стадией процессов дегидрирования. Так, ароматизация парафинов с длиной цепи не более пяти атомов углерода обязательно включает стадию изомеризации.
При отравлении алюмохромового катализатора пиридином или хинолином уменьшается не только изомеризующая активность, но и выходы «ненормальных» продуктов дегидроциклизации n-октана (т- и р-ксилолов), которые образуются через стадию изомеризации n-октана в изооктан или через промежуточные циклические соединения.
С другой стороны, в условиях риформинга (давление водорода, «бифункциональные»
катализаторы) дегидрирование может быть одной из стадий изомеризации
углеводорода. Так, при контактировании n-гептана с алюмосиликатом или платиной, нанесенной на Аl2O3, изогептаны не образуются; в присутствии же смеси этих
контактов выход изогептанов равен 24%. При этом образуется также толуол.
Изомеризация протекает через промежуточные стадии дегидрирования -
гидрирования:

Дегидрирование углеводородов, содержащих и не содержащих двойную связь.