Материал: Процесс выплавки стали в дуговых печах
Процесс выплавки стали в дуговых печах
РАСЧЕТНО-ПОЯСНИТЕЛЬНАЯ ЗАПИСКА
К КУРСОВОЙ РАБОТЕ
по курсу «Электротехнологические процессы»
на тему:
Процесс выплавки стали в дуговых печах
1. Задание для расчёта
Таблица 1
Химический состав выплавляемой стали и элементов шихты
|
Предназначение |
Марка |
Содержание, % |
|||||||
|
|
|
С |
Si |
Mn |
S |
P |
Cr |
Ni |
Ti |
|
Выплавляемая сталь |
1Х18Н9Т |
≤0,12 |
≤0,8 |
1,00-2,00 |
не более |
17,0-19,0 |
8,0-9,5 |
0.7 |
|
|
|
|
|
|
|
≤0.020 |
≤0.035 |
|
|
|
|
Шихта |
50Х |
0.46-0.54 |
0.17-0.37 |
0.5-0.8 |
0.035 |
0.035 |
0.8-1.1 |
≤0.3 |
___ |
|
|
1Х13 |
0.09-0.15 |
≤0.60 |
≤0.60 |
≤0.025 |
≤0.030 |
12.0-14.0 |
≤0.60 |
___ |
Ёмкость печи 25 тонн, количество печей - 3.
2. Введение
Применение электрической энергии в качестве источника тепла вместо энергии сжигаемого топлива, обусловливающее возможность получения при этом высокой температуры, определяет теплотехнические, конструктивные и производственно-технические преимущества электропечей.
При использовании электрического тока представляется возможность вести концентрированный нагрев. В этом случае исключаются потери, связанные с передачей тепла от топлива, сгорающего в закрытом пространстве, отпадают затраты энергии на нагрев топлива до температуры сгорания, снижаются потери с отходящими газами.
Нагревание электрическим током позволяет легче осуществлять быстрый подъем температуры, точнее регулировать нагрев. То обстоятельство, что при электронагреве тепло выделяется в самом нагреваемом теле или в непосредственно соприкасающейся с ним среде, позволяет вести процессы нагрева в различной атмосфере, при любом давлении.
Новая техника XX в. - техника высоких давлений и температур, больших скоростей и сильных химических воздействий - потребовала новых материалов для машин, аппаратов и других металлических изделий. Такими материалами и явились высококачественные и специальные стали и сплавы.
Высококачественной называется сталь с низким содержанием серы, фосфора, кислорода и других вредных или нежелательных примесей, обладающая высокими механическими и физическими свойствами.
Особое место среди высококачественных сталей занимают специальные легированные стали, которые содержат легирующие элементы (хром, никель, вольфрам, марганец, кремний, молибден, ванадий, титан, кобальт, цирконий, бор и др.) и благодаря этому обладают особыми свойствами.
Электрическая печь имеет ряд существенных преимуществ перед другими сталеплавильными агрегатами, поэтому высоколегированные инструментальные стали, нержавеющие, жаростойкие и жаропрочные, а также многие конструкционные стали выплавляют только в электрических печах.
В электропечи можно получать сталь с низким содержанием серы и фосфора, можно полнее раскислить металл, обеспечив низкое содержание в стали неметаллических включений. В электропечи значительно меньше потери легирующих элементов, вводимых в виде ферросплавов, значительно выше использование ценных составляющих, вносимых отходами легированных сталей. В электропечи легко осуществить быстрый подъем и точное регулирование температуры металлической ванны в узких пределах. В ней можно проводить все металлургические процессы, создавая окислительную, восстановительную или нейтральную атмосферу, можно выплавлять сталь любого состава.
Развитие производства стали
требовало одновременного роста производства ферросплавов. Специальные добавки
(марганец, хром, кремний, вольфрам и др.) вводят в сталь для легирования и
раскисления в виде сплавов с железом, называемых ферросплавами. Объясняется это
тем, что производство чистого марганца, кремния или хрома сопряжено с большими
затратами и трудностями; получать же ферромарганец, ферросилиций, феррохром и
другие сплавы с железом проще и дешевле.
3. Общие
характеристики и расчёт
3.1 Свойства и виды
термообработки заданной марки металла
Свойства элементов входящие в сталь:
1. Основные свойства железа. Железо является главным элементом, составляющим основу металлической фазы в процессе плавки и готовой стали. Содержание железа в металлической фазе по ходу плавки обычно повышается, но относительно незначительно - менее чем на 10%, тогда как содержание других примесей изменяется в несколько раз. Переход железа из металлической фазы в другие связан с рядом его физических и химических свойств. Физико-химические свойства железа определяют основные параметры процессов плавки стали температурный режим, режим окислительного рафинирования и т. д., поэтому в общей физико-химической характеристике сталеплавильных процессов важное место занимают данные о свойствах железа и его поведении во время плавки.
Основные физические свойства железа. Температура плавления химически чистого железа составляет 1539°С. Техническое железо, полученное окислительным рафинированием и имеющее высокое содержание кислорода, плавится примерно при 1530°С. Температура плавления стали всегда ниже, чем железа, и зависит от содержания примесей. Металлы (Mn, Cr, Ni, Co, Мо, V и др.) незначительно снижают температуру плавления железа: на 1-3°С при введении 1%, а металлоиды (С, О, S, Р и др.) на 30-80 °С. В процессе плавки температура плавления металла изменяется главным образом в результате изменения содержания углерода. В целом температура плавления металла в начале плавки минимальна, обычно незначительно превышает температуры плавления чугуна (1120-1150°С), а в конце плавки максимальна и при низком содержании углерода составляет 1520-1525°С. Перегрев металла выше температуры плавления в начале плавки для нормального проведения процессов рафинирования необходим не менее 30-50 °С, а в конце плавки, чтобы обеспечить нормальное проведение процессов раскисления-легирования и разливки, этот перегрев обычно требуется в пределах 70-150 °С. В связи с этим температура нагрева металла уже в начале плавки должна быть не менее 1350-1400 °С, а в конце до 1600-1650 °С, иногда и выше.
Теплота плавления железа, по данным В. И. Явойского, 15200 Дж/моль, или 271,7 кДж/кг. Температура кипения железа составляет 2735 °С, а теплота испарения его ~ 352,5 кДж/моль, или 6300 кДж/кг.
Вязкость (динамическая) жидкого железа обычно колеблется в пределах 0,01-0,05 Па×с и зависит от температуры и содержания примесей. Чем выше температура, тем меньше вязкость.
Плотность жидкого железа при 1550-1650 °С равна 6,7-6,8 г/см3, при температуре кристаллизации ~ 6,85 г/см3, плотность твердого железа при температуре кристаллизации ~ 7,45 г/см3 (усадка при кристаллизации ~ 8,7%), при комнатной ~ 7,8 г/смэ (общая усадка 14%). Из обычных примесей наибольшее влияние на плотность железа оказывают углерод и кремний, снижая ее, поэтому обычный жидкий чугун имеет плотность 6,2-6,4 г/см3, твердый при комнатной температуре 7,0-7,2 г/см3. Плотность жидкой и твердой стали, занимающей промежуточное положение между железом и чугуном, соответственно 6,5-6,6 и 7,5- 7,6 г/см3.
Теплоемкость и энтальпия. Удельная теплоемкость жидкой металлической фазы практически не зависит от температуры и составляет для чугуна 0,88 кДж/(кг×К) и металла конца окислительного рафинирования 0,84 кДж/(кг×К). А для твердых материалов она зависит от температуры, но в приближенных расчетах можно принимать средние значения, равные для чугуна 0,745 кДж/(кг×К) и стали 0,7 кДж/(кг×К).
На 1 т выплавляемой стали обычно выход шлака составляет 100-150 кг, газов 50-100 кг, поэтому расход тепла на нагрев всех трех продуктов плавки (металла, шлака и газов) обычно изменяется в пределах 1700-1900 МДж/т. Кроме того, дополнительно расходуется тепло на разложение загружаемых в ванну оксидов железа и карбонатов, а также на компенсацию неизбежных тепловых потерь.
Поверхностное натяжение (на границе металл - газ) жидкой металлической фазы зависит от температуры и химического состава (содержания углерода и других поверхностно-активных примесей) и обычно колеблется в пределах 1000-1800 кДж/м2. Поверхностное натяжение железа максимально при ~ 1550°С, в области более низких и высоких температур оно снижается, что отличает железо от большинства металлов, для которых характерно снижение поверхностного натяжения при повышении температуры. С повышением содержания углерода и кислорода поверхностное натяжение снижается, особенно в области концентраций менее 0,3-0,5% [С] и 0,05-0,08% [О]. При более высоких содержаниях их влияние незначительно.
Растворяющая способность жидкого железа. Теоретически (термодинамически) жидкое железо в той или иной степени способно растворять все металлы и металлоиды, но растворимость некоторых элементов в железе настолько незначительна, что ею можно пренебречь. Такой пренебрежимо малой растворимостью в жидком железе обладают металлы, стоящие в начале каждого периода Периодической системы элементов Д. И. Менделеева, имеющие большие атомные радиусы и рыхлую электронную оболочку: щелочные металлы (Li, Na, К, Rb, Cs) и щелочноземельные металлы (Mg, Ca, Sr, Ba). Кроме того, практически нерастворимыми являются Ag, Cd, Bi. Другие металлы в жидком железе растворяются полностью (неограниченно) или частично (ограниченно). К числу металлов, имеющих неограниченную растворимость, относятся Mn, Ni, Co, Си, Al, Sb, Се (все редкоземельные элементы) и др. Ограниченную растворимость имеют металлы: Сг, V, Mo, W, Ti, Zr, Pb, Sn, Pt и др. Но при высоких температурах все металлы, кроме Рb и Sn, имеют неограниченную растворимость. Металлоиды имеют ограниченную растворимость в жидком железе и, как правило, образуют с железом химические соединения.
Основные химические свойства железа и его поведение в сталеплавильных процессах. Окисление и восстановление железа, как и любого другого элемента, образующего оксид, означает распределение его между металлической и шлаковой фазами. Но распределение железа отличается от распределения примесей, содержащихся в нем: в металлической фазе активность железа близка к единице, а примесей всегда значительно меньше, поэтому описание закономерностей окисления железа несколько проще. Железо образует три оксида: Fe2O3, Fe3O4 и FeO.
Оксид Fe3O4 не является самостоятельным (по валентным связям), а представляет собой соединение оксидов FeO и Fe2O3 и называется ферритом железа. В жидких шлаках, особенно в основных, образование ферритов других элементов более вероятно, чем ферритов железа, поэтому целесообразно рассмотреть существование только двух оксидов: FeO и Fe2O3, в которых железо двух- и трехвалентно.
Наличие шлаковой фазы, способной растворять оксиды железа, создает термодинамически благоприятные условия для окисления железа, так как переход оксидов в раствор повышает их устойчивость. Вследствие этого примеси металла, образующие оксиды, на поведение железа влияют следующим образом: 1) способствуя образованию шлаковой фазы, облегчают протекание процесса окисления железа и перехода его в шлак; 2) имея большее химическое сродство к кислороду, чем железо, препятствуют его окислению (поступающий в ванну кислород расходуется главным образом на окисление примесей). Это влияние примесей сказывается лишь до тех пор, пока не достигнуто равновесие реакций их окисления. Таким образом, примеси, содержащиеся в металле и образующие оксиды, более прочные, чем FeO, в период окисления защищают железо от окисления, но не предотвращают этого процесса, так как для формирования шлака расходуется некоторое количество оксидов железа.
Углерод обладает большей способностью защищать железо от окисления, чем другие примеси. Это объясняется следующим: 1) концентрация углерода в металле по ходу плавки выше равновесной и углерод непрерывно окисляется, забирая поступающий в ванну кислород; 2) в результате окисления углерода образуются газообразные оксиды, причем главный продукт реакции СО является хорошим восстановителем.
В реальной сталеплавильной ванне неизбежно присутствует некоторое количество шлаковой фазы, образующейся или только в результате окисления примесей металла и разрушения футеровки (кислые процессы), или еще дополнительно в результате участия флюсов (основные процессы). В связи с этим протекание процесса частичного окисления железа и переход его оксидов в шлак в период окислительного рафинирования неизбежны даже в условиях защитного действия (непрерывного окисления) углерода. Содержание оксидов железа в шлаке зависит от большого числа факторов, главными из которых являются окислительное действие газовой фазы и восстановительное действие примесей металлической фазы. В результате окислительного действия газовой фазы и восстановительного действия примесей металла по ходу плавки наблюдается обычно стабильное для каждого периода содержание оксидов железа в шлаке, которое неравновесно ни с газовой, ни с металлической фазами, но связано с содержанием углерода в металле.
В период окислительного рафинирования неизбежны окисление железа металлической фазы и переход его в шлак, а также восстановление оксидов железа, введенных в ванну. Эти реакции протекают до тех пор, пока не будет достигнуто стабильное содержание оксидов железа в шлаке, характерное для конкретных условий ведения плавки.
Температура ванны существенно влияет на содержание оксидов железа в шлаке лишь в области перегревов над температурой плавления металла менее 40-60°С; в области более высокого перегрева это влияние незначительно, если основность шлака оптимальна. В том и другом случае чем выше температура, тем ниже содержание оксидов железа в шлаке, если другие факторы остаются неизменными. В условиях низких температур начала плавки, когда шлак еще гетерогенный и неблагоприятны кинетические условия окисления примесей металла кислородом оксидов шлака, содержание оксидов железа высокое даже при значительных содержаниях. Вследствие восстановительного действия углерода металла железо в шлаке находится главным образом в виде низшего оксида FeO. Соотношение FeO и Fe2O3 в шлаке главным образом зависит от окислительного потенциала газовой фазы и основности шлака. Чем больше окислительный потенциал газовой фазы и основность шлака, тем больше содержание Fe2O3.
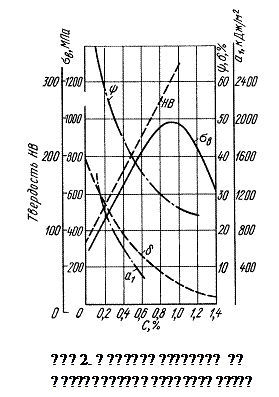
2. Углерод. Является важнейшей примесью
металла, играющей огромную положительную роль в процессах производства стали.
Этот элемент присутствует в сталях большинства марок. Расширяя область
температур устойчивого состояния γ-Fe
и улучшая свойства железа, углерод позволяет получать сталь с широким
диапазоном механических свойств. В сталях очень немногих марок специального
назначения (электротехнических, коррозионностойких, жаропрочных и т. п.)
углерод является нежелательной примесью. Углерод является главным потребителем
кислорода, подводимого в ванну для окисления примесей.
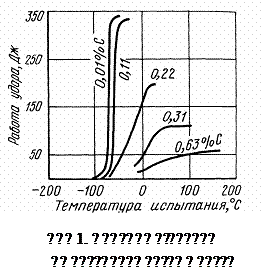
Перемешивание (кипение) ванны обусловлено выделением газообразных продуктов реакции окисления углерода. При окислении углерода образуются СО и СО2, объем которых в тысячи раз превышает объем металла. Выделение такого количества газа обеспечивает интенсивное перемешивание металла и шлака, облегчает массо- и теплопередачу, создавая условия для ускорения других физико-химических и физических процессов и форсирования плавки в целом. Пузыри СО, проходя через жидкий металл, также способствуют удалению из него газов и неметаллических включений в процессе плавки (особенно в подовых процессах) и во время вакуумирования.
Углерод имеет ограниченную растворимость в жидком железе, но она в несколько раз выше, чем даже в δ-Fe. Растворимость углерода при 1600°С [С]maх = 5,75%. Такое содержание может наблюдаться только тогда, когда углерод является единственной примесью железа. Присутствие других примесей изменяет растворимость углерода. Карбидообразующие примеси (Мn, Сr и др.) способствуют повышению [С]max, а примеси, образующие соединения с жидким железом (Si, Р и др.), уменьшают [С]max, поэтому в чугунах и ферросплавах содержание углерода различно, если даже в процессе их производства происходит насыщение металла углеродом (жидкий металл находится в постоянном контакте с твердым углеродом - коксом).