Материал: Приготовление нанесенных катализаторов и их химический анализ
В работе [38], в реакции конверсии метанола, как в присутствии водорода, так и в его отсутствии, максимальная активность была достигнута для системы содержащей 70 % CuO и 30 % ZnO.
Авторы полагают, что в данной системе имеет место синергетический эффект между компонентами, а именно: метанол активируется на металлической меди образуя формильную группировку, что является лимитирующей стадией, а оксид адсорбируется и предварительно активируется метанол, образуя также метокси - и гидрокс группы, которые находятся в динамическом равновесии с таковыми на металлической меди, таким образом повышая их концентрацию и увеличивая скорость реакции. Относительно инертный пористый оксид кремния, выключающий небольшие концентрации кальция проявляет каталитические свойства при разложении метанола с образованием формальдегида при температурах примерно 500˚С [39]. Авторы работ [40], также предложен катализатор для получения формальдегида на основе SiO2, для температурного диапазона 800-900˚С, что довольно сложно реализовать технически. Ими же предложено для получения производительности катализатора вести процесс в присутствии перекиси водорода. Авторы считают, что перекись водорода препятствует образованию кокса на поверхности катализатора. Таким образом, в реакции дегидрировании метанола можно ожидать синергетического эффекта при введении в состав катализатора данных компонентов.
Цель работы:
1. Приготовить катализаторы на основе соединений кремния, меди, цинка и калия и изучить влияние состава солевых систем на физико-химических свойства образцов, получаемых методом нанесения и осаждения компонентов.
. Изучить каталитические свойства
полученных модельных катализаторов в реакции дегидрирования метанола с целью
получения формальдегида.
2. Экспериментальная часть
2.1 Приготовление и анализ катализаторов
Приготовление осажденных катализаторов
В наших ранних работах обнаружено [41], что при соединении аммиачно-карбонатных растворов меди и цинка и силиката калия образуются осадки, которые после отделения, сушки и прокаливания идентифицированы методами рентгенографии. В настоящей работе варьировали соотношение между исходными растворами так, чтобы получить, возможно, более дисперсные оксидные и силикатные соединения меди и цинка.
В таблице 1 представлены результаты изменения концентрации
растворов от начала смешения компонентов до получения и отделения осадка (т.е.
маточника). Концентрация меди в растворе несколько уменьшается, но существенно
ниже по сравнению с концентрацией цинка, которая уменьшается почти на порядок.
Концентрация калия снижается в меньшей степени (примерно в 5 раз), а кремния
очень существенно (примерно в 30 раз), т.е. в осадке следует ожидать гидроксосиликатные
соединения цинка и калия с включением меди. Анализ катализатора, в общем,
подтверждает это положение. Пересчет состава прокаленной массы на оксиды
показывает, что их сумма превышает 100%. Это может быть обусловлено тем, что в
твердой фазе находятся также в виде гидрокарбонатов (например, КНSiO3),
где роль катиона выполняет ион Н+ малярная масса которого 1, а тогда
как у калия 39. Поэтому формальный пересчет состава на оскиды меди, цинка и
калия неправомерен. В частности, справочные данные по фазовому составу
гидросиликатов цинка и калия [42], указывают на существование именно
гидрокарбонатов калия и кремния (KHSi2O5). Соединения
цинка представлены гидротироанными гидрокарбонатами кремния (например, Zn4Si2O7
(OH) 2 (H2O). По нашим данным мольное соотношение
катионов и анионов (Cu+Zn+K) /Si <1и соотношение зарядов катионов к анионам,
также меньше единицы, что подтверждает данный тезис - в прокаленном осадке
присутствуют гидроксосиликатные соединения.
Таблица 1
Анализ при приготовлении осажденного катализатора (SU-27)
№
Анализируемые растворы и катализаторы
Концентрации компонентов, моль/л
Cu
Zn
K
Si
1
Исходный раствор МЦАКР (120 мл) К2SiO3
(180 мл)
0.100
0.490
1.200
0.600
2 0.040
0.196
0.720
0.360
3
Фильтрат после отделения осадка
0.035
0.026
0.120
0.014
4
Прокаленный катализатор (400°С) пересчет на
металлы пересчет на оксиды
Содержание компонентов, мас. %
1.57 1.96
25.44 31.66
10.34 12.96
33.00 70.70
Сумма оксидов 117.28 мас. %
5
Мольное соотношение компонентов в катализаторе
0.021
0.33
0.22
1.00
[ (Cu+K+Zn) /Si] мол. =0.571 ∑Zi+/∑
Zi--=0.46
В таблице 2 сведены результаты анализа осажденного
катализатора, где варьировали составы и соотношения исходных
аммиачно-карбонатных и силикатных растворов. Установлено, что принципиально
можно варьировать состав катализатора, хотя, разумеется, соотношения между
составов растворов и осадка нелинейное, и для каждого интервала концентрации
требуется детально экспериментальная проработка системы.
Удельная поверхность образцов определенная методом бэт дает
значение от 10 до 23 м2/г в интервале прокаливания образцов 400-600 ˚С,
при более высокой температуре пористая структура осажденного катализатора
существенно меняется, за счет агломерации частиц и спекания. Удельная
поверхность существенно уменьшается порядка до 2-3 м2/г.
Таблица 2
Условия приготовления и состав осажденных катализаторов
№
Наименование и тип катализатора
Условия приготовления
Химический состав катализатора, мас. %
Уд. Поверхность, м2/г
1
SU-15 СuO. ZnO. K2O. SiO2
Начальные концентрации: (Сu+Zn) =1.33моль/л K=0.66 моль/л Si=0.33 моль/л
Осаждение из раствора МЦАКР (100 мл). Состав:
Cu=1 моль/л, Zn=1 моль/л. раствором K2SiO3 (50 мл) Si=1
моль/л
Cu=12.6 Zn=44.8 K=1.2 Si=21.9
Не определяли
2
SU-22 СuO. ZnO. K2O. SiO2
Начальные концентрации: (Сu+Zn) =0.9 моль/л K=0.4 моль/л Si=0.2 моль/л
Осаждение из раствора МЦАКР (150 мл). Состав:
Cu=0.25 моль/л, Zn=0.94 моль/л. раствором K2SiO3 (50
мл) Si=0.81 моль/л
Cu=3.0 Zn=30.0 K=7.1 Si=13.0
15.1 12.1 (Tпр=600˚C)
3
SU-24 СuO. ZnO. K2O. SiO2
Начальные концентрации: (Сu+Zn) =0.3 моль/л K=1.2 моль/л Si=0.6 моль/л
Осаждение из раствора МЦАКР (100 мл). Состав:
Cu=0.25 моль/л, Zn=0.94 моль/л. раствором K2SiO3
(300мл) Si=0.81 моль/л
Cu=3.2 Zn=27.3 K=14.0 Si=18.3
23.3 12.7 (Tпр =600˚C)
4
SU-27 СuO. ZnO. K2O. SiO2
Начальные концентрации: (Сu+Zn) =0.24 моль/л K=0.65 моль/л Si=0.324 моль/л
Осаждение из раствора МЦАКР (120 мл). Состав:
Cu=0.10 моль/л, Zn=0.49 моль/л раствором K2SiO3 (180мл)
Si=0.54 моль/л
Cu=1.6 Zn=25.4 K=10.3 Si=33.0
18.0 2.3 (Tпр =600˚C)
Разложение осадка при термообработке методом термографии
которая представлена на рисунке 1. Потеря массы происходит на всем изученном
интервале температур от комнатной до 700˚С, что сопровождается выделением
в газовую фазу паров воды примерно с постоянной скоростью. Но в интервале
температуры примерно 140-220˚С имеет место, резкое падение уменьшения
массы образца с выделением в газовую фазу углекислоты, аммиака и воды, что
можно отнести к разложению аммиачно-карбонатного комплекса меди и цинка по
реакции:
(NH3) 4CO3. nH2O→ZnO
+ 4NH3+ CO2 +nH2O (1)
Данные рентгенографического анализа прокаленных образцов
представлены на рисунке 2. В зависимости от состава катализатора существенно
изменяется дисперсность оксидных фаз меди и цинка. В образцах с относительно
высоким содержание меди и цинка и низким содержанием калия, оксиды меди и цинка
представлены крупными кристаллитами, но на всех изученных образцах проявляется
так называемый диффузный галлофон в районе углов дифракции 2θ от 22 до 25 градусов, которая принципиально отличается от
галлофона чистого SiO2 расположенного в районе углов дифракции от 16
до 27 градусов. Его мы относим к мелкодисперсной фазе силикатов цинка и меди,
характеризующимся максимумом межплоскостного расстояния порядка 3,1 ангстрем.
Поскольку, гидросиликаты цинка имеют слоистую структуру [22] данные значения
рефлекса очевидно характерно расстояние между слоями. при более высокой
температуре прокаливания 600˚С кристалличной данной фазы увеличивается, а
расстояние между слоями практически не меняется.
Качественно данный состав катализатора можно реализовать и в
нанесенных системах, где в качестве носителя используется силикагель с большой
удельной поверхностью. В наше работе мы использовали марки ШСМ (шариковый
силикагель мелкопористый) с удельной поверхностью примерно 200 м2/г
и марки КСК (кусковой силикагель крупнопористый) с удельной поверхностью 150 м2/г.
В качестве пропитывающих растворов также использовали аммиачно-карбонатные
растворы меди и цинка, а также карбонатные и силикатные растворы калия.
Перечень приготовленных Т.о. образцов, приведен в таблице 3. Данный метод
представляет большею возможность для регулирования химического состава катализатора,
что достигается изменением качественного состава и концентрации пропитывающего
раствора. Калий в систему вводили двумя способами:
) в аммиачно-карбонатном растворе растворяли гидрокарбонат
калия и этим раствором пропитывали силикагель, далее образцы просушивали при
температуре 100˚С и далее прокаливали при температуре 400˚С;
) носитель пропитывали раствором силиката калия, образец
просушивали и пропитывали аммиачно-карбонатным раствором меди и цинка,
просушивали и прокаливали. При повторной пропитке, часть калия растворялась в
растворе, поэтому концентрация в готовом катализаторе получается ниже, чем в
модифицированном силикате (K2SiO3/SiO2). При
сушке пропитанного носителя удаляется вода и происходит кристаллизация
гидроксидов или силикатных солей. Но в отличие от осажденных катализаторов,
этот процесс усложняется взаимодействием растворенного вещества носителем, т.е.
центры кристаллизации располагаются на поверхности носителя и следовательно,
образующиеся твердые фазы будут иметь некую деформированную решетку по
сравнению со свободными соединениями. Эти эффекты проявляются при небольших
концентрациях нанесенного вещества. Поскольку, удельная поверхность нанесённых
катализаторов изменяется не слишком сильно по сравнению с исходным носителем и
пористая структура катализатора в общем задается носителем, данные эффекты
должны проявляться в катализаторах приготовленные в на шей работе.
Таблица 3
Приготовление и химический состав нанесенных катализаторов
№
Наименование и тип катализатора
Приготовление
Химический состав. масс. %
1
SU-28 CuO. ZnO/SiO2
Пропитка раствором МЦАКР Cu-0.10 моль/л.
Zn-0.49 моль/л 2
SU-29 CuO. ZnO. К2О/SiO2
Пропитка раствором МЦАКР Cu-0.1 моль/л. Zn-0.49
моль/л
Cu=1.00 Zn=7.30 K=0.97
3
SU-30 CuO. ZnO/К2SiO3/SiO2
(К2SiO3/SiO2 провяленный)
1. Пропитка раствором K2SiO3
K=0.2 моль/л 2. Пропитка раствором МЦАКР Cu-0.10 моль/л. Zn-0.49 моль/л
Cu=0.90 Zn=8.83 K=0.90
4
SU-31 CuO. ZnO/К2SiO3/SiO2
(К2SiO3/SiO2 прокаленный К=2.6
мас. %)
1. Пропитка раствором K2SiO3
K=0.2 моль/л 2. Пропитка раствором МЦАКР Cu-0.10 моль/л. Zn-0.49 моль/л
Cu=0.71 Zn=7.83 K=1.90
5
SU-32 CuO. ZnO/К2SiO3/SiO2
(К2SiO3/SiO2 K=6.1 мас. %)
1. Пропитка раствором K2SiO3
K=0.6 моль/л 2. Пропитка раствором МЦАКР Cu-0.10 моль/л. Zn-0.49 моль/л
Cu=1.73 Zn=7.64 K=4.00
6
SU-33 CuO. ZnO/К2SiO3/SiO2
(К2SiO3/SiO2 K=8.04 мас. %)
1. Пропитка раствором K2SiO3
K=1.2 моль/л 2. Пропитка раствором МЦАКР Cu-0.10 моль/л. Zn-0.49 моль/л
Хим. состав, мас. %
Уд. поверхность, м2/г
Cu=1.65 Zn=6.95 K=5.77
170.1
7
DM-30 CuO. ZnO/К2SiO3/SiO2
1. Пропитка раствором K2SiO3
K=0.4 моль/л 2. Пропитка раствором МЦАКР Cu-0.30 моль/л. Zn-0.40 моль/л
Cu=4.15 Zn=8.00 K=3.10
164.6
Если модифицированный носитель (K2SiO3/SiO2)
прокалить примерно 400˚С, то обменное взаимодействие при пропитке МЦАКРом
получается меньшим, чем при пропитке такого же носителя, но только высушенного,
и в последнем случае химический состав катализатора характеризуется большей
концентрацией меди и цинка, и меньшей калия за счет растворения соединений калия
в пропиточном растворе. Очевидно, такие катализаторы будут по свойствам ближе к
образцам полученных методом осаждения.
Описание установки для исследования
каталитических свойств образцов и расчетные формулы
Определение каталитических свойств производили на
микрокаталитической установке в проточном режиме. Хроматографический анализ
продуктов реакции позволяет разделить и количественно определить состав и
содержание продуктов катализа. Для контроля каталитических свойств в реакциях,
где выход целевого продукта при атмосферном давлении очень низок, необходим
детектор высокой чувствительности, достаточной для количественного определения
органических соединений (спиртов, эфиров и т.п.). Поэтому в газовой схеме
наряду с катарометром использовали пламенно-ионизационный детектор.
После прохождения реактора - (2), в котором поддерживается
необходимая температура, не прореагировавшие исходные вещества и продукты
реакции направляются в хроматографическую колонку с адсорбентом porapak Q - (6)
для разделения отходящих газов. При температуре адсорбента 120°C газы СО, СО2,
Н2 и СН4 на нем практически не удерживаются выходя из
колонки разделения и направляются сначала в катарометр, а затем в рабочую
ячейку ДИП- (7), а затем удаляются в атмосферу. Регистрация сигналов от
проходящих легких газов и компонентов продуктов реакции, имеющих большое время
удерживания регистрируются на приборе КСП.
С целью разделения "легких" газов (СО, СО2,
Н2, СН4) отбираемые газовые пробы направляются в
хроматографическую колонку (6) с активированным углем, и последовательно
проходят два детектора - катарометр (9) и ДИП (7).
Для предотвращения конденсации компонентов газовой смеси в
регулирующей аппаратуре и коммуникациях и сокращения размеров аппаратуры все
регистрирующие узлы вместе с колонкой для разделения смеси компонентов помещены
в термостат крана-дозатора - (1). Избыточное давление в системе определяется
гидравлическим сопротивлением двух разделительных колонок и составляет ~ 0,2
МПа.
Расчетные формулы:
Расчет степени разложения метанола проводился по следующей
формуле:
Θ= где: Sхол - площадь холодного пика, мм2
Si - площадь i-ого хроматографического пика, мм2
Расчет концентрации по метанолу:
= где площадь хроматографического пика, мм2
КСН3ОН-калибрвочный коэффициент по метанолу, мкмоль/мм2
22,4-мольный объем газа при н. у., см3/моль
,5-объем дозы, см3
0,845-фактор н. у. для крана дозатора
=hпривСН3ОН∙ (a+b∙exp (-c∙
hпривСН3ОН), мм2
где a,b,c - параметры модели получаемые при аппроксимации данных
Расчет удельной производительности по метанолу при i -
температуре=, мкмоль/с∙г, где: Vсг - объем сухого газа без
метанола,
,047-коэффициент соответствующий концентрации метанола
паро-газовой смеси 4,5об. %.нав - масса навески, г
Расчет количества израсходованного метанола (удельная
производительность):
∆G= Расчет удельной производительности катализатора по ДМЭ, водороду,
при i - температуре.
прв-ва -
высота пика соответствующего вещества при данной температуре, мм;в-ва
- калибровочный коэффициент по соответствующему веществу, мкмоль/мм;
Обсуждение результатов измерения каталитической активности
Конверсия метанола в условиях эксперимента сопровождается образованием
следующих продуктов, которые определялись методами газовой хроматографии и
фотокалориметрии: водород, метан, метилформиат и диметиловый эфир, образование
которых можно отобразить следующими уравнениями реакции:
3OH→CH2O+H2
(2), CH3OH→ CH3-O - CH3 + H2O
(3)3OH→ CH3OCOH +2H2 (4), 2 CH3OH→
CH4+2 H2O+C (5)
Процесс выхода катализатора на стационарный режим работы
оказывается достаточно длительным (несколько часов, в зависимости от образца
катализатора). При этом изменяется степень переработки метанола и
производительность по отдельным продуктам: водороду, формальдегиду и
метилформитату, тогда как концентрация диметилового эфира при данной
температуре остается практически неизменной. Длительный процесс формирования
обуславливает наблюдаемый дебаланс между образовавшимся количеством водорода и
формальдегида, т.к. согласно стехиометрии реакции мольное соотношение этих
веществ должно быть равно 1. Весьма вероятно, наблюдаемое зауглераживание
катализатора происходит через образование поверхностных гидроксометиленовых
полимерных части по следующей реакции: CH3OH→ (CH2O-)
n+ n H2г (6), которые далее уплотняются с образованием
более сложных графеновых структур (рис. 4-6). Далее на рисунках приведены
данные по активности катализатора, полученный при выдержке в реакционной среде
не менее часа. В исследуемых образцах при температуре 500 ˚С дебаланс
водорода и формальдегида уменьшается, то есть катализатор постепенно выходит на
стационарный режим работы. Внесение в катализатор калия улучшает как
активность, так и селективность, а именно уменьшает количество диметилового
эфира и количество выделяющегося углерода. Увеличение содержание калия
уменьшает время выхода на стационар, очевидно за счет уменьшения образования
твердых углеродистых соединений (рис.7). Эти же зависимости проявляются и в
катализаторах осажденного типа, продуктами являются формалин и водород, причем
соотношение их не сильно отличается от единицы, поскольку эти образцы содержат
большую концентрацию калия (рис.12). Но каталитическая активность в их меньше,
поскольку это обусловлено низкой удельной поверхностью катализатора.
Прокаливание при высокой температуре приводит к спеканию катализатора, что
собственно и приводит к уменьшению его производительности (рис.13). Оптимизация
состава соосажденного катализатора путем введения большого количества кремния
позволяет несколько увеличить активность катализатора, но тем не менее остается
ниже нанесенных систем.
Таблица 4
Производительность модельных катализаторов при t=500˚С
Приготовление
нанесенных катализаторов
![]() ,
,
![]() - приведённая высота пика метанола, мм;
- приведённая высота пика метанола, мм;
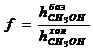 - поправочный коэффициент;
- поправочный коэффициент;
![]() - высота холостого пика в день эксперимента, мм
- высота холостого пика в день эксперимента, мм
![]()
![]() -высота холодного пика в день калибровки, мм
-высота холодного пика в день калибровки, мм
![]()
![]() , м. д.
, м. д.
![]()
![]() , мкмоль/с∙г
, мкмоль/с∙г
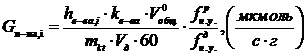 , где:
, где:
![]() , суммарный расход газовой смеси (газ-носитель + испарившийся
метанол) на входе в реактор, см3/мин;г/н - расход
газа-носителя;
, суммарный расход газовой смеси (газ-носитель + испарившийся
метанол) на входе в реактор, см3/мин;г/н - расход
газа-носителя;
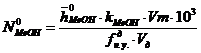 - мольная доля паров метанола в исходной газовой смеси на входе в
реактор;
- мольная доля паров метанола в исходной газовой смеси на входе в
реактор;
![]() - средняя высота пика метанола в холодном реакторе, мм;
- средняя высота пика метанола в холодном реакторе, мм;
![]() и
и ![]() - фактор нормальных условий для газа,
находящегося в петле крана-дозатора и газа проходящего реометр;д -
объём петли в кране-дозаторе.
- фактор нормальных условий для газа,
находящегося в петле крана-дозатора и газа проходящего реометр;д -
объём петли в кране-дозаторе.
Название и тип образца
Каталитическая активность
O/C
H/C
Θ, д. е.
FD
H2
1
SU-28 CuO. ZnO/SiO2
0.96
18.5
30.3
1.0
5.0
2
SU-29 CuO. ZnO. К2О/SiO2
0.89
21.8
27.4
1.0
4.4
3
SU-30 CuO. ZnO/К2SiO3/SiO2 (К2SiO3/SiO2 провяленный K=0.9 мас. %)
0.79
20.3
23.9
0.9
3.5
4
SU-32 CuO. ZnO/К2SiO3/SiO2 (К2SiO3/SiO2 K=6.17 мас. %)
0.53
16.4
18.6
1.0
4.0
5
DM-30 CuO. ZnO/К2SiO3/SiO2
0.40
13.4
13.2
1.0
4.0
6
SU-27 СuO. ZnO. K2O. SiO2
0.28
8.5
8.9
1.0
4.0
Выборочные данные по активности сведены в таблицу 4, которые принципиально подтверждают предшествующую трактовку изменения каталитических свойств модельных образцов.
Выводы:
1. Методами соосаждения силикатных соединений меди, цинка и калия из аммиачно-карбонатных растворов и пропитки пористого силикагеля приготовлены модельные катализаторы с различным соотношением компонентов цинка, меди, калия и кремния.
. Установлены концентрационные интервалы растворов, позволяющие получать гидроксосиликаты меди, цинка и калия с мелкодисперсной структурой и удельной поверхностью прокаленных образцов порядка 15 м2/г.
. Показано, что выход на стационарный режим силикатных катализаторов достаточно длительный процесс, который обусловлен образованием поверхностных углеводородных соединений и на образцах содержащие силикаты калия он существенно сокращается.
. Разработан способ введения калия в нанесенные катализаторы,
который позволяет сократить процесс формирования катализатора и улучшить его
селективность в отношении целевого продукта реакции дегидрирования метанола -
формальдегида.
Список литературы
1. Караев М.М., Леонов В.Е., Попов И.Г. Технология синтетического метанола // Под ред. Караева М.М. - М.: Химия, 1984. - 240 с
2. Шелдон Р.А. Химичесие продукты наоснове синтез-газа // М.: Химия. 1987, 248 с.
. Сеттерфилд Ч. Практический курс гетерогенного катализа // М.: Мир, 1984г.520 с.
. Розовский А.Я. Катализатор и реакционная среда // М. Наука. 1988. - 303с
. Носков А.С. Промышленный катализ в лекциях // М.: Калвис. 2005, 128 с.
. Мухленов И.П., Добкина Е.И., Дерюжкин В.И. и др., Технология катализаторов // Под ред. проф. Мухленова И. П.3-е издание, перераб. - Л.: Химия, 1989, 272 с.
. Дзисько В.А., Карнаухов А.П., Тараева Д.В. Физико-химические основы синтеза окисных катализаторов // Наука, 1978, 384 с.
. Неймарк Е.И. Силикагель, свойства, применение и методы его получения // Успехи химии, 1956, т.25, №6, с.748-769
. Айлер Р.К. Коллоидная химия кремнезема и силикатов // М., Стройиздат, 1959, 288 с.
. Garather K., Grissback R. Oberflachengrosse und Porenstruktur von Kieselglen in abhangigkeit von iher vorgeschichte // Kolloid Z, 1958, bd.100, №1, s.21-26
. Бресков Г.К., Борисова М.С., Джигат О.А. и др., Влияние условий приготовления на структуру силикагеля // ЖФК, 1948, т.22, №5
. Неймарк Е.И., Шейнфан Р.Ю. О влиянии промывной жидкости на процесс формирования структуры силикагеля // Коллоидный журнал, 1953, т.15, №1, с.45-59
. Слинякова И. Б, Неймарк И.Е. Структура и адсорбционные свойства силикагелей, полученных из щелочных сред // Коллоидный журнал, 1958, т. 20, №1, с.84-91
. Высоцкий З. З, Шаля В.В. Теплоты гидратации некоторых катионов и влияние адсорбции последних на структуру силикагеля // Коллоидный журнал, 1958, т. 20, №1, с.29-33
. Wolf F., Beyer H. Ober beriechungenu zwischen herstellungsbedingen und oberf la chen strukturen von kiesilgelen // Kolliod Z, 1959, Bd.165, №2, S.151-155
. Берестнева З.Я., Корецкая Т.А., Каргин В.А. Электронно-микроскопическое и адсорбционное исследование SiO2 золей // Коллоидный журнал, 1949, т.11, №6, с.369-370
. Оккерсе К. Пористый кремнезем, В. кн. "Строение и свойства адсорбентов и катализаторов // Под ред. Линсела Б.Г. пер. с англ.М., "Мир", 1973, с.233-284
. Киселев А.В., Лыгин В.И., Неймарк Е.И. и др., Электронно-микроскопическое и адсорбционное исследование силиказолей и силикагелей // Коллоидный журнал, 1958, т. 20, №1. С.52-58
. Берестнева З.Я., Корецкая Т.А., Каргин В. А Электронно-микроскопическое исследование TiO2 золей и механизм образования коллоидных частиц // Коллоидный журнал, 1950, т.12, №5, с.338-341
. Рыжак И.А. Исследование генезиса морфологических структур гидроокисей и окисей алюминия и железа // Канд. дис., Навосибирск, 1971, 128с.
. Al M. Dehydrogenation of methanol formate over copper-based catalyst // Applied Catalisis, 1984, p.259-270
. Горшков C.В., Лин Г.И., Розовский А.Я. Механизм дегидрирования метанола в метилформиат и пути управления селективностью процесса // Кинетика и катализ, 1999, том40, №3, с.372-375
24. Chung M. - J., Park K. - Y., Lee B. - J. and Ihm S. - K. Methylformate formation from methanol and CO ON Cu/ZnO catalysts // Korean Journal of Chemical Engineering <http://link.springer.com/journal/11814>, 1993, V.10, Is.3 <http://link.springer.com/journal/11814/10/3/page/1>, pp.188-190
25. Okamoto Y., Fukino K., Imanaka T., and Teranishi S. Synergy Between Cu and ZnO methanol conversion over Cu-ZnO catalysts // Chemistery letters, 1984, pp.71-74
26. Tsoncheva T., Sarkadi-Priboczki E.11C-radiolabeling study of methanol decomposition on copper oxide modified mesoporous SBA - 15 silica // Appl. Surf. Science, 2011, том 257, с.6661-6666
. Соломатин Г.И., Соболевский В.С., Григорьев В.В. и др. Ик-спектры катализаторов и адсорбированных молекул
. Антонюк С.Н., Егорова Е.В., Якерсон В.И. и др. Каталитические превращения метанола с целью получения метилформиата, водорода и монооксида углерода
. Hong X., Ren S. Selective hydrogen production from methanol oxidative steam reforming over Zn-Cr catalysts or without Cu loading // International journal of hydrogen enerdgy 33, 2008, p.700-708
. Шлегель Л., Гутшик Д., Розовский А.Я. Разложение метанола на Сu-содержащих катализаторах синтеза метанола // Кинетика и катализ, 1999, том40, №3
. Усачев Н.Я., Круковский И.М., Канаев С.А. Неокислительное дегидрирование метанола в формальдегид // Нефтехимия, 2004, том 44, № 6, с.411-427
32. Music <http://www.sciencedirect.com/science/article/pii/S0926860X97001956> A., Batista <http://www.sciencedirect.com/science/article/pii/S0926860X97001956> J., Levec <http://www.sciencedirect.com/science/article/pii/S0926860X97001956> J. Gas-phase catalytic dehydrogenation of methanol to formaldehyde over ZnO/SiO2 based catalysts, zeolites, and phosphates // Appl. Catalysis, 1997, V.165, №1, P.115-131
. Li J. X., REN L. - P., Dai W. - L., Yong CAO and FAN K. - N. Novel Flower-Like Ag-SiO2-MgO-Al2O3 Material: Preparation, Characterization and Catalytic Application in Methanol Dehydrogenation // Chinese Journal of Chemistry<http://onlinelibrary.wiley.com/doi/10.1002/cjoc.v26:6/issuetoc> 2008 V, 26, Is.6, p.1045-1051
. Chen A. K., Masel R. Direct conversion of methanol to formaldehyde in the absence of oxygen on Cu (210) // Surf. Science. 1995, V.343, №1, Р.17-23.
35. Zhang R., Sun Y., Peng S. In situ FTIR studies of methanol adsorption and dehydrogenation over Cu/SiO2 catalyst // Fuel. 2002, V.81, №11, Р.1619-1624
36. Сhan L., Griffin J. Methanol decomposition on oriented ZnO thin films // Surf. Science. 1985, V.155, №3, Р.400-412
37. Okamoto Y., Fukino K., Imanaka T., and Teranishi S. Synergy Between Cu and ZnO methanol conversion over Cu-ZnO catalysts // Chemistery letters, 1984, p.71-74
38. Юрьева Т.М., Плясова Л.М., Кринер Т.А., Макарова О.В. // Кинетика и катализ, 1995, т.36, №5, с.769-773
39. Matsumura Y., Hashimoto K., Yoshida S. Degydrogenation of methanol to formaldehyde over silicalite // J. Catalysis. 1986, V.100, №3, Р.392-400.
40. Третьяков В.Ф., Бурдейная Т.Н., Давыдова М.Н. Каталитическое неокислительное дегидрирование метанола в формальдегид // Ученые записки МИТХТ, 2003, выпуск 9
41. Уменушкина С.И. Приготовление катализаторов на основе силикатов цинка для конверсии метанола // Дипломная работа, кафедра ТНВ, ИГХТУ, 2012, 75с
. База данных AST