Материал: Потенциометрический метод исследования мясных продуктов
Диспергирование
К пробе добавляют 450 см3 воды. Емкость закрывают и включают смеситель (блендер) на малую скорость вращения для начального диспергирования. Затем проводят тщательное перемешивание при высокой скорости в течение от 1 до 2 мин так. чтобы получить однородную суспензию твердого материала.
Сразу после перемешивания в предварительно взвешенный стакан вместимостью 250 см3 с помощью пипетки вносят 50 см3 полученной суспензии пробы. Определяют массу испытуемого раствора
Кривая титрования
В стакан вместимостью 250 см3 с помощью пипетки вносят 25 см3 раствора хлорида натрия. Разбавляют водой до общего объема примерно 50 см3 и добавляют 50 см3 разбавленной азотной кислоты.
В полученный раствор помещают электроды и
включают перемешивание раствора. В процессе титрования перемешивание должно
проводиться с постоянной скоростью достаточно энергично и без разбрызгивания
(рис 5).

Рисунок 5 - Потенциометрическое титрование
Титрование проводят раствором азотнокислого серебра, регулируя скорость капания по скорости изменения потенциала так. чтобы построить правильный график зависимости изменения потенциала в милливольтах (ось У) от объема раствора азотнокислого серебра в см3 (ось X).
Всего добавляют 50 см3 раствора азотнокислого серебра для построения полной кривой титрования. Точку перегиба определяют, проведя две прямые линии под углом наклона 45° к осям и касательно к кривой титрования в двух точках ее наибольшей кривизны.
Точка перегиба определяется как точка пересечения кривой титрования и линии, находящейся посередине между двумя проведенными линиями и параллельно им.
Точку перегиба используют как конечную точку при титровании раствора пробы. Периодически перепроверяют потенциал конечной точки относительно связующего потенциала электрода сравнения. При замене отдельного электрода, комбинированного электрода либо рН-метра конечную точку определяют заново построением новой кривой титрования.
Исходя из израсходованного на титрование раствора азотнокислого серебра рассчитывают его молярную концентрацию и доводят ее до 0.0856 мопь/дм3.
Определение
В суспензию пробы добавляют 50 см3 разбавленной азотной кислоты (и титруют, как описано для раствора хлорида натрия. Если концентрация хлорида равна или меньше 1 %. то используют бюретку вместимостью 10 см3.
При проведении серии испытаний одного и того же мясного продукта для достижения большей точности используют конечную точку, измеренную по кривой титрования этого мясного продукта, а не конечную точку, полученную на стандартном растворе хлорида натрия.
Расчет
Содержание хлоридов в образце вычисляют по
формуле (4):
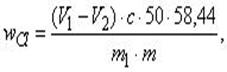 (4)
(4)
где wCI - содержание хлоридов в образце, выраженное в виде массовой доли хлорида натрия в процентах:- объем азотнокислого серебра, израсходованного на титрование суспензии пробы, см3: - объем азотнокислого серебра, израсходованного на контрольное титрование, см3:
с - концентрация раствора азотнокислого серебра, моль/дм3: - масса испытуемой суспензии, г:- масса испытуемой пробы, г.
Результат записывают с округлением до 0.1 % (массовая доля).
Точность
Показатели точности метода установлены с помощью межлабораторных испытаний, выполненных в соответствии с ГОСТ Р ИСО 5725-1-2002. Значения предела повторяемости г и предела воспроизводимости R получены для уровня вероятности 95 %.
Повторяемость
Абсолютное расхождение между результатами двух
независимых единичных определений, полученных при использовании одного и того
же метода, для идентичного испытуемого материала, в одной и той же лаборатории,
одним и тем же оператором, с использованием одного и того же оборудования в течение
короткого промежутка времени, не должно превышать предел повторяемости г.
вычисляемый по формуле (5):
г = 0.002 + 0.033 wCI (5)
где wCI - среднеарифметическое значение двух результатов определения массовой доли хлорида натрия, %.
Воспроизводимость
Абсолютное расхождение между результатами двух
независимых единичных определений, полученных при использовании одного и того
же метода, для идентичного испытуемого материала, в различных лабораториях,
разными операторами, с использованием различного оборудования, не должно
превышать предел воспроизводимости R, вычисляемый по формуле (6):
R = 0.005 + 0,066 WCI (6)
где WCI - среднеарифметическое значение двух результаты определения массовой доли хлорида натрия. %.
Протокол испытаний должен включать:
использованный метод отбора образцов, если он известен:
полученный (е) результат(ы) испытания;
если проводилась проверка повторяемости, окончательный оцененный результат.
В протокол испытаний также должна быть включена
вся информация, необходимая для полной идентификации образца.
Заключение
В настоящее время предприятия пищевой промышленности поставляют на потребительский рынок широкий ассортимент продуктов питания, которые не всегда удовлетворяют современным требованиям качества, поэтому вопросам безопасности пищевых продуктов уделяется серьезное внимание.
Контроль качества продовольственного сырья и пищевых продуктов осуществляется различными физико-химическими методами, среди которых лидирующие позиции занимают классические методы анализа (титриметрия, гравиметрия и др.), электрохимия, фотометрия и газовая хроматография.
Разработка и внедрение эффективных инструментальных методов подтверждения подлинности продуктов питания позволяет оздоровить конкурентную борьбу между производителями за рынок сбыта и повысить средний уровень качества продукции.
В результате выполненной работы в первом разделе изучены методы потенциометрии, а именно: сущность метода, стандартный водородный электрод, электроды сравнения, прямая потенциометрия, метод потенциометрического титрования и метод добавок.
Наибольшее распространение среди прямых потенциометрических методов получил метод определения рН. Прямые потенциометрические методы стали называть ионометрическими методами анализа, или ионометрией. Эта группа методов интенсивно развивается в связи с успехами в конструировании и улучшении качества ионоселективных электродов, позволяющих проводить анализ быстро и точно. Например, ионометрический метод рекомендован как международный стандарт для анализа нитратов в овощах и фруктах.
Во втором разделе исследована методика определения массовой доли хлористого натрия с помощью метода потенциометрического титрования в мясных продуктах. Метод потенциометрического определения массовой доли хлоридов позволяет определить содержание хлоридов в мясе и мясных продуктах, включая мясо птицы и продукты из него, с массовой долей хлорида натрия равной или превышающей 0,25%.
Поваренная соль (химическое название - хлорид натрия, NaCl) является наиболее широко и давно применяемой «пищевой добавкой» и обычно играет одну из самых важных ролей в производстве мясных продуктов.
Определены средства измерения, условия
окружающей среды при проведении определения, пробоподготовка объекта
исследования, проведение измерения, расчет содержания хлористого натрия,
порядок заполнения протокола испытания.
Список литературы
1. Ковалева, Ирина Павловна. Методы исследования свойств сырья и продуктов питания: Рекомендовано Умо в качестве учебного пособия для вузов/ И.П. Ковалева, И.М. Титова, О.П. Чернега. - СПб.: Проспект Науки, 2012. - 152 с.
. Лакиза Н. В., Неудачина Л. К. Анализ пищевых продуктов : [учеб. пособие] / М-во образования и науки рос. Федерации, Урал. федер. ун-т. - Екатеринбург : изд-во Урал. ун-та, 2015. - 188 с.
. Физико-химические методы исследования: Учебник для бакалавров // Криштафович В.И., Криштафович Д.В., Еремеева Н.В., - 2015 год - 208 с.
. Тимофеева В.А. Т 50 Товароведение продовольственных товаров / В.А. Тимофеева.Учебник. Изд-е 5-е, доп. и перер. -Ростов н/Д: Феникс. 2005.- 386 с.
. Товароведение однородных групп продовольственных товаров: Учебник для бакалавров // Елисеева Л.Г., Родина Т.Г., Рыжакова А.В. и др.; под ред. Л.Г. Елисеевой - 2014 год.- 930 с.
. Аналитическая химия и физико-химические методы анализа (под ред. Ищенко А.А.). М., ИЦ «Академия», 2010.- 416 с.
. Нечипоренко А.П. Физико-химические (инструментальные) методы анализа. Электрохимические методы. Потенциометрия и кондуктометрия: Учеб.-метод. пособие / Под ред. В.В. Кириллова. - СПб.: НИУ ИТМО; ИХиБТ, 2013. - 34 с.
. Базарнова Ю.Г. Методы исследования сырья и готовой продукции: Учеб.-метод. пособие. СПб.: НИУ ИТМО; ИХиБТ, 2013. 76 с.
. Физико-химические методы анализа продуктов питания : учебно- методическое пособие / Г.Е. Башкеева, Н.У. Мухаметчина. - Нижнекамск : НХТИ ФГБОУ ВПО «КНИТУ», 2015. - 102 с.
. Нечипоренко А.П. Физико-химические (инструментальные) методы анализа. Электрохимические методы. Потенциометрия и кондуктометрия: Учеб.-метод. пособие / Под ред. В.В. Кириллова. - СПб.: НИУ ИТМО; ИХиБТ, 2013. - 34 с.
. Потенциометрические методы анализа: Метод. указ. к лаб. работам/ Сост. Б.М. Стифатов, Е.Ю. Мощенская. Самара; Самар. гос. тех. ун-т, 2013. - 31 с.: ил.
. Курлански М. Всеобщая история соли / Марк Курлански / Переводчики: Н. Жукова, М. Суханова. - М.: КоЛибри, 2007. - 520 с.
. Похлебкин В.В. История важнейших пищевых продуктов. Издатель- ство: Центрполиграф, 2009
. ГОСТ ISO 1841-2-2013 МЕЖГОСУДАРСТВЕННЫЙ СТАНДАРТ МЯСО И МЯСНЫЕ ПРОДУКТЫ Потенциометрический метод определения массовой доли хлоридов где выходные данные про эти стандарты
. ГОСТ Р ИСО 5725-1-2002 Точность (правильность и прецизионность) методов и результатов измерений. Часть 1. Основные положения и определения