Материал: Потенциометрический метод исследования мясных продуктов
Хлорсеребряный электрод. В качестве электрода сравнения используют также другой электрод второго рода - хлорсеребряный, представляющий собой серебряную проволоку, покрытую хлоридом серебра и помещённую в раствор хлорида калия. Хлорсеребряный электрод также обратим относительно анионов хлора: Аg / АgСl, КСl
Величина потенциала хлорсеребряного электрода
зависит от активности ионов хлора; данная зависимость имеет следующий вид (2):
![]() (2)
(2)
Чаще всего в качестве электрода сравнения используется насыщенный хлорсеребряный электрод, потенциал которого зависит только от температуры. В отличие от каломельного, он устойчив при повышенных температурах и применим как в водных, так и во многих неводных средах.
Каломельный электрод. Работа с водородным электродом довольно неудобна, поэтому в качестве электрода сравнения часто используется более простой в обращении каломельный электрод, величина электродного потенциала которого относительно стандартного водородного электрода точно известна и зависит только от температуры. Каломельный электрод состоит из ртутного электрода, помещенного в раствор КСl определенной концентрации и насыщенный каломелью Hg2Сl2: Нg / Нg2Сl2, КСl
Каломельный электрод обратим относительно
анионов хлора и уравнение Нернста для него имеет вид (3):
![]() (3)
(3)
Потенциометрический метод анализа существует в нескольких вариантах:
Прямая потенциометрия. Метод основан на установлении зависимости потенциала измерительного электрода от концентрации раствора (построение калибровочного графика или настройка измерительного прибора) и последующим ее использовании для анализа растворов неизвестной концентрации. Метод достаточно прост и экспрессен. Наиболее широко применяется для измерения рН.
Точность метода зависит, в первую очередь, от типа измерительного электрода. Так для рН-электродов достижима точность 0,01 рН и выше, а для ионоселективных электродов принято оценивать погрешность величиной 4% для однозарядных ионов и 8% для двухзарядных. Точность измерений так же заметно зависит от степени отклонения крутизны электродной функции от теоретического значения. Поэтому крутизна электродной функции является показателем качества электрода. Реальная крутизна электродной функции обычно равна или несколько ниже теоретического значения, превышение ее над теоретической величиной чаще всего говорит об ошибке эксперимента. Следует помнить, что со временем, по мере выработки ресурса электрода, крутизна снижается, и погрешности измерений возрастают.
Достоинством и недостатком метода одновременно является то, что измеряемый потенциал зависит от активности. Это единственный метод прямого определения активности ионов в растворах. Но с другой стороны аналитиков чаще интересует концентрация, а пересчет активности ионов в концентрацию с применением эмпирических коэффициентов активности вызывает некоторую дополнительную погрешность.
Существует вариант метода, в котором в калибровочные и анализируемые растворы вводится индифферентный электролит. Это позволяет проводить калибровку и последующий анализ в единицах концентрации.
Наибольшее распространение среди прямых потенциометрических методов получил метод определения рН. Прямые потенциометрические методы стали называть ионометрическими методами анализа, или ионометрией. Эта группа методов интенсивно развивается в связи с успехами в конструировании и улучшении качества ионоселективных электродов, позволяющих проводить анализ быстро и точно. Например, ионометрический метод рекомендован как международный стандарт для анализа нитратов в овощах и фруктах.
Потенциометрическое титрование. Метод существует во множестве вариантов. Он основан на проведении специфической химической реакции под контролем ионоселективного или редокс-электрода. Могут применяться следующие реакции: нейтрализации, осаждения, комплексообразования или окисления-восстановления. Калибровка электрода обычно не требуется, он служит только для установления точки эквивалентности. Расчет концентрации анализируемого вещества производится на основании объемов и концентраций, участвующих в реакции растворов.
Метод более сложный и трудоемкий по сравнению с предыдущим, но имеет ряд преимуществ. Результаты, полученные этим методом, обычно более точны и воспроизводимы (< 1%). Титрование позволяет определять вещества, на которые не существует ионоселективных электродов (косвенное определение). От применяемого электрода не требуется высокой линейности и стабильности характеристики. Правильный подбор реактивов позволяет проводить анализ в присутствии мешающих ионов.
К недостаткам метода следует отнести невозможность его применения для непрерывного контроля, а так же то, что в ряде случаев им нельзя определять малые концентрации.
Методы добавок. Родственный титрованию метод. Существует во множестве вариантов, некоторые из которых обладают преимуществами, существенно расширяющими область применения потенциометрии. Это, например, возможность анализа малых концентраций, лежащих на пределе линейности электродной характеристики, а иногда и ниже («метод добавок с последующим разбавлением»).
В присутствии избытка комплексообразующих агентов метод стандартных добавок является единственным методом, пригодным для определения общей концентрации ионов, входящих в состав комплексов.
Измерение ЭДС при прямой и косвенной
потенциометрии проводят с помощью потенциометра - прибора, в котором
смонтирована вся электрическая схема установки с выводом контактов для
подключения гальванического элемента (рис.3).

Рисунок 3 - Потенциометр (иономер)
2.
Практическая часть
2.1 Объекты, постановка целей и задач
исследования
Цель работы - изучить возможность применения методов потенциометрического анализа мясных продуктов.
Для достижения поставленной цели необходимо было решить следующие задачи:
изучить метод потенциометрического анализа;
проанализировать объекты исследований;
изучить методики потенциометрического анализа в приложении к данному объекту.
Объектом исследования представленной работы являются мясные продукты.
Мясные товары - это пищевые продукты, произведенные только из мяса теплокровных животных и птицы или с добавлением другого вспомогательного сырья растительного или животного происхождения и подвергнутые определенной технологической переработке.
Далее будет показана возможность применения потенциометрического метода определения массовой доли хлоридов.
Поваренная соль (химическое название - хлорид натрия, NaCl) является наиболее широко и давно применяемой «пищевой добавкой» и обычно играет одну из самых важных ролей в производстве мясных продуктов.
С химической точки зрения NaCl - это натриевая соль соляной кислоты. В большинстве стран мира соль относят к пищевым продуктам, а не к добавкам.
Соль состоит из 39,3% натрия и 60,7% хлора, для сохранения сыпучести в течение длительного периода времени в нее нередко вносят небольшое количество антислеживающего агента. Соль получают путем разработок месторождений (каменная соль) или выпариванием (морская соль).
Натрий является жизненно важным нутриентом и должен поступать в организм вместе с пищей. Недостаточное потребление натрия представляет собой угрозу нервной и мышечной системам человеческого организма, в то время как переизбыток натрия приводит к таким отрицательным последствиям, как высокое кровяное давление.
В растворе хлорид натрия распадается на ионы Na+ и Сl-.
Добавление соли к мясу увеличивает ионную силу
раствора, кроме того, ионы соли связываются с ионами боковых цепей белков и
способствуют разделению этих боковых цепей (рис.4)
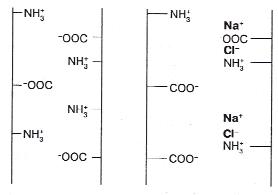
Рисунок 4 - Ионы соли связываются с ионами
боковых цепей белков и способствуют разделению этих боковых цепей
Хлорид-ион также важен, поскольку способствует абсорбции калия в организме человека. Он является компонентом желудочного сока и усиливает способность крови переносить диоксид углерода из тканей в легкие.
Соленый вкус мясных продуктов, содержащих хлорид натрия, обусловлен прежде всего присутствием отрицательно заряженных ионов Сl- и в меньшей степени - положительно заряженных ионов Na+.
В продуктах с пониженным содержанием натрия часто альтернативой поваренной соли является хлорид калия.
В мясе и мясных продуктах соль выполняет несколько функций:
соль является усилителем вкуса и аромата, и при недостаточном количестве соли мясное блюдо или мясной продукт не будут иметь хорошего вкуса, даже если в процессе приготовления использовали специи.
соль в сочетании с фосфатами переводит белок мяса в гидратированное состояние, что повышает способность белка связывать дополнительную воду, а также эмульгировать жир в мясных продуктах. Внесение соли влияет на взаимодействия между актином и миозином. Электростатические взаимодействия обусловлены наличием в молекуле белков положительных и отрицательных зарядов, которые притягивают или отталкивают друг друга. При добавлении соли возникает эффект отталкивания, при этом расширяются промежутки между молекулами актина и миозина. Для эффективного активирования белка дозировка соли должна составлять не менее 12 г на килограмм мясного продукта.
При активировании белка также улучшается текстура мяса.
соль снижает содержание свободной воды в продукте), поэтому в таких мясных продуктах, как сырая ферментированная салями или вяленые продукты, на начальных стадиях производства соль является важным средством предупреждения микробиологической порчи.
Добавление соли способствует росту грамположительных бактерий. Среди патогенных бактерий лишь очень немногие являются грамположительными, например, Salmonella spp. и Escherichia coli.
соль как таковая ядовита для бактерий, поскольку создает дисбаланс электролитов в клетке. Добавление соли к мясу вызывает небольшой сдвиг изоэлектрической точки белков мышечной ткани в более кислую область (изоэлектрическая точка с 5,2 может сдвинуться примерно до 5,0). В результате может быть связано большее количество воды без изменения значения рН мяса, так как сдвиг изоэлектрической точки от 5,2 до 5,0 приводит к увеличению разницы между значением рН мяса и его изоэлектрической точкой. Например, до добавления соли эта разница составляла 0,5 единиц рН (между значениями 5,7 и 5,2). После добавления соли разница составила 0,7 единиц (между значениями 5,7 и 5,0). Увеличение разницы между двумя значениями рН обусловливает усиление капиллярного эффекта мышечных волокон, что в свою очередь ведет к повышению ВСС.
соль, и особенно ионы натрия, может вызывать повышение кровяного давления при чрезмерном потреблении. Существуют «легкие» мясные продукты, в которых количество натрия составляет около 450-750 мг на 100 г продукта (в зависимости от пищевых нормативов в соответствующей стране). В таких продуктах на килограмм добавляют только около 8 г поваренной соли (хлорида натрия), заменяя его хлоридом калия. Таким образом, в целом на килограмм продукта приходится 12-16 г солей.
При оценке содержания натрия в мясном продукте
также не следует забывать, что натрий часто вносят в мясные продукты в составе
других веществ, таких как нитрит натрия, эриторбат натрия и фосфаты натрия.
.2 Потенциометрический метод определения
массовой доли хлоридов
Метод потенциометрического определения массовой доли хлоридов позволяет определить содержание хлоридов в мясе и мясных продуктах, включая мясо птицы и продукты из него, с массовой долей хлорида натрия равной или превышающей 0,25%.
Сущность метода. Пробу диспергируют в воде. Аликвоту полученной суспензии подкисляют и потенциометрически титруют раствором азотнокислого серебра с использованием серебряного электрода.
Необходимые реактивы:
Вода дистиллированная и не содержащая ионов галогенов.
Проба на отсутствие ионов галогенов: к 100 см3 воды добавляют 1 см3 азотнокислого серебра c (AgN03) = 0.1 моль/дм3 и 5 см3 азотной кислоты (с (HN03) = 4 моль/дм3). Допускается образование только легкого помутнения.
Азотная кислота, разбавленный раствор в объемном соотношении 1:49.
Разбавляют 20 см3 концентрированной азотной кислоты (ρ = 1.40 г/см3) водой и доводят объем до 1000 см3 водой.
Серебро азотнокислое, стандартный раствор, с (AgNO3) = 0,0856 моль/дм3
В воде растворяют 14.541 г азотнокислого серебра, предварительно высушенного в течение 2 ч при температуре (150 ± 2) °С и охлажденного в эксикаторе. Полученный раствор количественно переносят в мерную колбу с одной отметкой вместимостью 1000 см3 и доводят водой до отметки. Полученный раствор хранят в темной стеклянной посуде в защищенном от прямого солнечного света месте.
Натрия хлорид, стандартный раствор с (NaCI) = 0.0856 моль/дм3
В воде растворяют 5.000 г хлорида натрия, предварительно высушенного в течение 2 ч при температуре (110 ± 2) °С и охлажденного в эксикаторе. Полученный раствор количественно переносят в мерную колбу с одной отметкой вместимостью 1000 см3 и доводят водой до отметки.
Необходимое оборудование:
Устройство для гомогенизации механическое или электрическое, способное гомогенизировать пробу.
Это может быть высокоскоростной ротационный куттер или мясорубка с решеткой, диаметр отверстий которой не превышает 4.5 мм.
Лабораторный смеситель (блендер), оборудованный переключателем для перемешивания при низкой и высокой скорости вращения.
Электроды, комбинированный серебряный электрод биллетного (твердотельного) типа, или отдельные серебряный индикаторный электрод и стеклянный электрод сравнения.
Перед первым использованием и. при необходимости, ежедневно перед использованием рабочую поверхность серебряного комбинированного электрода чистят чистящим порошком или другим подходящим средством, затем тщательно ополаскивают водой (после испытания некоторых видов образцов может потребоваться ополаскивание горячей водой). Очистку других типов электродов проводят в соответствии с рекомендациями изготовителя. При необходимости, для предотвращения смещения измеряемой конечной точки титрования проводят дополнительную очистку. В течение испытаний нескольких образцов периодически ополаскивают электроды водой и вытирают тканью для предотвращения образования пленки. При использовании серебряных электродов биллетного типа нет необходимости покрывать их хлоридом серебра.
Магнитная мешалка с регулировкой на постоянную скорость вращения.метр предпочтительно с непосредственным, например, цифровым, отсчетом показаний с ценой деления шкалы не более 10 мВ и диапазоном измерения не менее ± 700 мВ.
Пипетка вместимостью 50 см3.
Весы с погрешностью взвешивания ± 0.1 г.
Отбор проб. Масса представительной пробы должна быть не менее 200 г.
Подготовка пробы. Лабораторную пробу гомогенизируют с помощью подходящего оборудования. Температура пробы при этом не должна превышать 25 °С. При использовании мясорубки пробу пропускают через нее не менее двух раз.
Подготовленную пробу помещают в воздухонепроницаемую емкость, закрывают и хранят, не допуская ее порчи и изменения состава. Испытания (анализ) пробы проводят по возможности быстрее. но не позднее 24 ч после гомогенизации.
Порядок определения:
Проба
В емкости смесителя (блендера) вместимостью 1000 см3 взвешивают пробу массой примерно 50 г с точностью не более 0,1 г.