Материал: подготовка к контрольной работе 1

концентрация уменьшается в 2 раза. Подставляем в формулу для расчета рН буферных растворов, образованных слабой кислотой и ее солью,
числовые данные:
[H |
+ |
] =1,82 |
10 |
−5 |
|
0,1 2 |
|
|
|
2 |
0,1 |
||||
|
|
|
|
|
|
||
pH = − lg[H+] = 5 –
=1,82 10 |
−5 |
моль/л |
|
lg 1,82 = 4,74
Таким образом, при равных концентрациях компонентов буферного раствора, образованного слабой кислотой и ее солью, рН буферного раствора равно рK слабой кислоты.
Задача № 8. Какая из малорастворимых солей более растворима в
воде: AgSCN или Ag2CrO4 и во сколько раз?
K |
S |
(AgSCN) |
|
|
= 1,1∙10−12;
KS (Ag2C2O4 ) = 1,1∙10−12.
Решение. Поскольку соли не являются однотипными (т.е. имеют разный стехиометрический состав), нельзя сравнивать их растворимость по значениям произведений растворимости. Необходимо рассчитать ионные растворимости и сравнить их.
В общем виде ионная растворимость электролита состава KtmAnn
рассчитывается по формуле:
SKt mAnn |
= |
m+n |
|
KS (Kt m Ann ) |
|
|||
m |
m |
n |
n |
|
||||
|
|
|
||||||
|
|
|
|
|
|
|
||
Для бинарного электролита типа AgSCN растворимость рассчитывается по формуле:

S( AgSCN) = |
K |
S |
(AgSCN) = |
1,1 10 |
−12 |
|
|||||
|
|
|
|
|
1 10 |
−6 |
|
моль/л
Для Ag2CrO4 растворимость будет равна:
|
|
|
|
|
K |
S |
(Ag |
2 |
CrO |
4 |
) |
= 3 |
1,1 10 |
−12 |
||
S(Ag |
|
CrO |
|
) =1+2 |
1 10 |
|||||||||||
2 |
4 |
|
1 |
|
|
2 |
|
4 |
||||||||
|
|
|
|
|
2 |
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
1 |
|
|
|
|
|
||||
Таким образом, соль Ag2CrO4 |
более растворима в |
|||||||||||||||
− 4 |
моль/л |
|
воде, чем соль
AgSCN в 10−4 = 100 раз.
10−6
Задача № 9. Как изменится растворимость иодида серебра, если к его насыщенному раствору прибавить иодид калия до концентрации
1,0 10 −4 моль/л? KS(AgI) = 8,3 · 10 −17.
Решение. Введение в раствор одноименных с осадком ионов (в
данном случае иодид-ионов) приводит к сдвигу равновесия реакции:
AgI Ag+ + I −
в сторону образования осадка AgI и, соответственно, к уменьшению его растворимости.
Исходя из произведения растворимости иодида серебра рассчитаем вначале растворимость его в чистой воде:
KS(AgI) = [Ag+][I −] = 8,3 · 10 −17
S(AgI) = [Ag+] = [I −] = 
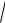 KS (AgI) =
KS (AgI) = 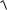
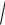 8,3 10−17 = 9,1 10−8 моль /л
8,3 10−17 = 9,1 10−8 моль /л

При добавлении иодида калия в растворе будет находиться избыток иодид-ионов, и произведение растворимости будет выражаться следующим образом:
KS(AgI)= [Ag+]([I −] + [I −]KI),
где [I −]KI – концентрация прибавленного к раствору иодида калия. Так как присутствие иодид-ионов подавляет растворение иодида серебра,
концентрацией иодид-ионов, образующихся в результате растворения иодида серебра, можно пренебречь, тогда
|
|
|
KS(AgI) = [Ag+][I −]KI |
|
|
||||
S(AgI) = [Ag |
+ |
] = |
KS (AgI) |
= |
8,3 10−17 |
= 8,3 10 |
−13 |
моль /л |
|
|
[I−]KI |
|
1,0 10−4 |
|
|||||
|
|
|
|
|
|
|
|||
Таким образом, при введении в раствор иодида серебра иодида калия
растворимость AgI уменьшается в 9,1 10−8 = 1,1 10 4 раз за счет влияния
8,3 10−13
одноименных ионов.
Задача № 10. Осадок BaSO4 массой 0,2534 г промыт: а) 200 мл дистиллированной воды (при условии полного насыщения); б) 200 мл
0,01 М H2SO4 .
Сколько процентов BaSO4 будет потеряно при промывании в каждом случае? KS (BaSO4 ) =1 10−10, M (BaSO4 ) = 233,4 .
Решение. Потери при промывании осадка рассчитываются по общей формуле:
(BaSO4,%) = S∙V∙M ,

но растворимость (S) для случаев а) и б) определяется по-разному.
а) При промывании водой потери за счет растворения осадка BaSO4 в
воде рассчитывают из произведения растворимости, при этом потери составляют:
(BaSO4 ) = 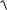
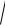 KS (BaSO4 ) V (H2O) M (BaSO4 ) =
KS (BaSO4 ) V (H2O) M (BaSO4 ) =
= 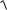
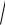 1 10−10 1000200 233,4 = 4,7 10−4 г
1 10−10 1000200 233,4 = 4,7 10−4 г
Массовая доля потерь в процентах составляет:
|
4,7 10 |
−4 |
|
ω(%) = |
|
||
0,2534 |
|||
|
|||
100 =
0,18
%
б) При промывании осадка BaSO4 раствором H2SO4 необходимо учитывать влияние одноименного иона на растворимость осадка, которая в данном случае будет рассчитываться по формуле, аналогичной формуле,
приведенной в задаче № 11. Потери при этом будут составлять:
(BaSO |
|
) = |
K |
S |
(BaSO |
4 |
) |
V (H |
|
O) M (BaSO |
|
) = |
||||||||||
4 |
|
|
|
|
|
|
|
|
|
2 |
4 |
|||||||||||
|
|
|
|
2− |
|
|
|
|
|
|
|
|||||||||||
|
|
|
[SO |
|
] |
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
4 |
H |
2 |
SO |
4 |
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
1 10 |
−10 |
|
200 |
|
|
|
|
|
−7 |
|
|
|
|||||||
|
|
= |
|
|
|
|
|
|
233,4 = |
4,7 10 |
г |
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
0,01 |
1000 |
|
|
|
|
|
|
|
|
|||||||||
|
ω(%) = |
|
4,7 10−7 |
100 =1,8 10−4 % |
|
|
|
|||||||||||||||
|
|
|
|
0,2534 |
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||

Задача № 11. Рассчитать растворимость осадка CaC2O4 в 0,1 М
растворе уксусной кислоты.
KS (CaC2O4 ) = 2,3 10 |
−9 |
; |
Ka (H2C2O4 ) = 5,6 10 |
−2 |
; |
|
|||||||||||||
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|
K |
|
|
(H |
|
C |
|
O |
|
) = 5,4 10 |
−5 |
; K |
|
(CH |
COOH) =1,82 10 |
−5 |
||||
a |
|
2 |
2 |
4 |
|
|
a |
. |
|||||||||||
|
2 |
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Решение. Если осадок представляет собой соль слабой (например,
двухосновной) кислоты, то при добавлении другой кислоты анионы осадка, находящиеся в растворе, будут взаимодействовать с ионами водорода:
MAn (ос) M2+ + An2− |
(1) |
An2− + H+ HAn −
|
|
|
|
|
[H |
+ |
][An |
− |
] |
||
K |
|
(H |
|
An) = |
|
|
|||||
a |
2 |
[HAn |
− |
] |
|
||||||
|
|
|
|
||||||||
|
2 |
|
|
|
|
||||||
HAn − + H+ H2An |
Ka |
(H |
|
An) = |
[H+][HAn−] |
|
|
2 |
H2An |
||||||
|
1 |
|
|
||||
|
|
|
|
|
|||
При этом равновесие реакции (1) сдвигается вправо, и растворимость |
|||||||
осадка увеличивается. |
|
|
|
|
|
|
|
С учетом концентраций всех |
форм, |
в которых кислота H2An |
|||||
присутствует в растворе, |
|
|
|
|
|
|
|
c(An2−) =[An2−] + [HAn−] + [H2An]