Материал: подготовка к контрольной работе 1

Тема «Химические равновесия»
Задача № 1. Вычислить ионную силу раствора, содержащего в 1 л
0,01 моль CaCl2 и 0,1 моль Na2SO4.
Решение. Вычисление ионной силы раствора проводят по формуле:
|
1 |
i |
2 |
|
|
|
I = |
(ci zi |
) , |
(1) |
|||
2 |
|
|||||
|
1 |
|
|
|
||
|
|
|
|
|
||
где сi − молярная концентрация i-го иона; zi |
– заряд i-го иона. |
|||||
I= 0,5 [c(Ca 2+)∙22 + c(Cl−)∙12 + c(Na +)∙12 + c(SO4 2−)∙22 ] =
=0,5 (0,01∙22 +2∙0,01∙12 + 2∙0,1∙12 + 0,1∙22 ) = 0,33 моль/л
I = 0,33 моль/л
Задача № 2. Вычислить коэффициенты активности и активности ионов в 0,0001 М растворе Fe2(SO4)3 .
Решение. На основании формулы (1) вычисляем ионную силу раствора:
I = 0,5 [c(Fe 3+)∙32 + c(SO4 2−)∙22] = 0,5 [0,0001 (2∙32 + 3∙22)] = 0,5 (0,001∙30) =
0,0015 моль/л I = 0,0015 моль/л
Зависимость коэффициента активности иона от ионной силы разбавленного водного раствора электролита c ионной силой ≈ 10−3 М,
выражается формулой Дебая-Хюккеля:
lgγ = − 0,5 z2 
 I
I

На основании вышеприведенной формулы вычисляем коэффициен-
ты активности:
lgγ(Fe3+) =
−0,5∙32 
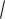 0,0015
0,0015
γ(Fe3+) ≈ 0,67
= − 0,1743
lgγ(SO42−) = − 0,5 · 22 
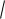
γ(SO42−) ≈
0,0015
0,84
= − 0,0775
Рассчитываем активности по формуле:
a = c∙γ
a(Fe |
3+ |
) = 0,0001 2 |
0,67 |
=1,34 |
10 |
−4 |
||||
|
|
|
|
|||||||
a(SO |
|
|
2− |
) = 0,0001 3 0,84 = 2,52 |
10 |
−4 |
||||
4 |
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
||
Задача № 3. Рассчитайте концентрацию ионов водорода [H+] и рН водных 0,01 M растворов HCl и NaOH.
Решение. 1) HCl – сильная кислота, в водных растворах диссоциирует полностью, поэтому концентрация ионов водорода равна концентрации кислоты:
[H+] = c(HCl)
рН = − lg [H+] = − lg 0,01 = 2
2) NaOH – сильный электролит, в водных растворах диссоциирует полностью, поэтому концентрация гидроксил-ионов равна молярной концентрации щелочи:

[OH −] = c(NaOH)
Используя ионное произведение воды Kw = [H+]∙[OH−] = 10−14,
рассчитываем концентрацию ионов водорода: |
|
||||||||
[H+] = |
KW |
|
= |
10−14 |
=10−12 |
моль/л |
|||
|
|
|
|
||||||
c(NaOH) |
10 |
−2 |
|||||||
|
|
|
|
||||||
|
|
|
|
|
|
|
|||
pH + pOH = 14 pOH = − lg [OH−]
рН = 14 – pOH = 14 + lg c(NaOH) = 14 + lg 0,01 = 12
Задача № 4. Рассчитайте рН 0,01 М раствора муравьиной кислоты НСООН; константа кислотности муравьиной кислоты (Кa) равна 2∙10 −4.
Решение. Муравьиная кислота как слабый электролит в водном растворе подвергается электролитической диссоциации:
HCOOH H + + HCOO−
c константой кислотности
[H+] [HCOO−] Ka = HCOOH
Равновесные концентрации ионов [H+] и [HCOO−] одинаковы, а
равновесную концентрацию муравьиной кислоты [HCOOH] можно принять равной исходной молярной концентрации эквивалента c(1/1НСООН) в растворе, поскольку степень ионизации мала. Поэтому

Кa =
[H |
+ |
2 |
] |
|
|
c(1/ 1HCOOH) |
||
,
a концентрация ионов водорода будет определяться по формуле:
[H+] = 
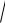 Ka c(1
Ka c(1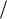 1HCOOH) =
1HCOOH) = 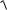
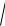 2 10−4 10−2 =
2 10−4 10−2 = 
 2 · 10 −3 моль/л
2 · 10 −3 моль/л
pH = − lg [H+] = 2,85
Задача № 5. Рассчитайте рН 0,1 М раствора гидроксида аммония
NH4OH; константа основности NH4OH Кb = 1,81 · 10 −5.
Решение. Для растворов слабых оснований концентрация ионов OH−
рассчитывается по формуле, приведенной ниже; для самостоятельного вывода формулы используйте рассуждения, аналогичные тем, которые приведены в задаче № 4:
[OH |
− |
] = |
K |
|
|||
|
|
|
b |
c(1/ 1NH |
4 |
OH) = |
1,81 10 |
−5 |
0,1 |
= |
1,81 |
|
|||||||
|
|
|
|
|
|
|
pH = 14 – pOH = 14 + lg [OH−] = 11,85.
· 10−3 моль/л
Задача № 6. Какие растворы называются буферными? Приведите примеры буферных растворов и объясните сущность буферного действия.
Решение. Буферными растворами называют растворы, содержащие одновременно какую-либо слабую кислоту и ее соль или какое-либо слабое основание и его соль, не изменяющие своего рН при умеренном разбавлении их и добавлении к ним небольшого количества сильной кислоты или щелочи.

Для буферных растворов, образованных слабым основанием и его солью, (например, NH4OH + NH4Cl,) концентрация рассчитывается по формуле:
[OH |
−] = K |
|
(NH |
|
OH) |
c(NH |
4 |
OH) |
||
b |
4 |
|
|
|
||||||
|
|
|
|
c(NH |
4 |
Cl) |
||||
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
||
При добавлении к такому раствору небольших растворов сильных кислот и щелочей отдельные компоненты буферной смеси связывают ионы водорода или гидроксила с образованием слабых электролитов, поэтому рН буферных растворов практически не изменяется:
NH4OH + HCl → NH4Cl + H2O
NH4Cl + NaOH → NH4OH + NaCl
Для буферных растворов, образованных слабой кислотой и ее солью
(например, CH3COOH + CH3COONa), концентрация H+-ионов рассчитывается по формуле:
[H+] = K |
|
(CH |
COOH) |
c(CH COOH) |
|
a |
3 |
||||
|
3 |
|
c(CH |
COONa) |
|
|
|
|
|
||
|
|
|
|
3 |
|
Задача № 7. Чему равно значение рН раствора, полученного при смешивании 100 см3 0,1 н раствора CH3COOH и 100 см3 0,1 н раствора
CH3COONa? Ka(CH3COOH) =1,82 · 10 −5 .
Решение. При смешивании получаем буферный раствор, для кото-
рого концентрация ионов водорода рассчитывается по соответствующей формуле. Учитываем также, что при смешивании растворов их исходная