Материал: Патан Серов учебник
Плазморрагия - выход плазмы из кровеносного русла. Следствием плазморрагии является пропитывание плазмой стенки сосуда и окружающих тканей - плазматическое пропитывание. Плазморрагия - одно из проявлений нарушенной сосудистой проницаемости, обеспечивающей в норме транскапиллярный обмен.
Обмен веществ через стенку капилляра осуществляется с помощью механизмов ультрафильтрации, диффузии и микровезикулярного транспорта.
Под ультрафильтрацией понимается проникновение веществ через поры в мембрану под влиянием гидростатического или осмотического давления. При диффузии переход веществ из крови в ткань и из ткани в кровь определяется градиентом концентрации этих веществ по обе стороны стенки капилляра (пассивная диффузия) или с помощью ферментов клеточных мембран - пермеаз (активная диффузия). Микровезикулярный транспорт, микропиноцитоз, или цитопемзис, обеспечивают переход через эндотелиальные клетки любых макромолекул плазмы крови; это - активный метаболический процесс, о чем свидетельствует высокая ферментативная активность микровезикул. Межклеточному пути в транскапиллярном обмене отводится ничтожная роль. Доказано существование органных различий сосудистой проницаемости. К органам с относительно высокой сосудистой проницаемостью относятся печень, селезенка, костный мозг, с относительно низкой сосудистой проницаемостью - сердце, легкие, головной мозг, к органам, занимающим промежуточное положение, - почки, кишечник, эндокринные железы.
При микроскопическом исследовании плазматическое пропитывание стенки артериолы делает ее утолщенной, гомогенной (рис. 58). При крайней степени плазморрагии возникает фибриноидный некроз.
При электронно-микроскопическом исследовании о повышении сосудистой проницаемости свидетельствуют гипервезикуляция, отек или истончение эндотелия, образование в нем фенестр и туннелей, появление широких межклеточных щелей, нарушение целости базальной мембраны. Эти изменения позволяют считать, что при плазморрагии используются как транс-, так и интерэндотелиальные пути.
Механизм развития. Патогенез плазморрагии и плазматического пропитывания определяется двумя основными условиями - повреждением
сосудов микроциркуляторного русла и изменениями констант крови, способствующими повышению сосудистой проницаемости. Повреждение микрососудов связано чаще всего с нервно-сосудистыми нарушениями (спазм), тканевой гипоксией, иммунопатологическими реакциями. Изменения крови, способствующие плазморрагии, сводятся к увеличению содержания в плазме вазоактивных веществ (гистамин, серотонин), естественных антикоагулянтов (гепарин, фибринолизин), грубодисперсных белков, липопротеидов, появлению иммунных комплексов, нарушению реологических свойств. Плазморрагия встречается наиболее часто при гипертонической болезни,
146
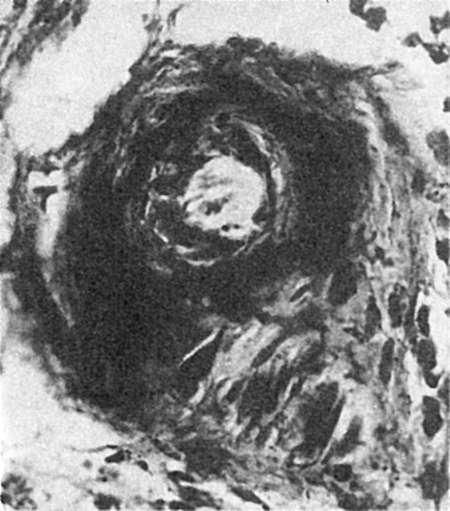
Рис. 58. Плазматическое
пропитывание стенки мелкой артерии (белки плазмы черные)
атеросклерозе, декомпенсированных пороках сердца, инфекционных, инфекционноаллергических и аутоиммунных заболеваниях.
Исход. В исходе плазматического пропитывания развиваются фибриноидный некроз и гиалиноз сосудов.
Значение плазморрагии заключается прежде всего в нарушениях транскапиллярного обмена, ведущих к структурным изменениям органов и тканей.
Стаз
Стаз (от лат. stasis - остановка) - остановка тока крови в сосудах микроциркуляторного русла, главным образом в капиллярах. Остановке тока крови обычно предшествует резкое его замедление, что обозначается какпредстатическое состояние, или предстаз.
Основными особенностями сладж-феномена (от англ. sludge - тина) считают прилипание друг к другу эритроцитов, лейкоцитов или тромбоцитов и нарастание вязкости плазмы, что приводит к затруднению перфузии крови через сосуды микроциркуляторного русла. Сладжфеномен можно считать разновидностью стаза.
147
Механизм развития. В возникновении стаза основное значение имеют изменения реологических свойствкрови, представленные усиленной внутрикапиллярной
агрегацией эритроцитов, что ведет к увеличению сопротивления току крови по капиллярам, замедлению его и остановке. Гемолиз и свертывание крови при стазе не наступают. Развитию внутрикапиллярной агрегации эритроцитов способствуют: изменения капилляров, ведущие к повышению проницаемости их стенок, т.е. плазморрагия; нарушения физико-химических свойств эритроцитов, в частности снижение их поверхностного потенциала; изменения состава белков крови за счет увеличения грубодисперсных фракций; дисциркуляторные расстройства - венозное полнокровие (застойный стаз) или ишемия (ишемический стаз), нарушения иннервации микроциркуляторного русла.
Причиной развития стаза являются дисциркуляторные нарушения. Они могут быть связаны с действием физических (высокая температура, холод) и химических (кислоты, щелочи) факторов, развиваются при инфекционных (малярия, сыпной тиф), инфекционноаллергических и аутоиммунных (ревматические болезни) заболеваниях, болезнях сердца и сосудов (пороки сердца, ишемическая болезнь сердца).
Значение стаза определяется не только его длительностью, но и чувствительностью органа или ткани к кислородному голоданию (головной мозг). Стаз - явление обратимое; состояние после разрешения стаза называется постстатическим. Необратимый стаз ведет к некробиозу и некрозу.
Тромбоз
Тромбоз (от греч. thrombosis - свертывание) - прижизненное свертывание крови в просвете сосуда или в полостях сердца. Образующийся при этом сверток крови называют тромбом.
При свертывании лимфы также говорят о тромбозе и внутрисосудистый сверток лимфы называют тромбом, однако закономерности лимфотромбоза и гемотромбоза различны.
Согласно современному представлению, свертывание крови проходит четыре стадии:
I - протромбокиназа + активаторы -> тромбокиназа (активный тромбопластин);
II - протромбин + Са2+ + тромбокиназа -> тромбин;
III - фибриноген + тромбин -> фибрин-мономер;
IV - фибрин-мономер + фибринстимулирующий фактор -> фибринполимер.
Процесс свертывания крови совершается в виде каскадной реакции (теория «каскада») при последовательной активации белковпредшественников, или факторов свертывания, находящихся в крови или тканях. На этом основании различают внутреннюю
(кровь) и внешнюю (ткань) свертывающие системы. Взаимоотношения внутренней и внешней систем представлены на схеме VIII.
148
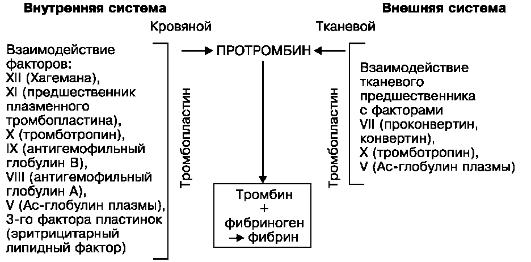
Следует иметь в виду, что, помимо системы свертывания, существует и противосвертывающая система, что обеспечивает регуляцию системы гемостаза - жидкое
состояние крови в сосудистом русле в нормальных условиях. Исходя из этого, тромбоз представляет собой проявление нарушенной регуляции системы гемостаза.
Механизм развития. Тромбообразование складывается из четырех последовательных стадий: агглютинация тромбоцитов, коагуляция фибриногена и образование фибрина, агглютинация эритроцитов, преципитация белков плазмы.
Агглютинации тромбоцитов предшествует выпадение их из тока крови, направленное движение и прилипание (адгезия) к месту повреждения
Схема VIII. Взаимоотношения внутренней и внешней систем свертывания крови (по В.А. Кудряшову)
эндотелиальной выстилки (рис. 59). По-видимому, «травма» тромбоцитов способствует высвобождению липопротеидного комплекса периферической зоны пластинок (гиаломер), который обладает агглютинирующими свойствами. Агглютинация тромбоцитов завершается их дегрануляцией, высвобождением серотонина и тромбопластического фактора пластинок, что ведет к образованию активного тромбопластина и включению последующих фаз свертывания крови.
149
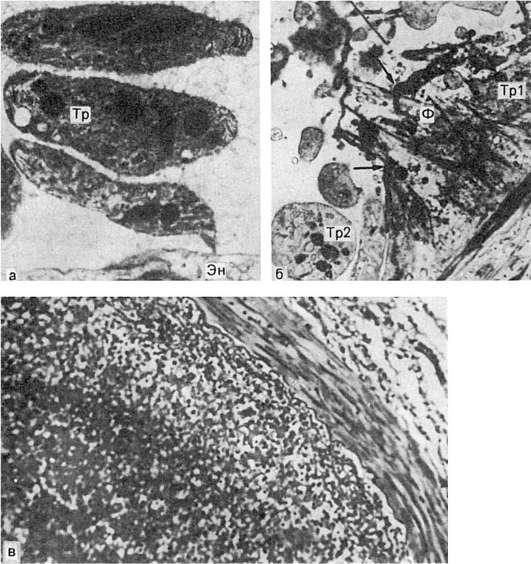
Рис.
59. Морфогенез тромбообразования:
а - первая стадия образования тромба. Небольшие скопления тромбоцитов (Тр) около поврежденной эндотелиальной клетки (Эн). х14 000 (по Ашфорду и Фримену); б - вторая стадия образования тромба. В участке разрушенного эндотелия видны скопления тромбоцитов (Тр1) и фибрина (Ф); Тр2 - неизмененные тромбоциты. х7500 (по Ашфорду и Фримену); в - тромботические массы, состоящие из фибрина, лейкоцитов и агглютинирующихся эритроцитов
Коагуляция фибриногена и образование фибрина (см. рис. 59) связаны с ферментативной реакцией (тромбопластин - тромбин - фибриноген - фибрин), причем матрицей для фибрина становится «оголенная» центральная зона пластинок (грануломер), которая содержит фермент с ретрактильными свойствами (ретрактозим пластинок). Активность ретрактозима, как и серотонина, высвобождающегося при распаде пластинок и обладающего сосудосуживающими свойствами, позволяет «отжать» фибринный сверток, который захватывает лейкоциты, агглютинирующиеся эритроциты и преципитирующие белки плазмы крови (см. рис. 59).
150