Материал: основы проектирования хим произв дворецкий

46Глава 3. ПРОЕКТИРОВАНИЕ ХИМИЧЕСКИХ ПРОИЗВОДСТВ
3)на основании литературно-патентного обзора предварительно выбирают один или несколько альтернативных типов аппаратов для осуществления процесса на данной технологической стадии;
4)окончательный выбор типа аппаратурного оформления делается на основании технико-экономического анализа, а при необходимости (для крупнотоннажных производств) с учетом результатов исследований отраслевого НИИ.
Далее рассмотрим общие принципы анализа и расчета процессов и аппаратов химической технологии.
К одним из важнейших принципов науки о процессах и аппаратах химической технологии относятся теоретические и технологические обобщения и выявление физико-химических аналогий основных процессов.
При исследовании и расчете процессов и аппаратов важно знать кинетические закономерности основных процессов химической технологии.
Кинетика – это учение о механизмах и скоростях процессов, в том числе гидродинамических, тепло- и массообменных. Кинетика является научной основой создания новых и совершенствования действующих аппаратов химической технологии.
По общепринятой классификации, основанной на кинетических закономерностях процессов, различают [13, 14]:
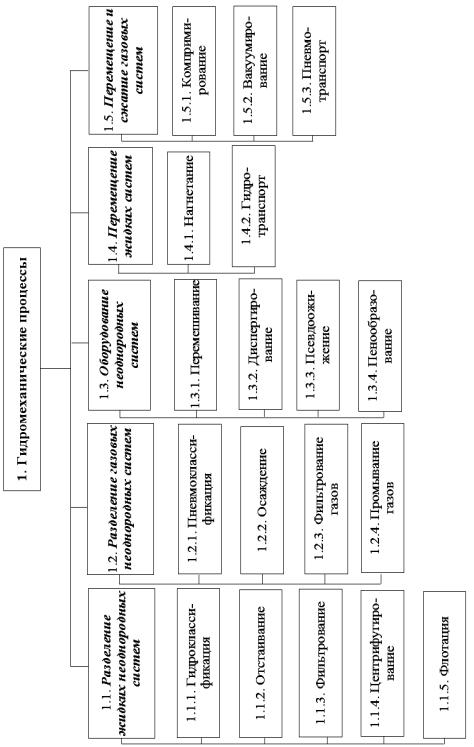
Гидромеханические процессы (рис. 3.4), скорость которых определяется законами гидродинамики:
j |
= |
dV |
= |
p |
= k p, |
(3.12) |
|
Fdτ |
R |
||||||
г |
|
|
1 |
|
|||
|
|
|
|
1 |
|
|
где jг – скорость процесса; V – объем протекающей жидкости; F – площадь сечения аппарата; τ – время; k1 – коэффициент скорости процесса (величина, обратная гидравлическому сопротивлению R1); р – перепад давления (движущая сила процесса).
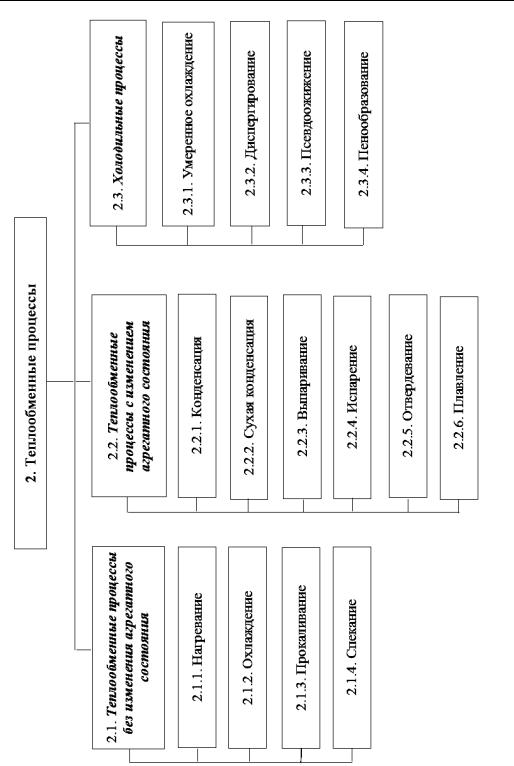
Теплообменные процессы (рис. 3.5), скорость которых определяется законами теплопередачи:
jт = |
dQ |
= |
t |
= k2 |
t, |
(3.13) |
Fdτ |
R |
|||||
|
|
|
2 |
|
|
|
где jт – скорость процесса; Q – количество переданного тепла; F – поверхность теплообмена; τ – время; k2 – коэффициент теплопередачи (величина, обратная термическому сопротивлению R2); t – средняя разность температур между обменивающимися теплом материалами (движущая сила процесса).
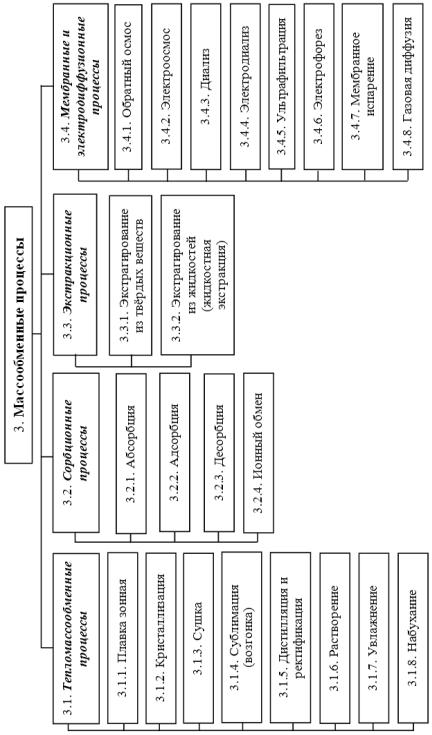
Массообменные (диффузионные) процессы (рис. 3.6), скорость которых определяется скоростью перехода вещества из одной фазы в другую:
j |
= dM |
= |
c |
= k |
|
c, |
(3.14) |
м |
Fdτ |
|
R |
|
3 |
|
|
|
|
|
3 |
|
|
|
|

ОБЩИЕПРИНЦИПЫАНАЛИЗА, РАСЧЕТАИВЫБОРАТЕХНОЛОГИЧЕСКОГООБОРУДОВАНИЯ… 47
где jм – скорость процесса; М – количество вещества, перенесенного из одной фазы в другую; F – поверхность контакта фаз; τ – время; k3 – коэффициент массопередачи (величина, обратная диффузионному сопротивлению R3); с – разность между равновесной и рабочей концентрациями вещества в фазах (движущая сила процесса).
Механические процессы (рис. 3.7), скорость которых определяется законами физики твердого тела.
Химические процессы, связанные с превращением веществ и изменением их химических свойств. Скорость этих процессов определяется закономерностями химической кинетики:
jх = |
dM |
= k4 f (c), |
(3.15) |
|
Vpdτ |
||||
|
|
|
где jх – скорость процесса; М – количество прореагировавшего в химическом процессе вещества; V – объем реактора; τ – время; k4 – коэффициент скорости химического процесса; f(с) – движущая сила процесса, которая является функцией концентраций реагирующих веществ.
Биохимические процессы, связанные с синтезом веществ и осуществляемые под воздействием и при непосредственном участии живых микроорганизмов и выделенных из них ферментов (биологических катализаторов). Скорость биохимических процессов, как и в предыдущем случае, определяется скоростью роста культуры от концентрации одного или нескольких наиболее важных компонентов среды, обеспечивающих основу метаболизма. Эти компоненты получили название лимитирующих субстратов.
Приведенная классификационная система основных процессов химической технологии удобна тем, что позволяет устанавливать единую номенклатуру типовой аппаратуры, используемой для этих процессов. Так, например, при классификации химических реакторов можно руководствоваться несколькими классификационными признаками:
1)способом организации процесса;
2)фазовым составом смеси;
3)гидродинамическими условиями проведения процесса в реакторе;
4)теплообменными условиями процесса в реакторе;
5)временными изменениями процесса;
6)конструктивными особенностями реактора;
7)агрегатным состоянием фазы и др.
По первому признаку (по способу подвода сырья и отвода продукта) различают периодические, полупериодические (полунепрерывные) непрерывно действующие химические аппараты-реакторы.
По второму признаку для проведения гетерогенных процессов выделяются системы газ – жидкость, жидкость – твердое и газ – твердое; для проведения гомогенных процессов – газо- и жидкофазные; отдельно рассматриваются реакторы для гетеро-каталитических процессов.
48 |
Глава 3. ПРОЕКТИРОВАНИЕ ХИМИЧЕСКИХ ПРОИЗВОДСТВ |
|
|
Рис. 3.4. Классификация гидромеханических процессов
ОБЩИЕПРИНЦИПЫАНАЛИЗА, РАСЧЕТАИВЫБОРАТЕХНОЛОГИЧЕСКОГООБОРУДОВАНИЯ… 49
Рис. 3.5. Классификация теплообменных процессов
50 |
Глава 3. ПРОЕКТИРОВАНИЕ ХИМИЧЕСКИХ ПРОИЗВОДСТВ |
|
|
Рис. 3.6. Классификация массообменных процессов