Материал: Основные положения статистической физики
![]() .
.
Внутренняя
энергия: ![]() т.е. это среднее значение микроскопической внутренней
энергии
т.е. это среднее значение микроскопической внутренней
энергии
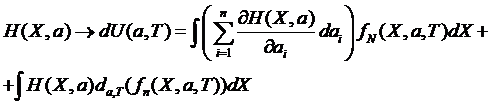 (*),
(*),
где
![]() - дифференциал по а и Т.
- дифференциал по а и Т.
Введем
микроскопические (зависит от Х) силы, соответствующие обобщенным координатам ![]() :
:
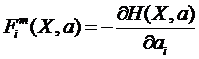 .
.
Отметим,
что размерность этих сил может быть различной в зависимости от параметров ![]() .
.
Термодинамические
силы ![]() определяются как средние от микроскопических сил:
определяются как средние от микроскопических сил:
![]() .
.
Работа
в термодинамике может быть определена как:
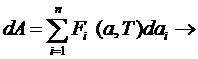
первый
член (*) равен работе термодинамических сил
![]()
![]() (**).
(**).
Вполне понятно, что работа связана с изменением внешних параметров, поскольку они не дают вклада в кинетическую энергию, то должны дать вклад в потенциальную.
То
есть ![]() определяется изменением функции распределения
вследствие изменения термодинамических переменных а, Т.
определяется изменением функции распределения
вследствие изменения термодинамических переменных а, Т.
Из
условия нормировки:
![]()
![]() . (***)
. (***)
В
выражении (**) разделим и умножим на ![]() и вычтем
выражение
и вычтем
выражение
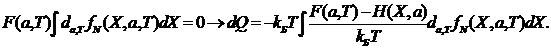
![]() с учетом
с учетом
![]() - вынесем за интеграл
- вынесем за интеграл ![]() →(***).
→(***).
![]() .
.
Из
определения энтропии в термодинамике: ![]() .
.
Если
приравнять величину ![]() в каноническом распределении Гиббса к
термодинамической температуре, то, сравнивая
в каноническом распределении Гиббса к
термодинамической температуре, то, сравнивая ![]() ,
получим:
,
получим:
![]() ,
,
где
![]() - константа, которая может быть определена только в
квантовой статистической теории. Или:
- константа, которая может быть определена только в
квантовой статистической теории. Или: ![]() .
.
Из
термодинамики свободная энергия определяется как:
![]() .
.
Таким
образом, действительно функция ![]() в
каноническом распределении Гиббса совпадает со свободной энергией, определенной
в термодинамике. Зная сводную энергию, можно вычислить основные
термодинамические параметры:
в
каноническом распределении Гиббса совпадает со свободной энергией, определенной
в термодинамике. Зная сводную энергию, можно вычислить основные
термодинамические параметры:
![]() .
.
Отсюда:
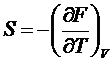 ,
, 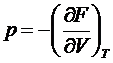 .
.
С
другой стороны можно определить теплоемкость:
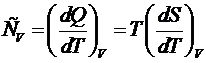 .
.
Таким
образом, основной алгоритм, на котором основана равновесная СФ, выглядит так:
![]() .
.
5. Энтропия - мера неопределенности при статистическом описании.
Статистическое обоснование третьего начала термодинамики
Определение
энтропии получено для ![]() - канонического распределения Гиббса. Для
произвольной функции распределения
- канонического распределения Гиббса. Для
произвольной функции распределения ![]() введем
энтропию (опуская
введем
энтропию (опуская ![]() ):
):
![]()
(квадратные
скобки означают, что величина ![]() определена
для совокупности случайной величин Х),
определена
для совокупности случайной величин Х),
![]() .
.
Это
для непрерывной переменной. Во многих случаях (в частности, в квантовой теории)
используются функции распределения случайных величин, принимающих дискретный
ряд значений n (например, набор квантовых чисел). Обозначим
соответствующую функцию ![]() . Тогда:
. Тогда: ![]() .
.
Тогда
энтропия для дискретного распределения может быть представлена в виде
![]() .
.
Свойства
![]() и
и ![]()
1.
Если ![]() при
при ![]() , и нулю
для всех остальных значений, то
, и нулю
для всех остальных значений, то ![]() . Это
соответствует нулевой неопределенности задания состояния системы.
. Это
соответствует нулевой неопределенности задания состояния системы.
. Если
число возможных значений дискретной переменной ![]() равно
равно ![]() и все возможные значения равновероятны:
и все возможные значения равновероятны: ![]() ,
, ![]() ,
, 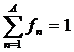 (- доказать).
(- доказать).
То
можно показать, что ![]() в этом случае максимальна и равна:
в этом случае максимальна и равна:
![]() .
.
В таком виде формула для энтропии была получена еще Больцманом.
Это соответствует полному хаосу (максимальной неопределенности) задания состояния системы.
Для
энтропии непрерывных величин ![]() результаты
аналогичны.
результаты
аналогичны.
Для
сравнения найдем энтропию, соответствующую квантовому микроканоническому
распределению Гиббса:
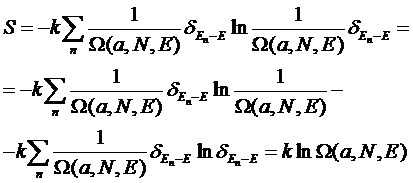 .
.
Второе
слагаемое равно нулю, поскольку содержит 0ln0 или 1ln1. Таким образом, мы снова
получаем формулу для энтропии в виде:
![]() .
.
Следовательно,
энтропия может служить мерой неопределенности при статистическом описании
процессов в макротелах. Такое определение энтропии можно использовать и для
исследования неравновесных процессов, когда ![]()
![]() .
.
Третье начало термодинамики с точки зрения статистической физики
На
основе анализа экспериментов Вальтер Нернст (1906 г.) пришел к выводу, что
разность энтропий ![]() соответствующих любым двум модификациям вещества
стремиться к нулю при приближении к нулю абсолютной температуры:
соответствующих любым двум модификациям вещества
стремиться к нулю при приближении к нулю абсолютной температуры: ![]() .
.
Позднее
Планк сформулировал Результат Нернста в еще более определенной форме: ![]() при
при ![]() -
теорема Нернста (третье начало).
-
теорема Нернста (третье начало).
Из
нее следует ряд термодинамических следствий. Обратимся к квантовому
каноническому распределению Гиббса. Из него следует выражение для энтропии:
![]()
![]() .
.
Из квантового канонического распределения Гиббса следует, что наиболее вероятным является квантовое состояние системы с наименьшим возможным значением энергии - основное состояние.
В
равновесном состоянии функция распределения ![]() максимальна
для основного состояния. Если через
максимальна
для основного состояния. Если через ![]() обозначить
разность энергий основного и возбужденного состояний, то при температуре
обозначить
разность энергий основного и возбужденного состояний, то при температуре ![]() вероятность функции
вероятность функции ![]() для
основного состояния будет близка к единице, а при Т=0:
для
основного состояния будет близка к единице, а при Т=0:
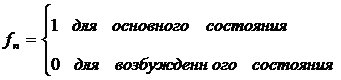
Эта функция удовлетворяет условию нормировки.
Действительно,
записывая условие нормировки в виде:
![]() ,
,
получим
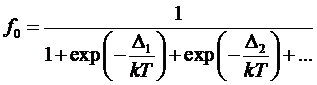 .
.
При
таком распределении все члены выражения для ![]() равны
нулю
равны
нулю ![]() при
при ![]() .
.
Таким образом, третье начало с точки зрения статистической физики можно сформулировать так:
при
![]() система находится только в основном состоянии,
поэтому неопределенность задания состояния равна нулю. Этому соответствует
равенство нулю энтропии, которая является мерой неопределенности состояния при
статистическом описании.
система находится только в основном состоянии,
поэтому неопределенность задания состояния равна нулю. Этому соответствует
равенство нулю энтропии, которая является мерой неопределенности состояния при
статистическом описании.
.
Возрастание энтропии в процессе эволюции. Теорема Гиббса
Обозначим
через ![]() распределение, не совпадающее в общем случае с
распределением Гиббса.
распределение, не совпадающее в общем случае с
распределением Гиббса.
![]() .
.
Кроме
того, внутренняя энергия, вычисленная с помощью ![]() одинакова
(
одинакова
(![]() - неизменные).
- неизменные).
![]() .
.
В
остальном ![]() -произвольная.
-произвольная.
Обозначим
через ![]() энтропии:
энтропии: ![]() ,
, ![]() , и покажем, что
, и покажем, что ![]() . Т.е.
энтропия, отвечающая каноническому распределению Гиббса, максимальна (равенство
имеет место, если
. Т.е.
энтропия, отвечающая каноническому распределению Гиббса, максимальна (равенство
имеет место, если ![]() ).
).
Представим
![]() в виде:
в виде:
![]() ,
,
где
![]() -произвольная (вспомогательная) функция, определяемая
-произвольная (вспомогательная) функция, определяемая ![]() . При этом должно выполняться условие нормировки:
. При этом должно выполняться условие нормировки:
![]() .
.
Найдем
разность энтропий:
![]() .
.
Второй
и четвертый члены, содержащие Н, сокращаются (вследствие одинаковости U).
Тогда получим:
![]() (*)
(*)
![]() .
.
Тогда
получим
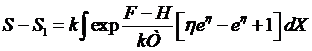 .
.
Первый множитель под интегралом положителен, т.к. это экспонента.
Но
второй множитель так же положителен: ![]() . Легко
показать, что он имеет минимум, равный нулю при
. Легко
показать, что он имеет минимум, равный нулю при ![]() .
.
Таким
образом, получим: ![]() . Равенство имеет место, если
. Равенство имеет место, если ![]()
![]() .
.
Можно
трактовать это и иначе: вместо ![]() можно
выбрать
можно
выбрать ![]() , где
, где ![]() - любой
момент времени, отвечающий эволюции к равновесному состоянию. Тогда
- любой
момент времени, отвечающий эволюции к равновесному состоянию. Тогда ![]() В замкнутой системе в ходе процесса эволюции к
равновесному состоянию энтропия достигает максимального значения в равновесном
состоянии.
В замкнутой системе в ходе процесса эволюции к
равновесному состоянию энтропия достигает максимального значения в равновесном
состоянии. ![]() второй закон для необратимых процессов в замкнутой
системе.
второй закон для необратимых процессов в замкнутой
системе.
Как
найти ![]()
![]() статистическая теория неравновесных процессов.
статистическая теория неравновесных процессов.
.
Теорема о равнораспределении
Рассмотрим
классическую систему, и покажем, что на каждую степень свободы в такой системе
приходится энергия, равная kT/2. То есть, нам нужно доказать равенство:
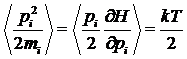 .
.
Используем
каноническое распределение Гиббса:
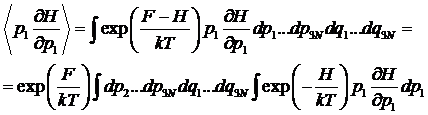 .
.
Интеграл
по p1 можно взять по частям:
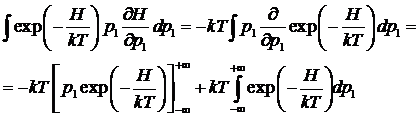 .
.
Слагаемое
в квадратных скобках равно нулю, поскольку экспонента стремится к нулю быстрее,
чем степенная функция. Поэтому
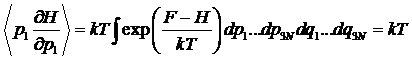 ,
,
поскольку интеграл в силу условия нормировки равен единице. Значение i = 1 мы взяли произвольно. Такое же выражение можно получить для любого i.
Для
координат можно получить аналогичное выражение:
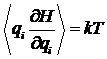 .
.
Важно
только то, что при возрастании координат H тоже
возрастает достаточно быстро. Например, для гармонического осциллятора имеем:
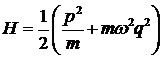 ,
, 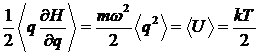 .
.
Рассмотрение вращательных степеней свободы проводится аналогично.
Таким образом, можно сделать общий вывод: в классической механике на каждую степень свободы молекулы приходится энергия, равная kT/2. Однако, такой вывод неверен в квантовой механике.