Материал: Основные положения статистической физики
) Система
не замкнута - возможен обмен энергией. В этом случае нельзя найти ![]() , она будет зависеть от обобщенных координат и
импульсов частиц окружающих тел. Это оказывается возможным, если энергия
взаимодействия рассматриваемой системы с окружающими телами
, она будет зависеть от обобщенных координат и
импульсов частиц окружающих тел. Это оказывается возможным, если энергия
взаимодействия рассматриваемой системы с окружающими телами ![]() .
.
При
этом условии функция распределения микросостояний ![]() зависит от средней интенсивности теплового движения
окружающих тел, которую характеризуют температурой Т окружающих тел:
зависит от средней интенсивности теплового движения
окружающих тел, которую характеризуют температурой Т окружающих тел: ![]() .
.
Температура
также играет особую роль. Она не имеет (в отличие от а) аналога в механике: ![]() (не зависит от Т).
(не зависит от Т).
В
состоянии статистического равновесия ![]() не зависит
от времени, неизменны и все внутренние параметры. В термодинамике такое
состояние называют состоянием термодинамического равновесия. Понятия
статистического и термодинамического равновесия эквивалентны.
не зависит
от времени, неизменны и все внутренние параметры. В термодинамике такое
состояние называют состоянием термодинамического равновесия. Понятия
статистического и термодинамического равновесия эквивалентны.
Функция распределения микроскопической изолированной системы - микроканоническое распределение Гиббса
Случай
энергетически изолированной системы. Найдем вид функции распределения ![]() для этого случая.
для этого случая.
Существенную
роль при нахождении при функции распределения играют лишь интегралы движения ![]() - энергия,
- энергия, ![]() -
импульс системы и
-
импульс системы и ![]() - момент импульса. Лишь они являются контролируемыми.
- момент импульса. Лишь они являются контролируемыми.
Гамильтониану в механике отводится особая роль, т.к. именно функцией Гамильтона определяется вид уравнения движения частиц. Сохранение полного импульса и момента импульса системы при этом является следствием уравнений движения.
Поэтому
выделяют именно такие решения уравнения Лиувилля, когда зависимость ![]() проявляется лишь через гамильтониан
проявляется лишь через гамильтониан ![]() :
:
![]() .
.
Так
как ![]() ,
, ![]() .
.
Из
всех возможных значений Х (совокупность координат и импульсов всех частиц
системы) выделяются те, которые совместимы с условием ![]() . Константу С можно найти из условия нормировки:
. Константу С можно найти из условия нормировки:
![]() ,
,
где
![]() - площадь гиперповерхности в фазовом пространстве
- площадь гиперповерхности в фазовом пространстве ![]() , выделяемой условием постоянства энергии.
, выделяемой условием постоянства энергии.
Т.е.
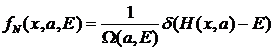 - микроканоническое распределение Гиббса.
- микроканоническое распределение Гиббса.
В
квантовой теории равновесного состояния, так же существует микроканоническое
распределение Гиббса. Введем обозначения: ![]() - полный
набор квантовых чисел, характеризующих микросостояние системы частиц,
- полный
набор квантовых чисел, характеризующих микросостояние системы частиц, ![]() - соответствующие допустимые значения энергии. Их
можно найти, решая стационарное уравнение для волновой функции
- соответствующие допустимые значения энергии. Их
можно найти, решая стационарное уравнение для волновой функции ![]() рассматриваемой системы.
рассматриваемой системы.
Функция
распределения микросостояний в таком случае будет представлять собой
вероятность для системы находиться в определенном состоянии: ![]() .
.
Квантовое
микроканоническое распределение Гиббса может быть записано в виде:
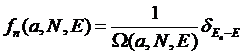 ,
,
где
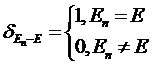 - символ Кронекера,
- символ Кронекера, ![]() - из
нормировки:
- из
нормировки: ![]() - число микросостояний с заданным значением энергии
(а так же
- число микросостояний с заданным значением энергии
(а так же ![]() ). Она называется статистическим весом.
). Она называется статистическим весом.
Из
определения ![]() все состояния удовлетворяющие условию
все состояния удовлетворяющие условию ![]() имеют одинаковою вероятность, равную
имеют одинаковою вероятность, равную ![]() . Таким образом, в основе квантового
микроканонического распределения Гиббса лежит принцип равных априорных
вероятностей.
. Таким образом, в основе квантового
микроканонического распределения Гиббса лежит принцип равных априорных
вероятностей.
Функция распределения микросостояний системы в термостате - каноническое распределение Гиббса.
Рассмотрим
теперь систему, обменивающуюся энергией с окружающими телами. Этому подходу с
термодинамической точки зрения соответствует система, окруженная очень большим
термостатом с температурой T. Для большой системы (наша система + термостат) можно
использовать микроканоническое распределение, поскольку такая система может
считаться изолированной. Будем полагать, что рассматриваемая система составляет
малую, но макроскопическую ![]() часть
большей системы с температурой Т и числом частиц в ней
часть
большей системы с температурой Т и числом частиц в ней ![]() . То есть выполняется равенство (
. То есть выполняется равенство (![]() >>
>>![]() )
)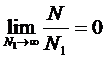 .
.
Будем
обозначать переменные нашей системы через X, а переменные
термостата через X1.
Тогда
для всей системы запишем микроканоническое распределение:
![]() .
.
Нас
будет интересовать вероятность состояния системы из N частиц при
любых возможных состояниях термостата. Эту вероятность можно найти,
проинтегрировав это уравнение по состояниям термостата
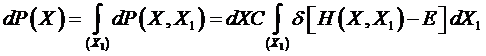 .
.
Функция
Гамильтона системы и термостата может быть представлена в виде
![]() .
.
Будем пренебрегать энергией взаимодействия между системой и термостатом по сравнению, как с энергией системы, так и с энергией термостата. Это можно сделать, поскольку энергию взаимодействия для макросистемы пропорциональна площади ее поверхности, в то время как энергия системы пропорциональна ее объему. Однако пренебрежение энергией взаимодействия по сравнению с энергией системы не означает, что оно равно нулю, в противном случае постановка задачи теряет смысл.
Таким
образом, распределение вероятностей для рассматриваемой системы можно
представить в виде
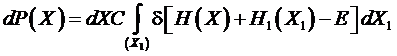 .
.
Перейдем
к интегрированию по энергии термостата
![]() ,
,
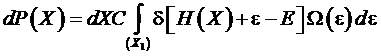 .
.
Отсюда,
воспользовавшись свойством d-функции
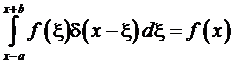 ,
,
Получим
![]() .
.
Будем в дальнейшем переходить к предельному случаю, когда термостат очень велик. Рассмотрим частный случай, когда термостат представляет собой идеальный газ с N1 частицами с массой m каждая.
Найдем
величину ![]() , которая представляет собой величину
, которая представляет собой величину
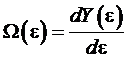 ,
,
где
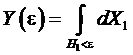 представляет собой объем фазового пространства,
заключенного внутри гиперповерхности
представляет собой объем фазового пространства,
заключенного внутри гиперповерхности ![]() . Тогда
. Тогда 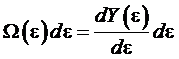 представляет собой объем гипершарового слоя (сравните
с выражением для трехмерного пространства
представляет собой объем гипершарового слоя (сравните
с выражением для трехмерного пространства 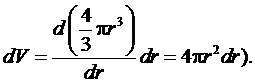
Для
идеального газа область интегрирования дается условием
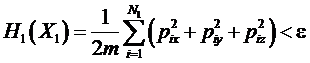 .
.
В
результате интегрирования в указанных границах получаем объем 3N1-мерного
шара с радиусом![]() , который будет равен
, который будет равен ![]() . Таким
образом, имеем
. Таким
образом, имеем
Откуда
имеем
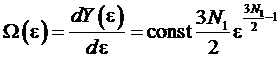 .
.
Таким
образом, для распределения вероятностей имеем
![]() .
.
Перейдем
теперь к пределу N1®¥ , однако, предполагая, что отношение 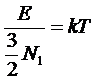 остается постоянным (так называемый термодинамический
предел). Тогда получим
остается постоянным (так называемый термодинамический
предел). Тогда получим
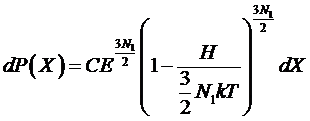 .
.
Принимая
во внимание, что
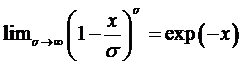 ,
,
получим
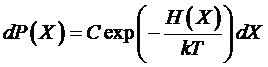 .
.
Тогда
функция распределения системы в термостате может быть записана в виде
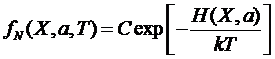 ,
,
где
С находится из условия нормировки:
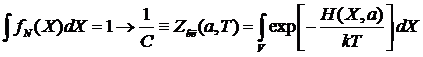 .
.
Функция
![]() называется классическим статистическим интегралом.
Таким образом, функция распределения системы в термостате может быть
представлена в виде:
называется классическим статистическим интегралом.
Таким образом, функция распределения системы в термостате может быть
представлена в виде:
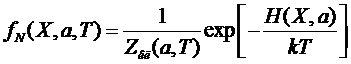
это и есть каноническое распределение Гиббса (1901 г.).
В этом распределении Т характеризует среднюю интенсивность теплового движения - абсолютную температуру частиц окружающей среды.
Другая
форма записи распределения Гиббса
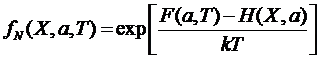 ,
,
![]() .
.
Далее
мы увидим, что![]() совпадает со свободной энергией из термодинамики
(энергия Гельмгольца).
совпадает со свободной энергией из термодинамики
(энергия Гельмгольца).
При
определении ![]() считались различными микроскопическими состояния,
отличающиеся лишь перестановкой отдельных частиц. Это означает, что мы в
состоянии следить за каждой частицей. Однако такое предположение приводит к
парадоксу.
считались различными микроскопическими состояния,
отличающиеся лишь перестановкой отдельных частиц. Это означает, что мы в
состоянии следить за каждой частицей. Однако такое предположение приводит к
парадоксу.
Выражение
для квантового канонического распределения Гиббса, может быть записано по
аналогии с классическим:
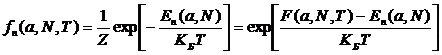 ,
,
![]() -
статистическая сумма:
-
статистическая сумма: 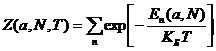 .
.
Она
является безразмерным аналогом статистического интеграла. Тогда свободная
энергия может быть представлена в виде:
![]() .
.
Рассмотрим
теперь систему, находящуюся в термостате и способную обмениваться энергией и
частицами с окружением. Вывод функции распределения Гиббса для этого случая во
многом аналогичен выводу канонического распределения. Для квантового случая
распределение имеет вид:
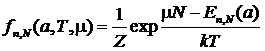
это распределение называется Большое каноническое распределение Гиббса. Здесь μ - химический потенциал системы, который характеризует изменение термодинамических потенциалов при изменении числа частиц в системе на единицу.
Z - из условия
нормировки:
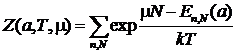 .
.
Здесь суммирование идет не только по квадратным числам, но и по всем возможным значениям числа частиц.
Другая
форма записи: введем функцию ![]() , но так
как ранее получено
, но так
как ранее получено 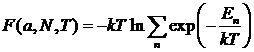 из термодинамики
из термодинамики ![]() , где
, где ![]() - большой термодинамический потенциал. В результате
получим
- большой термодинамический потенциал. В результате
получим
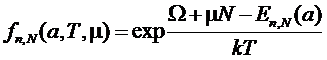 .
.
Здесь
![]() - среднее значение числа частиц.
- среднее значение числа частиц.
Классическое
распределение аналогично.
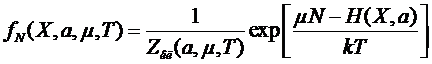 .
.
Распределения Максвелла и Больцмана
Каноническое
распределение Гиббса устанавливает (при заданной ![]() ) явный
вид функции распределения значений всех координат и импульсов частиц (6N-переменных).
Но такая функция
) явный
вид функции распределения значений всех координат и импульсов частиц (6N-переменных).
Но такая функция ![]() очень сложна. Часто достаточно более простых функций.
очень сложна. Часто достаточно более простых функций.
Распределение
Максвелла для идеального одноатомного газа. Каждую молекулу газа мы можем
считать «рассматриваемой системой», принадлежащими к термостату. Поэтому
вероятность какой-либо молекуле иметь импульсы в заданных промежутках ![]() дается каноническим распределением Гиббса:
дается каноническим распределением Гиббса: 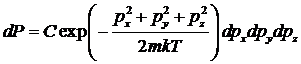 .
.
Заменяя
импульсы скоростями, и используя условия нормировки, получим
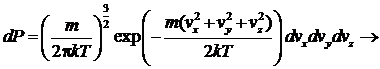
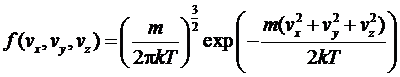 -
функция распределения Максвелла по компонентам скорости. Легко получить
распределение и по модулю.
-
функция распределения Максвелла по компонентам скорости. Легко получить
распределение и по модулю.
В
любой системе, энергия которой равна сумме энергий отдельных частиц имеет место
выражение, аналогичное максвелловскому. Это распределение Максвелла-Больцмана.
Опять будем считать, что «системой» является одна какая-либо частица, остальные
же играют роль термостата. Тогда вероятность состояния этой избранной частицы
при любом состоянии остальных дается каноническим распределением: 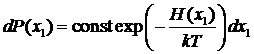 ,
, ![]() . По
остальным величинам
. По
остальным величинам![]() …
…![]() проинтегрировали
проинтегрировали
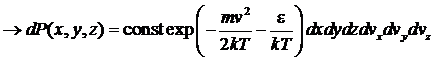 .
.
4. Первое начало термодинамики с точки зрения статистической физики.
Статистическое определение энтропии
Первое начало термодинамики для бесконечно малых величин может быть
записано в виде: