Материал: Общая физика_под ред. Белокопытова_2016 -506с
Из (13.1) и (13.2) получаем
cуд p(m1 + m2 ) = cуд p1m1 + cуд p2m2 ,
откуда
c |
|
= c |
|
|
|
m1 |
|
+ c |
|
|
|
m2 |
|
(13.3) |
уд p |
уд p1 |
--------------------- |
уд p2 |
--------------------- . |
||||||||||
|
|
m |
1 |
+ m |
2 |
|
m |
1 |
+ m |
2 |
|
|||
|
|
|
|
|
|
|
|
|
|
|
||||
Аналогично получаем выражение для удельной теплоемкости смеси в изохорном процессе:
c |
|
= c |
|
|
m1 |
|
+ c |
|
|
|
m2 |
|
(13.4) |
уд V |
уд V 1 m-------------------- |
|
+ m |
- |
уд V 2 |
--------------------- . |
|||||||
|
|
1 |
2 |
|
m |
1 |
+ m |
2 |
|
||||
|
|
|
|
|
|
|
|
|
|
||||
Учтем, что из соотношений (10.8) и (10.10) следуют выражения для удельных теплоемкостей идеального газа при постоянном объеме и постоянном давлении:
|
|
|
|
|
i |
R |
|
|
|
|
|
|
|
|
|
i + 2 |
|
R |
|
|
|
|
|
|
|
|
|
|
c |
уд V = |
---- |
--- |
, |
|
cуд p |
= |
|
----------- |
--- |
|
|
|
|
|
|
|
|||||||
|
|
|
2 μ |
|
|
2 μ . |
|
|
|
|
||||||||||||||||
Для смеси получаем: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
R |
|
|
|
|
|
|
|
i1 |
|
|
|
i |
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
cуд V |
= ----------------------------- |
|
|
|
|
|
|
|
|
------ |
m1 |
+ |
------- |
m2 |
|
; |
|
|
(13.5) |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
2(m1 |
+ m2) |
|
|
|
μ1 |
|
|
|
μ |
2 |
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
c |
|
= |
R |
|
|
|
|
|
i |
1 |
+ 2 |
m |
|
|
i2 |
+ 2 |
|
|
|
|
. |
(13.6) |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
уд p |
2-----------------------------(m1 + m2) |
|
|
-------------- |
1 |
+ -------------- m |
2 |
|
||||||||||||||||||
|
|
|
|
|
|
|
μ1 |
|
|
|
μ 2 |
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
Поскольку неон — одноатомный газ, то i1 = 3; так как водород — двухатомный газ, то i2 = 5. Подстановка числовых данных задачи дает:
cуд V = 2,58æ103 Дж/(кгæК); cуд p = 3,76æ103 Дж/(кгæК).
Пример 13.3. Кислород находится в сосуде объемом V1 при давлении p1 и температуре T1. В некотором политропном процессе его
объем увеличивается в 2 раза, а давление падает в 4 раза. Определите показатель политропы в данном процессе, массу кислорода, конечную температуру, удельную теплоемкость кислорода в данном процессе, изменение внутренней энергии газа, количество теплоты, сообщаемой газу (или отдаваемой газом) в этом процессе.
В соответствии с уравнением политропного процесса (10.13) можно записать: p1V1n = p2V2n , где n – показатель политропы. Тогда
166
n |
1 |
p1(2V1 ) |
n |
|
|
|
|
|
|
||
p1V1 = |
---- |
|
, откуда получаем n = 2. Поэтому данный поли- |
||||||||
4 |
|
||||||||||
тропный процесс описывается уравнением |
|
|
|||||||||
|
|
|
|
|
|
|
pV 2 = const . |
|
(13.7) |
||
|
|
|
|
|
|
|
|
|
m |
|
|
Массу газа определим из уравнения состояния p1V1 = |
--- |
RT1 : |
|||||||||
μ |
|||||||||||
|
|
|
|
|
|
|
|
p1V1μ |
|
|
|
|
|
|
|
|
|
|
m = |
---------------- |
|
|
|
|
|
|
|
|
|
|
RT1 . |
|
(13.8) |
||
Конечную |
температуру |
газа |
найдем из уравнения |
состояния |
|||||||
|
m |
|
|
|
|
p2V2μ |
|
|
|
|
|
p2V2 = |
--- |
RT2 |
: T2 |
= |
---------------- |
. Подставляя сюда p2 = p1 / 4, |
V2 = 2V1 и |
||||
μ |
mR |
||||||||||
|
|
|
|
|
|
|
|
|
|||
(13.8), получаем |
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
|
|
|
T2 = |
---- |
|
(13.9) |
|
|
|
|
|
|
|
|
2 T1 . |
|
|||
Поскольку в соответствии с (10.14) молярная теплоемкость газа в политропном процессе связана с показателем политропы соотношением
c |
|
= c |
|
R |
, |
(13.10) |
m |
mV |
– ------------ |
||||
|
|
n – 1 |
|
|
а удельная теплоемкость газа связана с молярной теплоемкостью
газа выражением c |
|
= c |
|
/ μ, то c |
|
= c |
|
R |
. Учтем, что |
уд |
m |
уд |
уд V |
– --------------------- |
|||||
|
|
|
|
μ(n – 1) |
|
||||
|
|
|
|
|
|
|
|
|
|
i R |
|
|
|
|
|
|
c |
---- --- |
|
|
|
|
|
|
уд V = 2 μ , число степеней свободы молекулы кислорода i = 5 и в |
|||||||
данном процессе n = 2. Тогда |
|
|
|
|
|
|
|
|
|
5 R |
R |
3 |
R |
|
|
|
cуд = |
---- --- |
--- |
---- |
--- |
|
(13.11) |
|
2 μ |
– μ |
= 2 |
μ . |
|
||
|
Изменение внутренней энергии |
газа |
определим из |
формулы |
|||
|
|
|
|
|
|
1 |
|
(10.5). В нашем случае i = 5, |
T = T2 – T1 = – |
---- |
|
||||
2 T1 , а масса газа т |
|||||||
определена соотношением (13.8). Окончательно получаем: |
|
||||||
|
|
|
5 |
|
|
|
|
|
U = – |
---- |
|
|
|
(13.12) |
|
|
4 p1V1 . |
|
|
||||
Количество теплоты, получаемое (отдаваемое) газом определяется выражением Q = cуд m T. Подставим сюда (13.8) и (13.11), получим:
|
3 |
R |
p |
1V1μ |
|
|
1 |
|
|
3 |
|
|
|
---- --- |
---------------- |
|
---- |
|
---- |
|
|
||||
Q = |
2 |
μ |
|
RT1 |
|
– |
2 |
T1 |
= – |
4 |
p1V1 . |
(13.13) |
Знак « – » в выражении (13.13) показывает, что в данном политропном процессе количество теплоты отводится от газа.
167
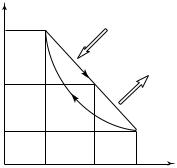
Пример 13.4. Определите КПД цикла, представленного на рис. 13.1, если он совершается одним молем идеального одноатомного газа. Процесс 1-2 описывается линейной зависимостью p(V ), процесс 2-1 — адиабатный. Известны объемы газа в начальном и конечном состояниях V1 и V2 , а также температура газа в начальном
состоянии T1.
Если предположить, что в процессе 1-2 к газу подводится количество теплоты Q12 , то, в соответствии с выражением (11.3), КПД
заданного цикла
η = 1 – |
|
Q21 |
|
|
|
------------ |
|
= 1 , |
|
|
Q12 |
|||
поскольку в адиабатном процессе Q21 = 0. Этот вывод противоречит
второму началу термодинамики, согласно которому КПД любого цикла всегда меньше единицы. Следовательно, предположение о том, что на протяжении всего процесса 1-2 к газу подводится некоторое количество теплоты, неверно. На участке 1-0 количество теплоты Q10 подводится к газу, а на участке 0-2 некоторое количество
теплоты Q02 должно отводиться от газа (рис. 13.1). В этом случае
противоречие со вторым началом термодинамики пропадает, и КПД цикла может быть рассчитан по известным соотношениям (11.2) или (11.3).
Определим объем V0. Для этого рассмотрим элементарный процесс на участке 1-2 вблизи точки 0. Запишем уравнение первого начала термодинамики для 1 моля: δQ = cmV dT + p dV , где cmV —
p |
|
|
|
|
p1 |
1 |
Q1 |
Подвод тепла |
|
|
|
|||
|
|
|
||
|
|
|
Q2 |
|
p0 |
|
0 |
|
|
|
|
|
|
|
|
|
|
Отвод тепла |
|
p2 |
|
|
2 |
|
|
|
|
|
|
0 |
V1 |
V0 |
V2 |
V |
|
|
Рис. 13. 1 |
|
|
168
молярная теплоемкость газа в изохорном процессе. Так как δQ = 0 в окрестности точки 0 с объемом V0, то
(cmV dT + p dV) |
|
= 0 . |
(13.14) |
|
|||
|
|
V0 |
|
|
|
|
Уравнение процесса 1-2 имеет вид p = a + bV, где a и b — постоянные коэффициенты. Учитывая уравнение состояния pV = RT, получаем (a + bV )V = RT, откуда T = (a + bV )V / R. Из последнего выражения
определим dT = |
1 |
|
|
|
|
|
---- (a dV + 2bV dV) . Подставим последнее соотно- |
||||||
|
R |
|
|
|
|
|
шение в (13.14): |
|
|
|
|
|
|
|
cmV |
(a + 2bV0 ) + |
(a + bV0 ) = 0 . |
|
||
|
--------- |
|
||||
|
R |
|
||||
После преобразований получаем |
|
|
||||
|
|
V |
|
a |
γ |
(13.15) |
|
|
0 |
= – ---- ------------ , |
|||
|
|
|
b |
γ + 1 |
|
|
где γ — показатель Пуассона [см. (10.16)]. Коэффициенты a и b определим из системы уравнений
p1 |
= a + bV1; |
|
|
|
|
|
p2 |
= a + bV2, |
|
|
|
|
|
решив которую получим: |
|
|
|
|
|
|
p1V2 – p2V1 |
|
p1 |
– p2 |
|
|
|
a = --------------------------------V2 – V1 |
; b = |
------------------- |
, |
(13.16) |
||
V1 |
– V2 |
|||||
где p1 = RT1 ⁄ V1 , p2 = RT2 ⁄ V2 . Конечную температуру T2 определим, использовав уравнение Пуассона:
T2 = T1(V1 ⁄ V2 )γ – 1 .
Таким образом, значение объема V0 полностью определено. Другие параметры газа в состоянии «0» легко определяются:
|
p0 = a + bV0 , |
|
|
(13.17) |
||
|
p0V0 |
|
a + bV |
0 |
|
|
T0 = |
------------ |
= |
------------------- |
V0 . |
(13.18) |
|
R |
R |
|
||||
Коэффициент полезного действия цикла находим по соотношению (11.2).
169

Работа газа за цикл равна сумме работ в процессах 1-2 и 2-1: Aц = = A12 + A21. Для процесса 1-2:
V2 |
|
|
|
b |
2 |
2 |
|
|
|
|
|
||||
A12 = ∫ (a + bV) dV = a(V2 |
– V1 ) + |
---- |
(V2 – V1 ) . |
||||
2 |
|||||||
V1 |
|
|
|
|
|
||
|
|
|
|
|
|
||
Для адиабатного процесса 2-1: |
|
|
|
|
|||
A21 = – U21 = – cmV(T1 – T2 ) = cmV(T2 – T1 ) . |
|||||||
Таким образом |
|
|
|
|
|
|
|
|
b |
2 |
2 |
|
|
|
|
Aц = a(V2 – V1 ) + |
---- |
(V2 – |
V1 ) + cmV(T2 – T1 ) . (13.19) |
||||
2 |
|||||||
Для определения количества теплоты, подводимого на участке 1-0, воспользуемся первым началом термодинамики:
Q10 = U10 + A10 ,
где A10 =
– T1).
V0 |
|
b |
2 2 |
|
|
|
|||
∫ (a + bV) dV = a(V0 |
– V1 ) + |
---- |
(V0 – V1 ) ; U10 = cmV(T0 – |
|
2 |
||||
V1 |
|
|
||
|
|
|
Окончательно
|
|
|
|
|
|
b |
2 |
2 |
Q10 = cmV (T0 – T1 ) + a(V0 – V1 ) + |
---- |
(V0 |
– V1 ) . (13.20) |
|||||
2 |
||||||||
С учетом (13.19) и (13.20) получаем |
|
|
|
|
||||
|
|
|
b |
2 |
2 |
|
|
|
Aц |
a(V2 – V1 ) + |
---- |
(V2 |
– V1 ) + cmV(T2 – T1 ) |
||||
2 |
||||||||
η = --------- |
|
= -------------------------------------------------------------------------------------------------------------- |
b |
|
|
|
|
. |
Q |
10 |
|
2 |
2 |
|
|
|
|
|
a(V0 – V1 ) + |
---- |
(V0 |
– V1 ) + cmV (T0 – T1 ) |
||||
|
|
2 |
||||||
Пример 13.5. Расстояние между стенками сосуда Дьюара L = 5 мм. Оцените давление воздуха между стенками, ниже которого средняя длина свободного пробега молекул газа при температуре t = 20 °C будет больше расстояния между стенками. Диаметр эффективного
сечения молекул воздуха принять равным 3æ10– 8 см.
Для решения задачи воспользуемся соотношением (12.4):
l |
|
kT |
|
kT |
= |
4------------2 ------------pπR2 |
= --------- |
2 -----------pπd2 . |
Из этой формулы следует, что при уменьшении давления средняя длина свободного пробега молекул возрастает и при некотором пре-
170