Материал: Общая физика_под ред. Белокопытова_2016 -506с
дельном значении pп становится равной расстоянию между стенками сосуда Дьюара, т.е. l = L . Тогда предельное давление можно
kT
найти как pп = --------------------- . После подстановки числовых значений полу-

 2 Lπd2
2 Lπd2
чаем: pп = 1,5æ10–2 мм рт. ст. Таким образом, начиная с давления около
10–2 мм рт. ст. и ниже, молекулы проскакивают между стенками сосуда и практически не взаимодействуют одна с другой.
Пример 13.6. Найдите отношение числа молекул водорода, скорости которых лежат в пределах от 1990 до 2000 м / с к числу молекул, скорости которых лежат в пределах от 990 до 1000 м / с, при температуре 400 К.
Для решения задачи используем максвелловское распределение молекул газа по скоростям (9.13), которое определяет, какое число dN молекул газа из общего числа его молекул N в единице объема имеет при данной температуре скорости, заключенные в интервале от v до v + dv:
|
|
3 |
|
|
m0v 2 |
|
|
|
|
|
|
|
m0 |
-- |
|
– |
-------------- |
|
|
2 |
|
|
|
2 |
|
2kT æ |
4π |
|
|
|
|
||||
dN = N |
------------- |
|
e |
|
|
v |
|
d |
v |
. |
|
2πkT |
|
|
|
|
|
|
В рассматриваемой задаче заданный интервал скоростей достаточно мал по сравнению с абсолютным значением скоростей молекул, поэтому без большой погрешности можно перейти к конечным разностям:
|
|
|
|
|
|
|
|
|
|
|
|
3 |
m |
0 |
v2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
-- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
m0 |
2 |
– ------------- |
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
= |
2kT æ |
4πv |
v . |
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
------- |
|
------------- |
e |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
N |
|
|
2πkT |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
Интервал скоростей в обоих случаях одинаков: |
|
v1 = |
|
v2 = |
v, поэ- |
||||||||||||||||||||||||
тому |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
m |
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
3 |
m |
|
|
2 |
|
|
|
|
|
|
|
|
0 |
v |
1 |
|
|
|
|
|
|
|
|
|
|
|
|
0 |
v |
2 |
|
|
|
|
||||
|
|
|
-- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
-- |
|
|
|
|
|
|
||||
N1 |
|
|
m0 2 |
|
– ------------- |
|
|
2 |
|
|
N2 |
|
|
m0 |
|
2 |
– ------------- |
|
|
2 |
|
||||||||
= |
e |
2kT æ |
4πv |
v , |
|
= |
2kT æ |
4 |
πv |
v , |
|||||||||||||||||||
--------- |
|
------------- |
|
|
|
|
|
--------- |
|
------------- |
e |
|
|
|
|
|
|||||||||||||
N |
|
2πkT |
|
|
|
|
|
|
|
1 |
|
N |
|
2πkT |
|
|
|
|
|
|
|
2 |
|
||||||
где v1 и v2 — среднеарифметические значения скоростей в соответствующих интервалах. Тогда
|
|
|
|
|
|
2 – |
m0(v12 – v22) |
|
N 1 |
= |
v1 |
|
--------------------------------2kT |
. |
|||
---------- N |
|
----- |
|
e |
|
|||
2 |
|
v |
2 |
|
|
|
||
|
|
|
|
|
|
|
||
171
Для получения окончательного ответа необходимо найти массу молекулы водорода m0. Вспомним, что масса одного моля молекул
(молярная масса) складывается из одинаковых масс NA молекул:
μ = NAm0 , где NA — число Авогадро. Тогда m0 = μ ⁄ NA . Учитывая,
что kNA = R, получаем:
N1
-----------
N2
=v----1- 2e
v2
μ(v12 – v |
22) |
– --------------------------- |
- |
2RT |
. |
|
Подстановка численных значений дает N1 ⁄ N2 = 1,6 .
172

Г л а в а 14
РЕАЛЬНЫЕ ГАЗЫ
Свойства не сильно разреженных газов отличаются от свойств идеальных газов, подчиняющихся уравнению Клапейрона — Менделеева (8.9). Например, из этого уравнения следует, что отношение
pV
---------- , называемое фактором сжимаемости, для идеальных газов
νRT
всегда равно единице. Однако опыты показывают, что факторы сжимаемости для всех газов зависят от давления и температуры. При достаточно высоких давлениях все реальные газы независимо от их температуры менее сжимаемы, чем идеальные.
Экспериментальные исследования удельной теплоемкости, вязкости и других свойств газов показали, что эти свойства тоже значительно отличаются от соответствующих свойств идеальных газов. Более того, приближенная теория идеальных газов часто не в состоянии объяснить даже качественно характер зависимости свойств газов от их параметров состояния. Например, реальные газы могут быть переведены в жидкое и твердое состояния. Уравнение Клапейрона— Менделеева не описывает подобные процессы.
Отступления от законов идеальных газов связаны с тем, что между молекулами газа действуют силы, которые в теории идеальных газов не принимаются во внимание. Поведение молекул реальных газов отлично от того, какое приписывается частицам идеальных газов. Во всех реальных телах (твердых, жидких и газообразных) молекулы взаимодействуют одна с другой. Силы взаимодействия между молекулами в сильной степени зависят от расстояния между ними. Эти силы имеют электромагнитную, а также особую квантовую природу.
14.1. Молекулярные силы
Своеобразные свойства поверхностного слоя жидкостей, а также способность твердых тел сопротивляться растяжению свидетельствуют о том, что между молекулами вещества действуют силы взаимного притяжения. Малая сжимаемость сильно уплотненных газов, а также способность твердых тел и жидкостей сопротивляться сжатию указывают на то, что между молекулами действуют и силы взаимного отталкивания. Важно, что силы притяжения и отталкивания
173
молекул действуют одновременно. Иначе молекулы, образующие тела, или разлетались бы в разные стороны, или «слипались».
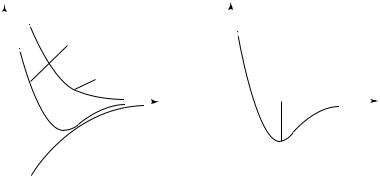
Кроме того, зависимость сил взаимного притяжения и отталкивания молекул от расстояния между ними должна быть различной: на очень близких расстояниях преобладают силы отталкивания, а на более далеких — силы притяжения. На рис. 14.1 показан примерный характер зависимостей Fпр(r) и Fот (r). Так обозначены проекции сил
º |
º |
º |
притяжения Fпр и отталкивания |
|
|
Fот на направление вектора r , |
||
проведенного в точку нахождения рассматриваемой молекулы из точки, где находится другая молекула, действующая на первую. Здесь же показана зависимость F(r), где F(r) = Fпр(r) + Fот (r).
º º
При r = r0 силы Fпр и Fот взаимно уравновешиваются и резуль-
º
тирующая сила F = 0. Если r > r0, то преобладают силы взаимного притяжения, а если r < r0, то преобладают силы отталкивания. Таким образом, r0 — это такое расстояние между двумя молекулами, на котором они находились бы при отсутствии теплового движения, нарушающего это равновесие.
Найдем выражение потенциальной энергии взаимодействия двух молекул Uп . При увеличении расстояния между молекулами на d r
потенциальная сила межмолекулярного взаимодействия |
º |
совер- |
||||||||||
F |
||||||||||||
шает работу δA |
º |
º |
|
|
|
|
|
|
||||
= ( F |
, d r ). Поскольку эта работа совершается за |
|||||||||||
счет уменьшения взаимной потенциальной энергии молекул, то δA = |
||||||||||||
F |
|
|
F |
|
|
|
Uп |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Fот |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
0 |
|
r0 |
|
|
|
0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
r0 |
|
|
|
|
|
|
r |
||||
|
|
|
|
r |
|
|
|
|||||
|
|
|
|
|
Fпр |
|
|
|
Рис. 14. 2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
Рис. 14. 1 |
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|||||
174
= – dUп . Тогда dUп = Fdr . Интегрируя это выражение по r от r до ×,
×
получаем Uп(r) – Uп(×) = ∫ F dr .
r
На бесконечно большом расстоянии одной от другой молекулы не взаимодействуют. Поэтому удобно принять Uп(×) = 0. Окончательно,
× |
|
Uп(r) = ∫ F dr . |
(14.1) |
r
Из рис. 14.1 видно, что при r > r0 взаимная потенциальная энергия отрицательна, так как F < 0. При r = r0, как видно из (14.1),
|
---------dUп- |
|
= – F(r0 ) = 0 , |
|
dr |
r = r0 |
т.е. функция Uп ( r ) достигает минимума. При сближении молекул до расстояния r0 их взаимная потенциальная энергия уменьшается,
а кинетическая увеличивается. Происходит это за счет положительной работы сил взаимного притяжения молекул (F < 0 при r > r0,
рис. 14.1). При дальнейшем сближении молекул сила взаимного отталкивания молекул совершает отрицательную работу (F > 0 при r < r0, рис. 14.1). Поэтому потенциальная энергия начинает расти.
Характер зависимости Uп ( r ) показан на рис. 14.2.
Зависимость потенциальной энергии двух молекул реального газа от расстояния между ними может быть описана формулой Ленарда — Джонса:
|
|
a |
1 |
|
a2 |
|
|
|
Uп |
= – |
----- |
+ |
------- |
, |
(14.2) |
||
r |
6 |
r12 |
||||||
|
|
|
|
|
||||
где a1 и a2 — положительные постоянные коэффициенты, зависящие от вида газа.
Дифференцируя (14.2) по r, находим зависимость проекции результирующей силы взаимодействия двух молекул реального газа:
|
dUп |
|
6a1 |
|
12a2 |
|
||
F = – |
---------- |
= – |
-------- |
+ |
----------- |
(14.3) |
||
dr |
r |
7 |
r |
13 . |
||||
|
|
|
|
|
|
|
||
Первое слагаемое в (14.3) соответствует силам молекулярного притяжения, которые часто называют ван-дер-ваальсовыми силами по имени нидерландского физика Я.Д. Ван-дер-Ваальса, который впервые начал учитывать межмолекулярное взаимодействие в газах. Второе слагаемое в (14.3) соответствует силам взаимного отталкивания молекул. Эти силы играют определяющую роль на малых рассто-
175