Материал: Модифікування полісульфонових мембран з альфа-амілазою, інкорпорованою в полімерні міцели
Об‘ємний потік крізь мембрану
(продуктивність мембрани, Jυ, л/(м2·год) розраховували за формулою:
Jυ
= ![]() ,
,
де ΔV - об‘єм фільтрату, що пройшов крізь мембрану площею S за час Δτ.
Активність α-амілази
визначали за ступенем конверсії крохмалю. Для цього під час процесу
ультрафільтрації крохмалю різної концентрації відбирали проби пермеату та
ретентату (ступінь відбору 80 %). Концентрацію крохмалю визначали за
концентрацією комплексу крохмаль-йод УФ-спектрофотометрично при довжині хвилі
580 нм. Ступінь конверсії крохмалю у % розраховували за формулою:
![]() ,
,
де С0 -
початкова концентрація крохмалю; Сt -
концентрація крохмалю у пробі.
.3.6 Методика розрахунку констант масопереносу крохмалю
На першому етапі досліджували
продуктивність мембран в діапазоні тисків від 50 до 300 кПа при
ультрафільтрації розчинів крохалю з різною концентрацією. Константи
масопереносу визначали з рівняння прямої залежності продуктивності мембрани від
логарифму концентрації крохмалю.
РОЗДІЛ 3. АНАЛІЗ ТА
УЗАГАЛЬНЕННЯ РЕЗУЛЬТАТІВ ДОСЛІДЖЕНЬ
.1 Визначення ККМ
блок-кополімеру
Для одержання полімерних
міцел необхідно знати ККМ три-блок-кополімеру, який визначали оптичним методом.
З
рис.
3.1 можна
зробити висновок, що різка зміна значення оптичної
густини
відбувається у проміжку концентрації від 0,024 до 0,028 %.
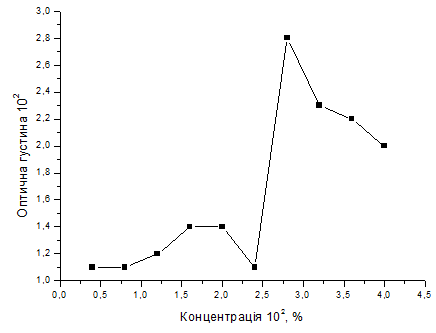
Рис. 3.1.
Залежність світлопропускання від концентрації розчину б-ПЕГ-б-ППГ-б-ПЕГ
Знаходимо значення концентрації міцелоутворення за пропорцією:
2250 г - 1 моль
,28 г - x моль
![]()
![]() моль/дм3.
моль/дм3.
Отже, для одержання міцел
потрібна концентрація б-ПЕГ-б-ППГ вища за ККМ.
.2 Модифікування
полісульфонових мембран полімерними міцелами з ферментом
На першому етапі дослідження
полімерні міцели іммобілізували на поверхню мембран за рахунок адсорбції. Для
цього використовували розчини б-ПЕГ-б-ППГ-б-ПЕГ концентрацією від 0,05 до 0,2
%. Однак, такі системи можуть бути нестабільними, тому ми вирішили дослідити
вимивання ПАР з міцел, однак опосередкованим методом, вимірюючи продуктивність
мембрани за водою через певні проміжки часу зберігання мембрани у воді.
Залежність об’ємного потоку від часу вимивання наведена на рис. 3.2.
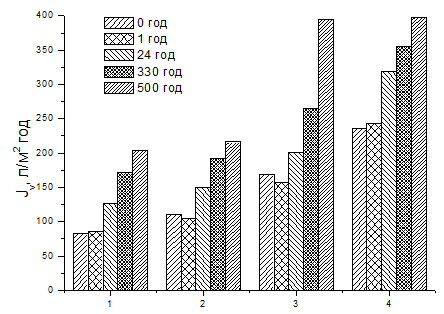
Рис. 3.2.
Залежність продуктивності мембран від тривалості відмивання при різній
концентрації ПАР: 1 - 0,05 %, 2 - 0,10 %, 3 - 0,15 %, 4 - 0,20 %.
З рис. 3.2. видно, що система залишається сталою тільки протягом однієї години, що буде призводити до забруднення продуктів блок-кополімером, а також до вимивання ферменту та його втрат. Отже, ми вирішили зробити прищеплення полімерних міцел з ферментом до поверхні полісульфонових мембран за допомогою УФ-опромінення. Однак це може призвести до деструкції білка та втрати його активності. Тому мембрани з адсорбованими міцелами опромінювали не більше 5 хвилин. Введена концентрація α-амілази становила 1мг/мл. Після опромінення стійкість системи до вимивання зберігається протягом 300 годин.
Після опромінення
досліджували активність α-амілази за
реакцією гідролізу крохмалю. Ми дослідили ступінь конверсії крохмалю у процесі
ультрафільтрації у пермеаті та ретентаті. Результати цього дослідження наведені
на рис. 3.3.
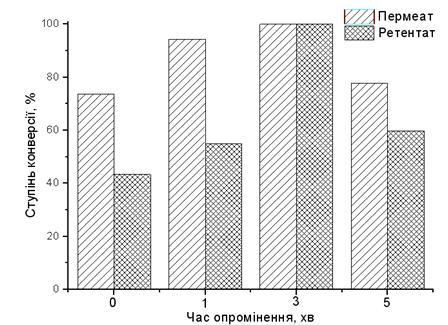
Рис. 3.3. Залежність
ступеню конверсії крохмалю α-амілазою від
тривалості УФ-опромінення
Активність ферменту на
опромінених мембранах порівнювали з активністю α-амілази
на неопроміненій мембрані (0 хв). З рис. 3.3 видно, що найбільша
активність ферменту спостерігається при трихвилинному опроміненні, так як
ступінь конверсії у ретентаті та у пермеаті 100%. У випадку одно- та
двохвилинного опромінення ступінь конверсії у пермеаті 67 та 98%, відповідно,
але у ретентаті ступень конверсії різко падає і становить 41 та 56%,
відповідно. Якщо опромінювати мембрану більше трьох хвилин, ступінь конверсії
знову починає падати. Це можна пояснити денатурацією ферменту під час
опромінення або неможливістю підходу високомолекулярного субстрату крохмалю до
активного центру ферменту внаслідок занадто сильного зшивання полімеру.
.3 Дослідження явища концентраційної
поляризації на полісульфонових мембранах, модифікованих полімерними міцелами з α-амілазою
Явище концентраційної поляризації та забруднення поверхні мембран є серйозною проблемою при ультрафільтрації високомолекулярних сполук, зокрема і розчину крохмалю. Усі процеси мембранного розділення супроводжуються цим феноменом, при якому склад суміші у при мембранному шарі з боку сировини відрізняється за складом вихідної суміші. Цього явища повністю уникнути неможливо, однак потрібно мінімізувати ефект концентраційної поляризації через те, що він знижує продуктивність мембрани та підвищує спорідненість мембрани до забруднення. Отже, зведення до мінімуму концентраційної поляризації є одним з найбільш важливих завдань у проектування та створенні систем мембранного розділення.
Ми дослідили залежність об’ємного
потоку розчину крохмалю крізь мембрану при різних зовнішніх тисках, так як з
цієї залежності можна зробити висновки про наявність концентраційної
поляризації. Дана залежність наведена на рис. 3.4.
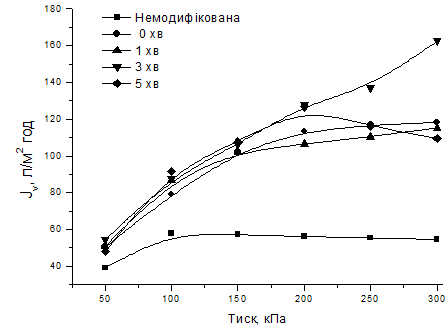
Рис. 3.4.
Залежність трансмембранного потоку від робочого тиску при пропусканні 0,01%
розчину крохмалю через мембрани
На рис. 3.4 видно, що продуктивність немодифікованої мембрани виходить на плато вже при тиску 100 кПа та починає поступово зменшуватися. Мембрани, модифіковані міцелами з ферментом, характеризуються вищими значеннями об’ємного потоку, ніж не модифікована, що можна пояснити гідрофілізацією поверхні мембран при модифікації. Для неопроміненої мембрани та мембран з часом опромінення 1 та 5 хв залежність продуктивності від тиску майже не відрізняється, що добре корелює зі значеннями активності ферменту на цих мембранах. Так, явище концентраційної поляризації спостерігається для цих мембран при тиску 200 кПа. Однак, найкращі показники має мембрана, опромінена протягом трьох хвилин. При концентрації крохмалю 0,01 % залежність Jv від тиску лінійна та не виходить на плато, тобто ефекту концентраційної поляризації не було досягнуто. Це можна пояснити високою активністю ферменту, який розкладає крохмаль у при мембранному шарі і не дає йому там накопичуватися і відкладатися на поверхні, утворюючи гелевий шар.
Для кількісної оцінки транспортних
характеристик мембран оцінювали коефіцієнт масопереносу. Для цього досліджували
залежність об’ємного потоку мембрани від тиску при різних концентраціях
крохмалю. Та будували залежність продуктивності мембрани, при якому вона
виходить на плато, від натурального логарифму концентрації крохмалю (рис. 3.5).
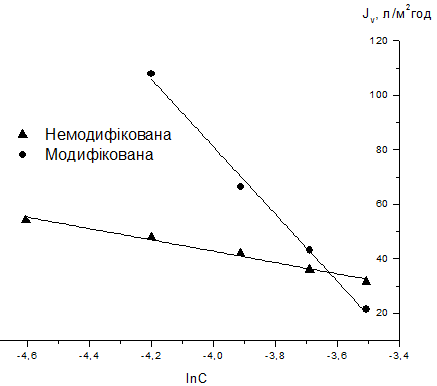
Рис. 3.5.
Визначення
коефіцієнту масопереносу не модифікованої
та мембрани, модифікованої полімерними міцелами з ферментам з часом опромінення
3 хв
Наведені залежності є лінійними.
Коефіцієнти рівнянь прямих наведені в табл. 3.1. Коефцієнт b
з протилежним знаком є константою масопереносу.
Таблиця 3.1. Коефіцієнти рівнянь прямих
|
Мембрана |
Коефіцієнт a |
Коефіцієнт b |
R2 |
||
|
|
Значення |
Похибка |
Значення |
Похибка |
|
|
Немодифікована |
-40,5592 |
5,5246 |
-20,8261 |
1,38116 |
0,9827 |
|
Модифікована |
-414,3741 |
23,8349 |
-123,8797 |
6,21423 |
0,9924 |
Коефіцієнт масопереносу не
модифікованої мембрани К1=20,8261±1,38116 м/с , а
модифікованої К2=123,8797±6,21423 м/с . Отже, К2 перевищує К1
у 5,95 разів.
ВИСНОВКИ
1. Розроблено методику модифікування полісульфонових мембран α-амілазою, інкорпорованою у полімерні міцели на основі поліетиленгліколь-блок-поліпропіленгліколь-блок- поліетиленгліколю.
. Встановлено, що оптимальними умовами модифікування мембран полімерними міцелами на основі поліетиленгліколь-блок-поліпропіленгліколь-блок- поліетиленгліколю є:
- концентрація ПАР - 0,1 %;
- концентрація α-амілази - 1 мг/мл;
час УФ-опромінення - 3 хв.
. Досліджено каталітичні властивості модифікованих мембран за реакцією гідролізу крохмалю та встановлено, що найбільший ступінь конверсії крохмалю характерний для мембрани з часом опромінення 3 хвилини.
. Досліджено транспортні характеристики модифікованих мембран та показано, що модифікація мембран полімерними міцелами призводить до зростання їх продуктивності на 100-120 %.
. Встановлено, що коефіцієнт
масопереносу мембрани, одержаної за оптимальних умов збільшується у 5,95 разів
порівняно з коефіцієнтом масопереносу немодифікованої мембрани.
СПИСОК ВИКОРИСТАНИХ ДЖЕРЕЛ
1. Zana R. / Dynamics of surfactant self-assembliesmicelles, microemulsions, vesicles, and lyotropic phases/- Boca Raton. FL 33487-2742: CRC Press, Taylorand Francis Group, 2005.- 2-16 с.
2. Sinko P. /Martin's physical pharmacy and pharmaceutical sciences./-Maryland, USA: Lippincott Williams and Wilkins, 2007.- 469-97 с.
3. Verma M. / Nano Res. 5/ Verma M., Liu S., Chen Y., Meerasa A., Gu F., 2012.-49-61c.
. A.N. Martin. Physical Chemical Biopharmaceutical Principles in the Pharmaceutical Sciences / P.J. Sinko, Y. Singh, Martin’s Physical PharmacySciences, 2011.- 6th ed.
. Bromberg L. Polymeric micelles in oral chemotherapy; JControl Release, 2008.-[128]99-12 c.
.Mondon K. Coloidal drug delivery system -Recent Advances with Polimeric Micelles / Gurny Robert,Moller Michael.-Chimia, 2008.-[62] 832-840 c.
.Bromderg L. Polymeric micelles in oral chemotherapy. -Journal of Controlled Release, 2008.-[128]99-112 c.
.Francis Mira F. Polimeric micelles for oral drug delivery:Why and how/ Cristea Mariana,Winnik Francoise M.-Pure Applied Chemistry, 2004.-[76] 1321-1335 c.
. Spectrofluorimetric Determination of Second Critical Micellar Concentration of SDS and SDS/Brij 30 systems / Romani Anna Paula, Machado Antonio Eduardo da Hora, Hioka, Noboru, Severino Divinomar.-J Fluoresc, 2009. -[19] 327-332 c.
. Kabanov A.V. Pluronic block copolymers as novel polymer therapeutics forand gene delivery / Batrakova E.V., Alakhov V.Y.- J Control Release, -2002.-[82]-189-201 c.
. Webber S.E. Polymer micelles: An example of self-assembling polymers.- J Phys Chem B, 1998.-[102] 2618-26 c.
. Size characterization of drug-loaded polymeric core/shell nanoparticles using asymmetrical flow field-flow fractionation / Kang D.Y., Kim M.J., Kim S.T., Oh K.S., Yuk S.H., Lee S. -Anal Bioanal Chem, 2008.-[390] 2183-88 c.
. Core-shell structure of degradable, thermosensitive polymeric micelles studied by smallangle neutron scattering / [Ramzi A., Rijcken C.F., Veldhuis T., Schwahn D., Hennink W.E., Nostrum C.F.].- J Phys Chem B, 2008.-[112] 784-92.
. Control. Release / [K. Kataoka, T. Matsumoto, M. Yokoyama, T. Okano, Y. Sakurai,S. Fukushima, K. Okamoto, G.S. Kwon.].- J 64, 2000.- 143-153 c.
. F. Cau. Macromolecules / S. Lacelle, 1996.- 170-178 c.
. Angew.Chem. Int. Ed. Engl /[ M. Shi, J.H. Wosnick, K. Ho, A. Keating, M.S. Shoichet],2007-[46] 6126-6131 c.
. P. Alexandridi. Amphiphilic Block Copolymers Self-assembly and Applications / B. Lindman,-Elsevier, Amsterdam, New York, 2000.
. A. Hatton J. Chem. Phys T./ P.H. Nelson, G.C. Rutledge,1997-[107] 10777-10781 c.
. J. Lu. Macromolecules 43/ M.S. Shoichet, 2010- 4943-4953 c.
. A polymeric micellar carrier for the solubilization of biphenyl dimethyl dicarboxylate / Chi S.C. Yeom D, Kim SC, Park E.S.- Arch Pharm Res,2003-[26] 173-81c.
22. Engineering polysaccharide-based polymeric micelles to enhanceof cyclosporin A across Caco-2 cells / Francis M.F., Cristea M., Yang Y., Winnik F.M.-Pharm Res, 2005-[22] 209-19 c.
. Methoxy poly(ethylene glycol)-block-poly(-valerolactone)copolymer micelles for formulation of hydrophobic drugs / Lee H., Zeng F., Dunne M., Allen C.-, 2005-[6]3119-28 c.
. Kabanov A.V. Pluronic block copolymers in drug delivery: From micellar nanocontainers to biological response modifiers /Alakov V.Y..-Crit Rev Ther Drug Carrier Syst , 2002-[19]1-73 c.
. Solubilisation of drugs in worm-like micelles of block copolymers of ethylene oxide and 1,2-butylene oxide in aqueous solution Zhou Z., Chaibundit C., Emanuele A., Lennon K., Attwood D., Booth C.- Int J Pharm,
-[354] 82-87 c.
. Dong Y. Surface activity and solubilization of a novel series of functional polyurethane surfactants /Jin Y, Wei D.-Polym Int, 2007-[56] 14-21c.
.Tochilin V.P.Micellar nanocarriers:Pharmaceutical Research,2007-[24(1)]1-16 c.
.Aliabadi H.M. Pollymeric micelles for drug delivery. Expert opinion on drug delivery / Lavasanifar A., 2006-[3(1)]139-162 c.
. Liu Y.L. Preparation of polysulfone-gpoly(N-isopropylacrylamide) graft copolymers through atom transfer radical polymerization and formation ofresponsive nanoparticles / Lin G.C., Wu C.S.-J Polym Sci Part: Polym Chem, 2008-[46] 4756-65 c.
. Control. Release /[J.E. Chung, M. Yokoyama, M. Yamato, T. Aoyagi, Y. Sakurai, T.Okano],-J. 62, 1999-115-127 c.
. Int. J. Pharm / [H.M. Aliabadi, S. Elhasi, A. Mahmud, R. Gulamhusein, P., A. Lavasanifar], 2007-[329]158-165 c.
. Control. Release /[ Y. Yamamoto, K. Yasugi, A. Harada, Y. Nagasaki, K. Kataoka], 2002-[82] 359-371 c.
.M.C. Porter, Industrial Engineering Chem. Production Res. Develop., ll(3) -1972-234.
34. M.J. Clifton, N. Abidine, P. Aptel and V. Sanchez, J.Membr. Sci., 21 ,1984-233.
35. W. Blatt, A. Dravid, A.S. Michaels and L. Nelsen, in:J.E. Flinn, ed., Membrane Science and Technology,Plenum, New York, 1970-pp. 47-91.
36. M.C. Porter, Industrial Engineering Chem. Production Res. Develop., ll(3) ,1972-234.
37. G.A. Denisov, J. Membr. Sci., 91 ,1994- 173.
. S.V. Gupta, Desalination, 85 ,1992-283.
. V. Gekas and B. Hallstorm, J. Membr. Sci., 30 ,1987-153.
. M.S.H. Bader and J.N. Veenstra, J. Membr. Sci., 114,1996-139.
. Z.V.P. Murthy and S.K. Gupta, Desalination, 109,1997-39.