Материал: Модифікування полісульфонових мембран з альфа-амілазою, інкорпорованою в полімерні міцели
Модифікування полісульфонових мембран з альфа-амілазою, інкорпорованою в полімерні міцели
ВСТУП
Процес біокаталізу полягає у перетворенні субстрату в корисні продукти за допомогою ферментів в гомогенних чи гетерогенних системах. Як і у всіх інших хімічних процесах відділення реагентів від продукції та регенерація і повторне використання каталізатора є важливим кроком, що значно зменшує собівартість процесу. Мембранні реактори надають можливість інтегрувати каталітичну конверсію, відділення продукту і/або його концентрування та регенерацію каталізатора в одній технологічній операції.
Більшість ферментативних процесів промислового використання в даний час проводять в реакторах періодичної дії. Однак, вони мають ряд відомих недоліків та обмежень, такі як висока вартість робочої сили, часті процедури запуску і вимкнення, а також необхідність відновлення ферменту або ферментного препарату після кожної партії товару. Використовуючи іммобілізовані ферменти, можна оперувати ферментними процесами безперервно з відповідними перевагами, такими як кращий контроль процесу, підвищення продуктивності, одержання більш однорідної продукції та інтеграції стадії очищення у процес. Іммобілізації ферментів можна досягнути шляхом хімічного або фізичного прищеплення до твердих поверхонь. Проте останнім часом набувають поширення мембранні реактори з ферментами, мікрокапсульованими в міцелярні системи, найбільшою з переваг яких є стабільність ферменту та його висока активність за рахунок збереження природньої конформації білка в міцелах. Однак, використання таких реакторів обмежується проблемою забруднення реакційного середовища поверхнево-активними речовинами. Нами було запропоновано іммобілізацію міцел на поверхню полімерних мембран як один із шляхів вирішення цієї проблеми.
Отже, метою роботи було одержати полісульфонові мембрани, модифіковані α-амілазою, інкорпорованою в полімерні міцели на основі триблок-кополімеру.
Відповідно до мети були поставлені такі завдання:
відпрацювати методику іммобілізації полімерних міцел з α-амілазою на поверхню полісульфонових мембран;
дослідити вплив тривалості процесу УФ-опромінення на каталітичну активність ферменту;
дослідити транспортні та каталітичні характеристики модифікованих мембран щодо розчину крохмалю.
РОЗДІЛ 1.
ОГЛЯД
ЛІТЕРАТУРИ
1.1 Міцели та їх характеристики
Міцела - це продукт асоціації, який утворюється у водних розчинах завдяки силам міжмолекулярного притягання, які зумовлюють асоціацію вуглеводневих ланцюгів, які містять кілька десятків молекул і мають загальну молекулярну масу 12000-22000 г/моль. Радіус сферичної міцели такий самий як довжина повністю розтягнутого мономера, в основному радіус 1-3 нм, через це міцели мають колоїдну ступінь дисперсності [1,2].
Процес утворення міцели називається міцелоутворенням. У результаті міцелоутворення неполярні ланцюги утворюють ніби вуглеводневу краплю, екрановану направленими у воду полярними групами. Стан міцели відповідає найбільшому зменшенню вільної енергії [3,4] .
Розміри міцели обмежуються силами електростатичного відштовхування між наближеними йоногенними групами. Рівновага асоціації між міцелами і окремими молекулами і ступінь їхньої іонізації залежить від концентрації, температури, pH, наявності електролітів у розчині [5,6].
Міцели містять внутрішнє ядро, утворене скупченням гідрофобних сегментів, які здатні до солюбілізації (розчинення) ліпофільних розчинів і зовнішньої гідрофільної корони, яка слугує стабілізатором внутрішньої поверхні між гідрофобним ядром і зовнішнім водним середовищем. Ґрунтуючись на меті доставки, ми можемо обрати розмір, заряд і властивості поверхні цих носіїв просто додаючи нові інгредієнти до мікстури з амфіфільних рідин перед приготуванням міцел і/або варіюючи препараційні методи [7,8].
Унікальність міцел як нанорозмірної
фази, що утворюється колоїдними ПАР, у тому, що вона практично не має
макроскопічного аналогу. Прикладами міцелярних систем є прямі і зворотні
міцели, мікроемульсії(масло/вода і вода/масло), везикули, ліпосоми, ліпідні
мембрани, плівки Ленгмюра-Блоджетт, рідкі кристали та інші системи [5].
Утворення міцелярних систем не пов’язано з виникненням міжмолекулярних
зв’язків, тому вони є самоорганізованими наносистемами, що мають
супрамолекулярну структуру [3].
.2 Полімерні міцели
.2.1 Характеристика полімерних міцел
Використання міцел на полімерній основі притягує багато уваги через велику різноманітність полімерів, їхню біодоступність, біорозпадання і численність функціональних груп, які дозволяють сполучатись сусіднім молекулам. Амфіфільні полімери асоціюють у воді створюючи "полімерні міцели", які містять гідрофобне ядро,яке стабілізується короною з гідрофільних полімерних ланцюгів.
Полімерні міцели можна використовувати як ефективні переносники для сполук ,які мають погану розчинність, небажану фармакокінетику і низьку стабільність у фізіологічному середовищі. Гідрофобна оболонка дуже сприяє фармацевтичній поведінці полімерних утворень підтримуючи міцели у дисперсному стані , а також знижуючи небажані взаємодії ліків з клітинами та білками через стерично-стабілізуючі ефекти.
Розмір полімерних міцел різниться від 10 до 100 нм. Ця топологія є схожою до міцел ПАР, отже можна очікувати,що полімерні міцели розчиняють гідрофобні ліки. Проте, є значні відмінності між двома типами міцел з фізико-хімічної точки зору.
Концентрація полімеру, з якої
починається утворення міцел називається ККМ( критична концентрація
міцелоутворення) і вона для полімерних міцел нижча на кілька порядків від
величини ККМ типових ПАР. Таким чином, полімерні міцели є більш стійкими до
розбавлення у біологічних розчинах. Вони можуть підвищувати біодоступність
ліків і утримання, поки ліки добре захищені від можливої інактивації під
впливом біологічного середовища[9,7,10].
.2.1.1 Критична концентрація міцелоутворення
У водних середовищах амфіфільні
полімери можуть існувати у формі міцел,коли їхня концентрація вище за ККМ, і
коли розбавлення нижче цієї концентрації міцели можуть розпадатись. Отже, ККМ є
ключовим параметром при утворенні і набутті стабільності полімерних міцел.
Деякі із способів визначення ККМ у водних дисперсіях міцел включають
вимірювання поверхневого натягу, хроматографію, розсіювання світла, малокутове рентгенівське
випромінювання, диференціальну скануючу колориметрію, віскозиметрію і
використання флуорисцентних зондів. Для легкого практичного визначення ККМ
отримують з ділянок поверхневого натягу як функцію логарифму від концентрації.
Кажуть, що ККМ досягнена, коли поверхневий натяг перестає збільшуватись і
досягає величини насичення. Багато дослідників зробили ставку на використання
пірену як флуорисцентний зонд для оцінки ККМ [11].
.2.1.2 Розмір, форма міцел та число агрегації
Після утворення міцел корисну інформацію щодо полідисперсності утворених структур добувають перевіряючи міцелярний розчин технікою квазіпружного розсіювання світла. Монодисперсні міцели мають блакитне забарвлення при розсіюванні світла, що свідчить про те, що міцели добреприготовані, та як контрастують з білим кольором агрегатів[12].
Розмір полімерних міцел завжди попадає в колоїдний діапазон. Скануюча електронна мікроскопія(СЕМ) і трансмісійна електронна мікроскопія (ТЕМ) широко використовуються для встановлення розміру і форми блок-кополімерних міцел. Нещодавно розвинена кріо-ТЕМ техніка стає всі більш важливою для характеристики блок-кополімерних міцел у водних середовищах. СЕМ або атомно-силова мікроскопія (АСМ) показують інформацію щодо розподілу розміру, коли представлені хімічно-прикріплені міцели до поверхні . Пряму візуалізацію блок-кополімерних міцел і в сухому стані і безпосередньо "в середовищі" без рідкокристалічнлї комірки можна отримати за допомогою АСМ. Гідродинамічні показники діаметру і полідісперсності міцел отримують використовуючи фотонну кореляційну спектроскопію. Нещодавно характеристики розміру полімерних міцел навантажених лікарськими засобами були отримані використовуючи асиметричні поля течії потоку фракції і структура угрупування була встановлена використовуючи малокутове розсіювання нейтронів [13,14].
Кількість полімерних ланцюгів ,які
об’єднуються для створення міцели називається числом агрегацій [15,16].
Число агрегації найпростіше можна виразити формулою:
Nag =M/M0
M-це
молекулярна маса одної міцели і М0 -це молекулярна маса полімерної
основи. Пряме визначення молекулярної маси міцели використовуючи седиментацію
центрифугуванням або іншими техніками може бути занадто важким; однак, оцінити
М можна підрахувавши розмір міцели за формулою:
M =4ПNAR3/3n2
Де R-це
радіус міцели, NA
-це число Авогадро, n2-частковий
специфічний об’єм полімеру. Використовуючи другий підхід Nag
можна вирахувати шляхом визначення гідродинамічного радіусу міцели та
вимірюванням внутрішньої в’язкості, як вказано у наступній формулі:
Nag =10ПRн3NA/3[η]M
де Rн
- це гідродинамічний радіус і [η]
-внутрішня в’язкість. Число агрегацій для міцели завжди варіюється від десятків
до сотень, але може і достягати тисяч[17-19].
Більшість полімерних міцел мають сферичну будову і їх розміри лежать в
діапазоні 10-200 нм [20]. Структура, молекулярна маса і
молекулярно-масовий розподіл між гідрофільними і гідрофобними сегментами
полімерної основи мають прямий вплив на розмір та форму міцел. В основному,
коли гідрофільний сигмент полімеру (корона) довший ,ніж гідрофобний сигмент
полімеру (ядро), сферичні міцели збираються в угрупування; однак, збільшення
кількості кристалічних складок у ядрі призводить до зниження скупчення корони,
і до збільшення стержневидної морфології. Так як міцели є фізично утвореними
структурами ,зміни в середовищі завжди мають вплив на розмір та ,а отже
впливають на стабільність міцели. Також розмір міцел визначається молекулярною
геометрією індивідуальних ланцюгів , які знаходяться під впливом умов розчину
таких як йонна сила, pH,
температура, і концентрація полімеру [17].
.2.1.3 Солюбілізація
Міцелярне ядро-це компактне мікро-середовище і центр для залучення нерозчинних у воді молекул-гостей. Гідрофобні молекули можуть бути ковалентно включені до блок-кополімерів або фізично-включені у гідрофобне ядро міцели. Процес солюбілізації веде до збільшення їхньої розчинності у воді, а отже і біодоступності [21]. Завжди можна спостерігати,що поглинання шлунково-кишечним трактом часточок істотно залежить від розміру часточок. Було відзначено, що у 15-250-разів більш високу ефективність поглинання ШК-трактом мають часточки приблизно 100 нм у діаметрі, ніж часточки розміром з мікрометр [22]. Таким чином, полімерні міцели (нанорозмірні) піднімають поглинання і підвищують біодоступність.
Ступінь солюбілізації базується на
процесі міцелізації, сумісності між ліками та ядро-утворюючим блоком, довжиною
ланцюга гідрофобного блоку, концентрацією полімеру та температурою [23]. Вище
ККМ, відбуваєтьтся різке збільшення солюбілізації ліків ,так як стає більше
простору для утворення агрегатів гідрофобними частинами міцел.Коли ліки
займають ядерну ділянку ,це призводить до підвищення Re
міцели. Важливо зазначити,що ядерна ділянка має обмежену здатність для
розміщення солюбілізату, наприклад, Pluronic
P85 має ядерну
дяліянку,яка займає 13% від усієї ваги міцели [24]. Вплив на солюбілізаційну
здатність довжини гідрофобного блоку було розглянуто для грізеофульвіну у
міцелі кополімеру поліоксиетилену та поліоксибутилену варіюючи довжини
гідрофобних блоків та гідрофільних блоків у достатній кількості для формування
сферичних міцел. З цього слідувало те, що солюбілізаційна здатність ґрунтується
на довжині гідрофобного блоку до певної міри (15 гідрофобних блоків), після
якої солюбілізаційна здатність досягає насичення[25].Також вивчався вплив
довжини гідрофобного блоку на солюбілізацію толуену у диблоку або триблоку
поліуритановому ПАР. Був зроблений висновок, що солюбілізаційна здатність
поліуританового ПАР зростає зі зростанням у гідрофобному сегменті кількості
однакових за структурою ланцюгів[26].
.2.2 Міцелярна структура
Полімерні міцели формуються з
амфіфільних кополімерів, що мають гідрофільний блок і гідрофобний блок . Будова
амфіфільного кополімеру може виявлятись у наступних можливих формах міцелах
[7]:
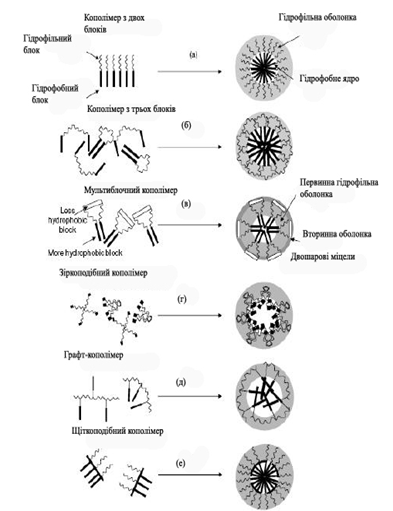
Рис. 1.
Різні міцелярні форми які можуть формуватись спонтанно у водному середовищі при
різній будові кополімерів
.2.3 Полімери для одержання полімерних міцел
Можна використовувати численні полімери для одержання полімерних міцел, з варіацією гідрофільних та гідрофобних блоків використовуючи експансивну бібліотеку для можливих засобів доставки лікарських засобів. Перед тим як доставляти ліки за допомогою полімерів і для подальшого перетравлення їх у організмі, вони повинні бути схвалені міністерством харчування та ліків. Ці вимоги обмежують вибір різних блоків, тому що легше розробити нову технологію, використовуючи вже схвалені міністерством харчування та ліків засоби для доставки ліків. В основному, для фармацевтичного застосування, амфіфільні полімери повинні демонструвати біосумісність та не токсичність [7].
Існує широкий вибір полімерів з гідрофільними блоками. Найбільш частіше використовують полі(етиленгліколь) (ПЕГ) через те,що він не дорогий, має низьку токсичність є хорошим стеричним протектором для багатьох біологічно активних макромолекул. ПЕГ також використовують у засобах доставки , які вдосконалені регулюючими агентами для внутрішнього застосування[27]. Не зважаючи на те, що ПЕГ не піддається біологічному розкладанню ,він легко виводиться з організму видільними шляхами ,якщо його молекулярна маса нижче 15 кДа [7].Майже всі сьогоднішні пошуки фокусуються на ланцюгах ПЕГ різної молекулярної маси ,але також можна використовувати і інші полімери. Такими полімерами, що викликають зацікавленість є полі(N-вініл-2-піралідон) та полівініловий спирт. Вони обидва є біосумісними і по розчинності у воді є близькими до ПЕГ [7].Якщо потрібна термостійкість та стійкість до pH середовища ,то використовують полі(N-ізопропілакриламід)[27].
Деякі полімери стикаються з вимогами фармацевтичного застосування до гідрофобного формуючого ядро блоку. Більшість таких полімер з родини поліестерів та поліамінових кислот [28]. Найбільш часто у наукових дослідженнях використовують полі(пропілен оксид), полі(капролактон),полі(L-лактанова кислота), полі(лактан-ко-гліколева кислота),полі(аспарагінова) кислота,полі(глютамінова кислота),полі(L-лізин) та різні полі(акрилати)[24-26]. Основна відміність між ними це те, чи бажана наявність заряду чи ні і стабільність зв’язку для контрольованого вивільнення. Багато з вищевказаних полімерів розпадаються на мономери ,які і так наявні у організмі і які затверджені міністерством харчування та ліків. Одним з прикладів таких полімерів є полі(лактан-ко-гліколева кислота) ,який і біосумісний і такий, що біорозкладається ,розкладаючись на ліктанову та гліколеву кислоту , які є продуктами метаболічного розпаду у організмі. Це самі ті дві різні опції для двох блоків ,що роблять полімери для налаштування даного лікарського препарату[27].
Міцело-формуючі амфіфільні кополімери можуть бути і блок-кополімерами(ди-,три- або тетра-), так і графт-кополімерами. Графт-кополімер є таким,що включає в себе полімерний ланцюг як основу і інший полімерний ланцюг як "прищеплену" частину. Такі кополімери зазвичай демонструють якості і основи і "прищепленої" частини."Клік"-реакції (селективні реакції для швидкого синтезу нових з’єднань через гетеро атомні з’єднання (С-X-C)) з’явилися як засіб для вбудовування ланцюгів полімеру у полімерну основу для отримання чітко визначеного графт-кополімеру [29]. Таблиця 1 показує різні можливі структури амфіфільних кополімерів з характерними представниками кожного класу.
Табл.1 Структури кополімерів та їх представники

У водних розчинах завжди сферичні міцели формуються само-агрегацією амфіфільного ди-блоку типу АВ або три-блоку типу АВС,коли довжина одного гідрофільного блоку перевищує в деякій мірі довжину гідрофобного блоку. Але, якщо довжина гідрофільного блоку занадто велика, кополімери знаходяться у воді як індивідуальні молекули (мономери) ,і молекули з розтягнутими гідрофобними блоками утворюють різні структури. Приклади різних амфіфільних кополімерів ,що були досліджені для утворення міцел показані у Таблиці 2.